Clear Sky Science · es
La señalización de guanosina monofosfato cíclico-proteína quinasa G atenúa la calcificación de la válvula aórtica mediante la autofagia mediada por ULK1
Por qué importa la “oxidación” de las válvulas cardiacas
A medida que las personas envejecen, la válvula aórtica —la principal puerta de salida del corazón— puede volverse rígida y recubrirse lentamente de calcio, una condición denominada enfermedad calcificada de la válvula aórtica. Esta “endurecimiento” obliga al corazón a bombear con más esfuerzo y puede provocar dolor torácico, desmayos, insuficiencia cardíaca o la necesidad de reemplazo valvular mediante cirugía. Hoy en día no existe un fármaco que desacelere este proceso de forma fiable; los médicos solo pueden esperar hasta que la válvula esté gravemente dañada y entonces operar. Este estudio explora una vía celular intrínseca que parece proteger a la válvula frente a la calcificación y prueba un fármaco moderno para insuficiencia cardíaca como posible manera de reactivar esa protección.
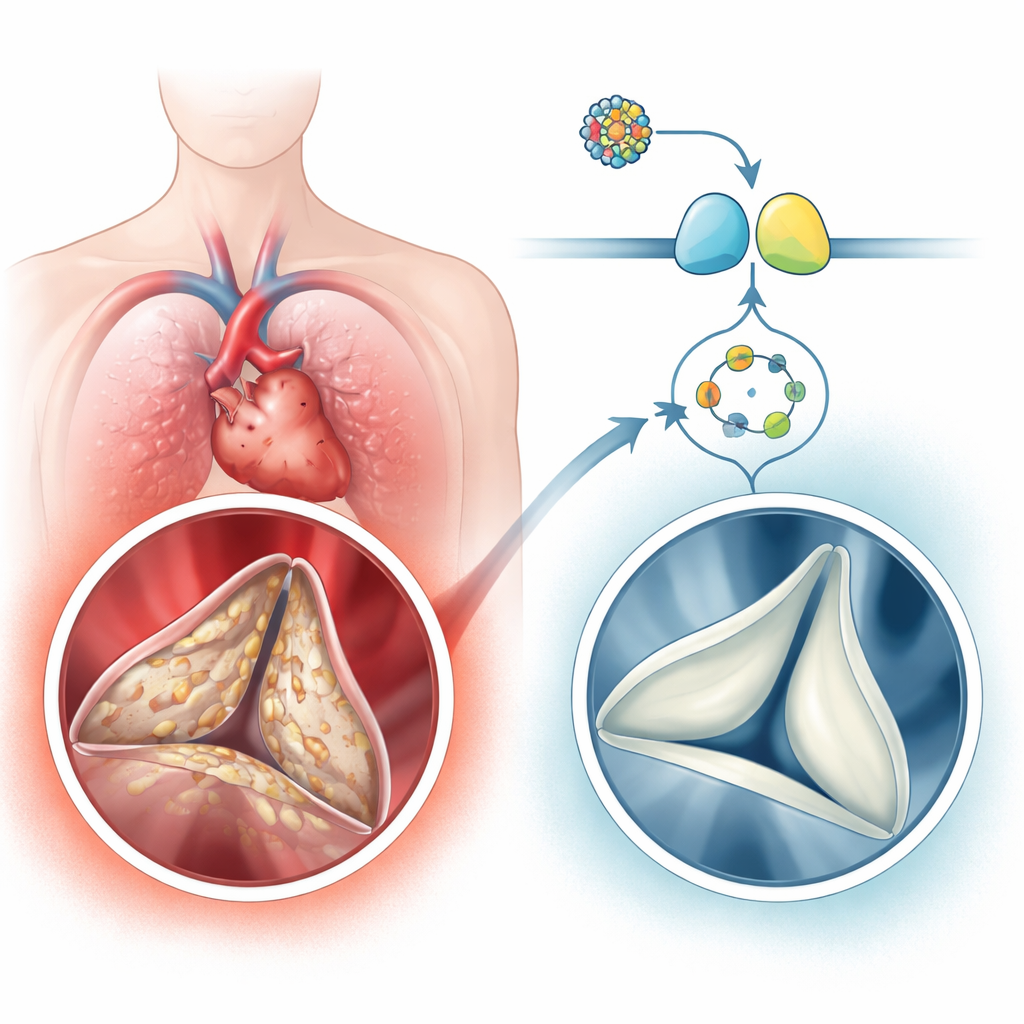
Un problema cardiaco común pero subestimado
La enfermedad calcificada de la válvula aórtica es sorprendentemente frecuente en adultos mayores, afectando a algunos porcentajes de personas mayores de 65 años y hasta a una de cada diez mayores de 75. La enfermedad no es simplemente un “desgaste” pasivo. En su lugar, las células del tejido conectivo blando de la válvula, conocidas como células intersticiales valvulares, pasan a estados de reparación y a fenotipos semejantes al hueso. Depositan colágeno adicional y luego calcio, convirtiendo las valvas antes flexibles en aletas rígidas como piedra. Los autores analizaron tejido valvular humano y grandes conjuntos de datos de expresión génica y encontraron que una vía de señalización centrada en una molécula pequeña llamada cGMP y su enzima asociada, la proteína quinasa G (PKG), estaba consistentemente disminuida en válvulas calcificadas, mientras que los genes y proteínas vinculados a la formación ósea estaban aumentados. Las personas con calcificación valvular severa también tenían niveles más bajos de cGMP en sangre, que se correlacionaban con el grado de estrechamiento y obstrucción valvular.
Una señal protectora que desaparece
Para investigar causa y efecto, el equipo usó ratones y células valvulares humanas en cultivo. Ratones diseñados para producir menos PKG desarrollaron valvas más gruesas y fuertemente calcificadas tras una lesión controlada de la válvula aórtica, y sus válvulas mostraron niveles más altos de una proteína maestra de formación ósea. En células valvulares humanas cultivadas en condiciones que favorecen la acumulación de calcio, reducir la PKG con herramientas genéticas aceleró este cambio hacia un fenotipo óseo. Estos resultados sugieren que la señalización cGMP‑PKG normalmente actúa como un freno sobre la reprogramación celular perjudicial en la válvula —y cuando ese freno se debilita, la calcificación se acelera.
Reutilizando un fármaco para insuficiencia cardíaca
Los investigadores preguntaron entonces si potenciar esta vía podría frenar o revertir la calcificación. Probaron tres medicamentos que aumentan cGMP por distintos mecanismos, incluido el vericiguat, un fármaco aprobado para ciertos pacientes con insuficiencia cardíaca. En células valvulares humanas, los tres fármacos redujeron los depósitos de calcio y los marcadores de cambio hacia un fenotipo óseo, siendo el vericiguat el que mostró el efecto más fuerte. Vericiguat también disminuyó la calcificación en pequeños fragmentos de tejido valvular humano mantenidos vivos fuera del cuerpo. En dos modelos murinos —uno impulsado por una dieta alta en colesterol y otro por lesión mecánica de la válvula—, el tratamiento diario con vericiguat condujo a valvas más finas y menos calcificadas y a mejor flujo sanguíneo a través de la válvula, sin debilitar la fuerza de contracción del corazón. Sin embargo, cuando la PKG se redujo genéticamente, el vericiguat perdió en gran medida sus beneficios, lo que indica que la PKG es la pieza clave aguas abajo.
Limpieza celular, válvulas más sanas
Al profundizar, el equipo observó que vericiguat y la PKG protegían las diminutas centrales energéticas de las células valvulares, las mitocondrias. Bajo condiciones calcificantes, las células acumulaban especies reactivas de oxígeno dañinas, perdían el potencial de membrana mitocondrial y producían menos energía. Vericiguat restauró el rendimiento mitocondrial y redujo el estrés oxidativo. Mapas a gran escala de proteínas y de sitios fosforilados les apuntaron hacia la autofagia —el sistema celular de limpieza y reciclaje interno. En válvulas humanas calcificadas, la imagen microscópica y los marcadores proteicos mostraron una reducción en la formación y actividad de los autofagosomas, las “bolsas de basura” de la autofagia. En análisis a nivel de célula única, varios subtipos de células valvulares de válvulas enfermas mostraron una supresión generalizada de los programas relacionados con la autofagia. En células en cultivo, bloquear la autofagia eliminó el efecto protector de la activación de PKG, lo que implica que la PKG actúa en gran parte reactivando este sistema de limpieza.
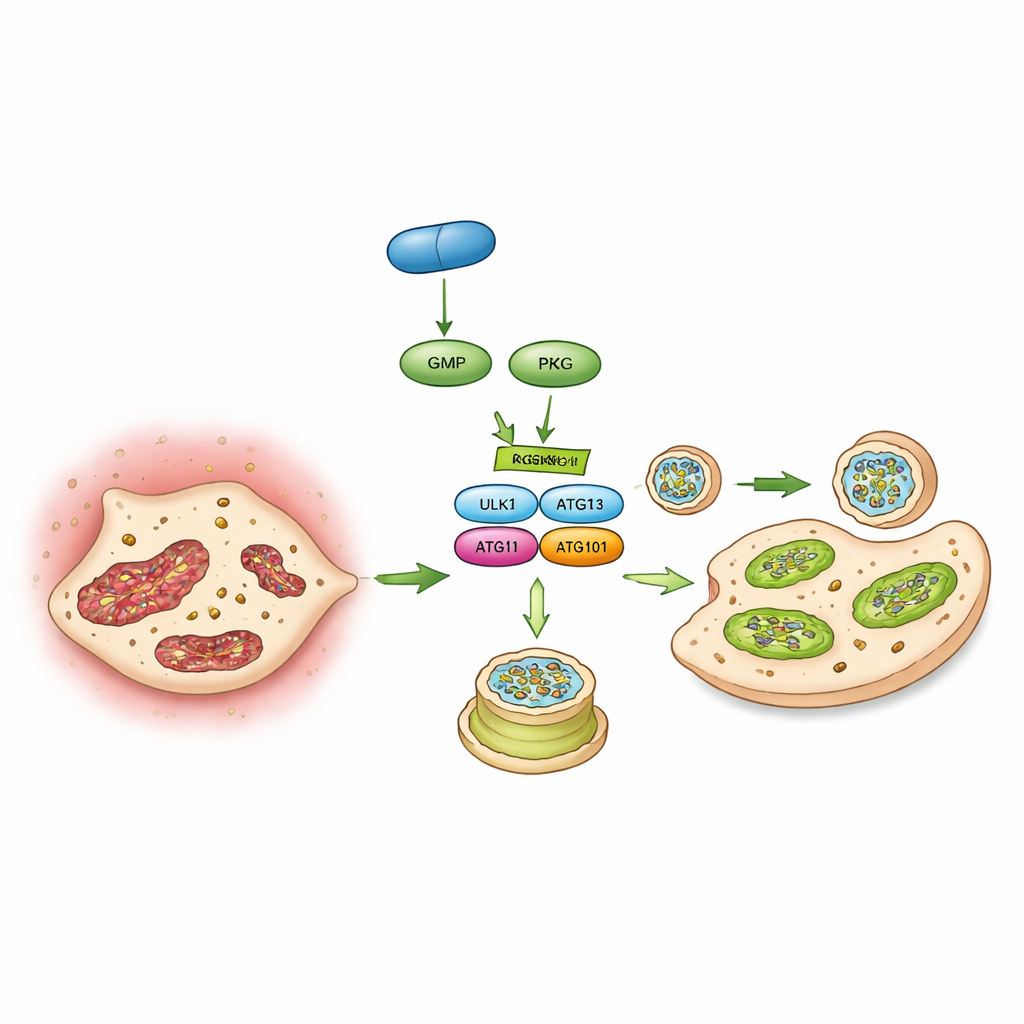
Activando un interruptor molecular
Finalmente, los autores identificaron un interruptor molecular específico que enlaza la PKG con la autofagia: una proteína llamada ULK1 que inicia la formación de autofagosomas. Mediante fosfoproteómica, estudios de interacción y ensayos de cinasa in vitro, demostraron que la PKG añade directamente un grupo fosfato a ULK1 en un sitio particular (un aminoácido llamado serina 556). Cuando ese sitio se mutó para que no pudiera ser modificado, la PKG ya no pudo aumentar la autofagia ni bloquear la calcificación en células valvulares. En ratones, forzar la expresión de esta variante de ULK1 no receptiva en las células valvulares también anuló la capacidad protectora del vericiguat. En conjunto, estos hallazgos delinean una cadena de eventos: el vericiguat estimula el cGMP, que activa la PKG, que acciona el interruptor ULK1, que reactiva la autofagia, preserva las mitocondrias y evita que las células valvulares se conviertan en formadoras de hueso.
Qué podría significar esto para los pacientes
Este trabajo sitúa al eje cGMP–PKG–ULK1–autofagia como un sistema de defensa intrínseco contra la “oxidación” de la válvula aórtica. En la enfermedad valvular calcificada, esa defensa se ve atenunada, lo que permite que las células acumulen daño y se desplacen hacia una identidad semejante al hueso. Al restaurar farmacológicamente la señal con un fármaco ya utilizado en clínicas de insuficiencia cardíaca, los investigadores ralentizaron la calcificación en varios modelos experimentales. Aunque serán necesarios ensayos en humanos con enfermedad valvular, el estudio propone una idea clara y comprobable: potenciar cuidadosamente esta vía de limpieza celular podría algún día retrasar o reducir la necesidad de reemplazo valvular en adultos mayores en riesgo de estenosis aórtica.
Cita: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Palabras clave: enfermedad calcificada de la válvula aórtica, señalización cGMP PKG, vericiguat, autofagia, calcificación de las válvulas cardiacas