Clear Sky Science · es
SHR-A1811, un nuevo conjugado anticuerpo‑fármaco dirigido a HER2, en tumores sólidos avanzados (HORIZON‑X): un ensayo global de fase 1
Nueva esperanza para personas con pocas opciones
Para muchas personas con cáncer avanzado, los tratamientos estándar acaban dejando de funcionar y quedan pocas opciones buenas. Este estudio evalúa un nuevo tipo de fármaco dirigido llamado SHR‑A1811 en pacientes cuyos tumores presentan copias extras o mutaciones de una señal de crecimiento conocida como HER2. Estos pacientes ya habían recibido varias rondas de terapia. La gran pregunta era si este medicamento experimental podía reducir los tumores durante un tiempo prolongado sin provocar efectos secundarios peligrosos.
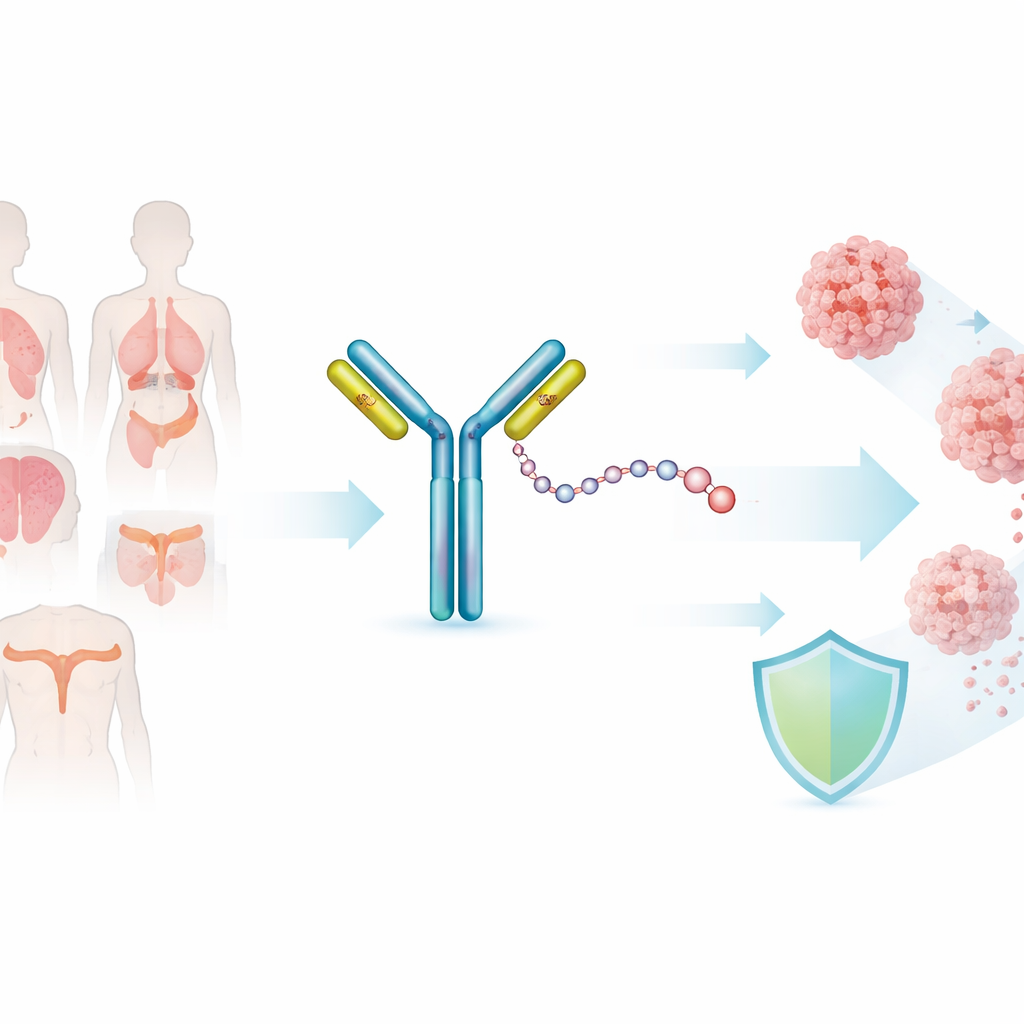
Un misil inteligente dirigido a las células cancerosas
SHR‑A1811 pertenece a una clase más reciente de medicamentos denominados conjugados anticuerpo‑fármaco, a veces descritos como «misiles inteligentes». Una parte del fármaco es un anticuerpo que reconoce HER2, una proteína presente en niveles altos en algunas células cancerosas. La otra parte es una quimioterapia muy potente que resulta demasiado tóxica para administrarse por sí sola. Un enlazador químico especial une estas piezas. La idea es que el anticuerpo lleve la carga tóxica directamente a las células tumorales marcadas por HER2, donde se libera en el interior del cáncer, protegiendo en gran medida a los tejidos sanos.
Quién recibió el nuevo tratamiento
Este ensayo global de fase 1 reclutó a 396 adultos con tumores sólidos avanzados o metastásicos en 38 hospitales. Todos los tumores producían HER2 en exceso o presentaban mutaciones en HER2. La mayoría de los pacientes tenían cáncer de mama, pero también hubo pacientes con cáncer de vías biliares, vejiga, ovario y útero, colon, estómago, pulmón, páncreas y otros. De media, los pacientes ya habían recibido tres o cuatro regímenes de tratamiento previos por enfermedad metastásica, lo que indica que sus cánceres eran difíciles de controlar. SHR‑A1811 se administró por infusión intravenosa cada tres semanas en dosis variables para identificar una dosis adecuada y vigilar la seguridad y las primeras señales de eficacia.
Equilibrando efectos secundarios y seguridad
Casi todos los pacientes experimentaron algún efecto secundario, como es esperable con fármacos anticancerosos potentes. Los problemas más comunes fueron descensos en las cifras sanguíneas, incluidos glóbulos blancos, glóbulos rojos y plaquetas, lo que puede aumentar el riesgo de infecciones y provocar fatiga o aparición de hematomas. Por lo general se pudieron manejar con ajustes de dosis, y solo alrededor de uno de cada diez pacientes interrumpió el tratamiento por efectos secundarios. Una preocupación importante de seguridad para fármacos similares es la aparición de fibrosis e inflamación pulmonar, que puede ser potencialmente mortal. En este estudio, los problemas pulmonares de cualquier gravedad ocurrieron solo en el 2,5% de los pacientes, mayoritariamente leves; solo un paciente falleció por esta complicación en la dosis más alta. En conjunto, el perfil de seguridad se mantuvo estable durante más de dos años de seguimiento, sin que surgieran riesgos nuevos o inesperados.
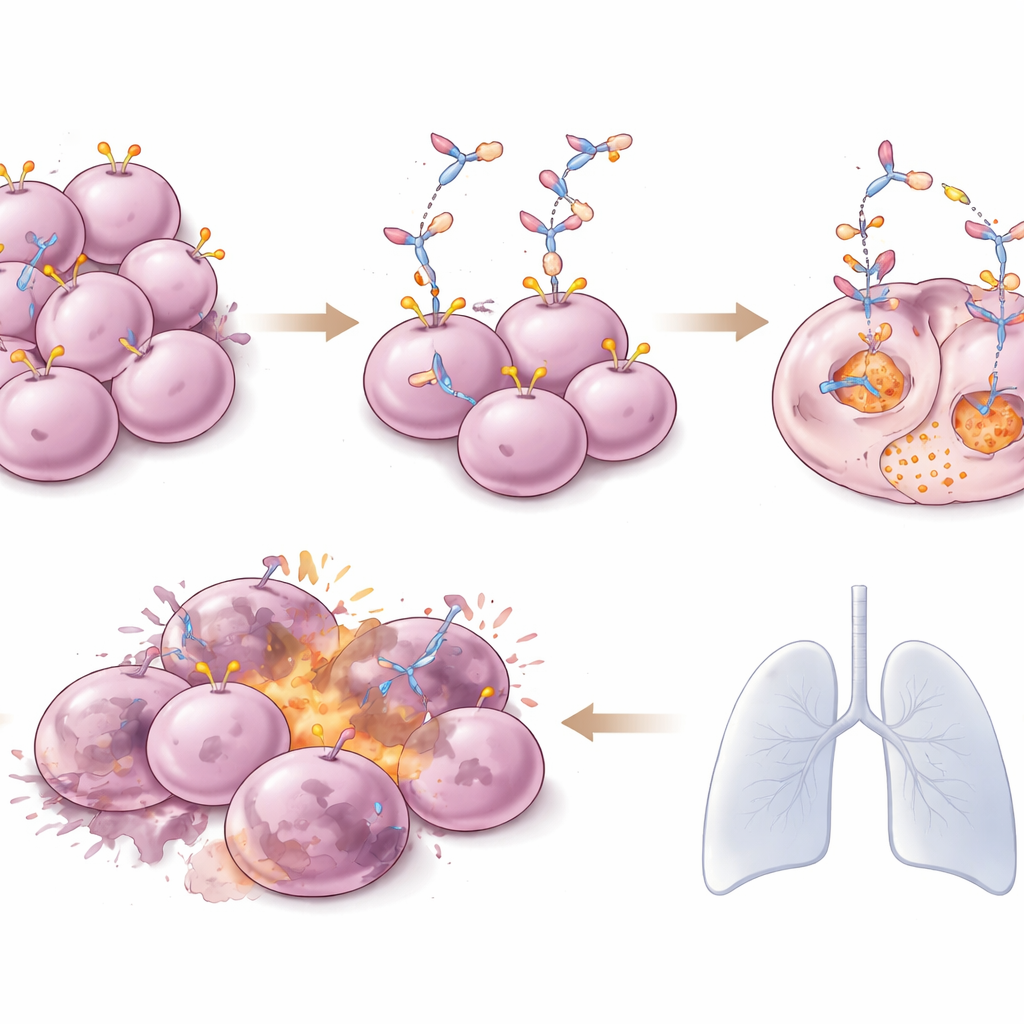
Reducción tumoral y control duradero
Los resultados sobre el control tumoral fueron llamativos para pacientes tan pretratados. En todos los tipos tumorales, casi el 60% de los pacientes vieron reducirse sus tumores, y algunos lograron la desaparición completa de la enfermedad visible en las pruebas de imagen. En personas con cáncer de mama HER2‑positivo, alrededor de cuatro de cada cinco presentaron reducción tumoral, y el tiempo típico hasta que el cáncer empezó a crecer de nuevo fue algo más de dos años. Los pacientes con niveles más bajos de HER2 en sus tumores mamarios también se beneficiaron, con un control de la enfermedad que duró cerca de un año de media. En tumores no mamarios —incluidas vías biliares, vejiga, ginecológicos, colorrectales, estómago y pulmón— las respuestas variaron pero fueron en general alentadoras, con muchos pacientes disfrutando de varios meses adicionales de control de la enfermedad. Es importante destacar que las respuestas tendieron a mantenerse: entre quienes vieron reducción tumoral, muchos conservaron el beneficio durante un año o más.
Alcanzando tumores con poca expresión del blanco
Un hallazgo intrigante fue que SHR‑A1811 ayudó a algunos pacientes cuyos tumores tenían muy poco HER2 detectable —niveles tradicionalmente considerados demasiado bajos para la terapia dirigida a HER2. En este grupo, más de la mitad todavía vio reducción tumoral, y el control de la enfermedad duró alrededor de diez meses. Estudios de laboratorio sugieren que esto puede ocurrir porque la carga tóxica, una vez liberada dentro de una célula marcada por HER2, puede filtrarse a las células cancerosas vecinas que no presentan mucho HER2, un llamado «efecto espectador». Esto plantea la posibilidad de que el fármaco pueda beneficiar a una gama más amplia de pacientes de lo que las definiciones clásicas de HER2‑positivo indicarían.
Qué significa esto para las personas con cáncer avanzado
En conjunto, este seguimiento a largo plazo del ensayo HORIZON‑X muestra que SHR‑A1811 puede proporcionar un control tumoral potente y duradero en muchos pacientes cuyos cánceres relacionados con HER2 ya habían resistido múltiples tratamientos, manteniendo al mismo tiempo los efectos secundarios graves —especialmente el daño pulmonar— relativamente infrecuentes. Aunque no se trató de una comparación directa, los resultados parecen al menos comparables a un «misil inteligente» dirigido a HER2 ya aprobado, y en ocasiones más favorables, especialmente en seguridad. Aún se necesitan ensayos más amplios y aleatorizados, pero la evidencia hasta ahora sugiere que SHR‑A1811 podría convertirse en una nueva opción importante para personas con cánceres impulsados por HER2 difíciles de tratar.
Cita: Yao, H., Yan, M., Tong, Z. et al. SHR-A1811, a novel HER2-targeting antibody-drug conjugate, in advanced solid tumors (HORIZON-X): a global phase 1 trial. Sig Transduct Target Ther 11, 104 (2026). https://doi.org/10.1038/s41392-026-02612-9
Palabras clave: Terapia dirigida a HER2, conjugado anticuerpo‑fármaco, cáncer de mama metastásico, tumores sólidos, ensayo clínico