Clear Sky Science · es
Señalización fibrinógeno–Bmal1 como diana terapéutica para limitar la disección aórtica preservando la contractilidad de las CMLV
Por qué importa el guardián oculto de la aorta
La disección aórtica es una de las emergencias más temidas en medicina: la arteria principal que sale del corazón puede rasgarse de repente, a menudo sin aviso, y muchos pacientes mueren en pocas horas. La cirugía puede salvar vidas, pero es arriesgada y no siempre es posible de inmediato. Este estudio explora a un aliado inesperado ya circulando en nuestra sangre—el fibrinógeno, una proteína de la coagulación—y muestra que, además de ayudar a detener el sangrado, podría contribuir a mantener la integridad de la aorta y ralentizar la enfermedad, potencialmente dando a los médicos tiempo valioso para actuar.
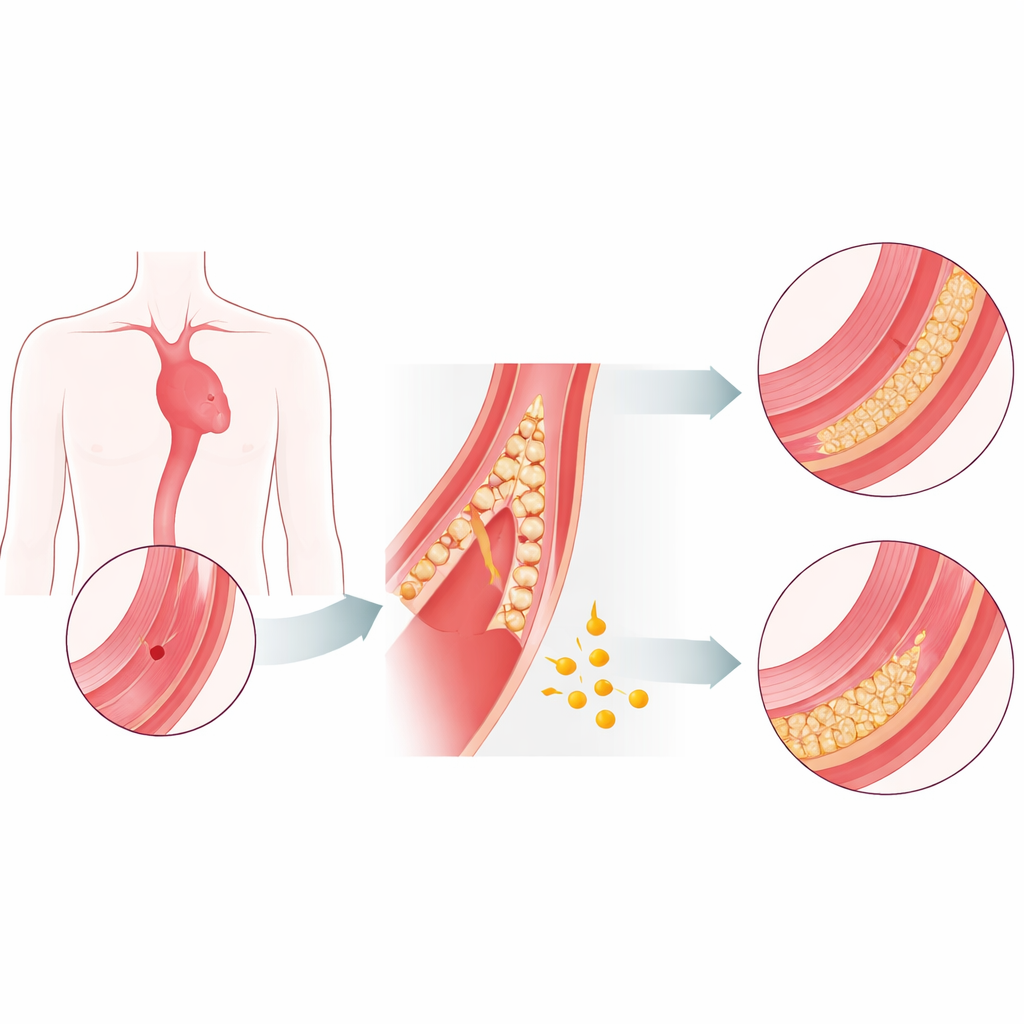
Un asesino silencioso que necesita nuevas opciones
La aorta está construida como una manguera resistente y en varias capas. Cuando sus capas internas se debilitan y se separan, la sangre puede infiltrarse en la pared y desgarrarla: esto es una disección aórtica. En la fase inicial peligrosa, el riesgo de morir aumenta hora tras hora, y la cirugía de urgencia suele ser la única opción. Los pacientes que sobreviven el tiempo suficiente para alcanzar una fase crónica más estable tienden a tener un pronóstico mucho mejor. Hoy no existen fármacos probados que ralenticen de forma fiable el proceso de desgarro o refuercen la pared aórtica. Los autores se propusieron averiguar si el fibrinógeno, una proteína sanguínea común conocida sobre todo por su papel en la coagulación, podría también actuar como un estabilizador natural de la aorta.
Pistas de los pacientes: más fibrinógeno, mejor supervivencia
El equipo examinó primero a 310 pacientes con disección aórtica aguda que no pudieron ser operados y fueron tratados solo con medicamentos. Compararon a los que sobrevivieron su estancia hospitalaria con los que no. Los pacientes que murieron solían presentar niveles mucho más bajos de fibrinógeno en sangre. Al agrupar a los pacientes por nivel de fibrinógeno, encontraron que niveles muy bajos (por debajo de 2 gramos por litro) se asociaban a tasas de mortalidad mucho más altas, mientras que niveles elevados (por encima de 4 gramos por litro) se vinculaban a una mejor supervivencia. Este patrón sugirió que el fibrinógeno no era solo un espectador, sino que podría estar ayudando a la aorta a resistir desgarros adicionales.
Observar cómo la aorta se rompe y se repara en ratones
Para ir más allá de la asociación y probar causalidad, los científicos usaron modelos murinos en los que la aorta puede debilitarse y diseccionarse. En estos animales, el fibrinógeno normalmente estaba ausente de la pared aórtica sana, pero a medida que la enfermedad se desarrollaba, comenzó a filtrarse en la capa media donde residen las células del músculo liso. De forma llamativa, la mayor acumulación de fibrinógeno apareció en segmentos gravemente dañados pero aún no rotos, lo que sugería que su presencia podría ayudar a evitar que la pared cediera finalmente. Cuando los investigadores utilizaron terapia génica para reducir la producción de fibrinógeno en el hígado, las disecciones empeoraron: las aortas se dilataron más, el daño estructural aumentó y murieron más ratones. La administración de fibrinógeno purificado revirtió estos efectos. Experimentos independientes usando un modelo distinto de aneurisma aórtico mostraron una tendencia protectora similar, reforzando la hipótesis de que el fibrinógeno protege activamente la pared vascular.
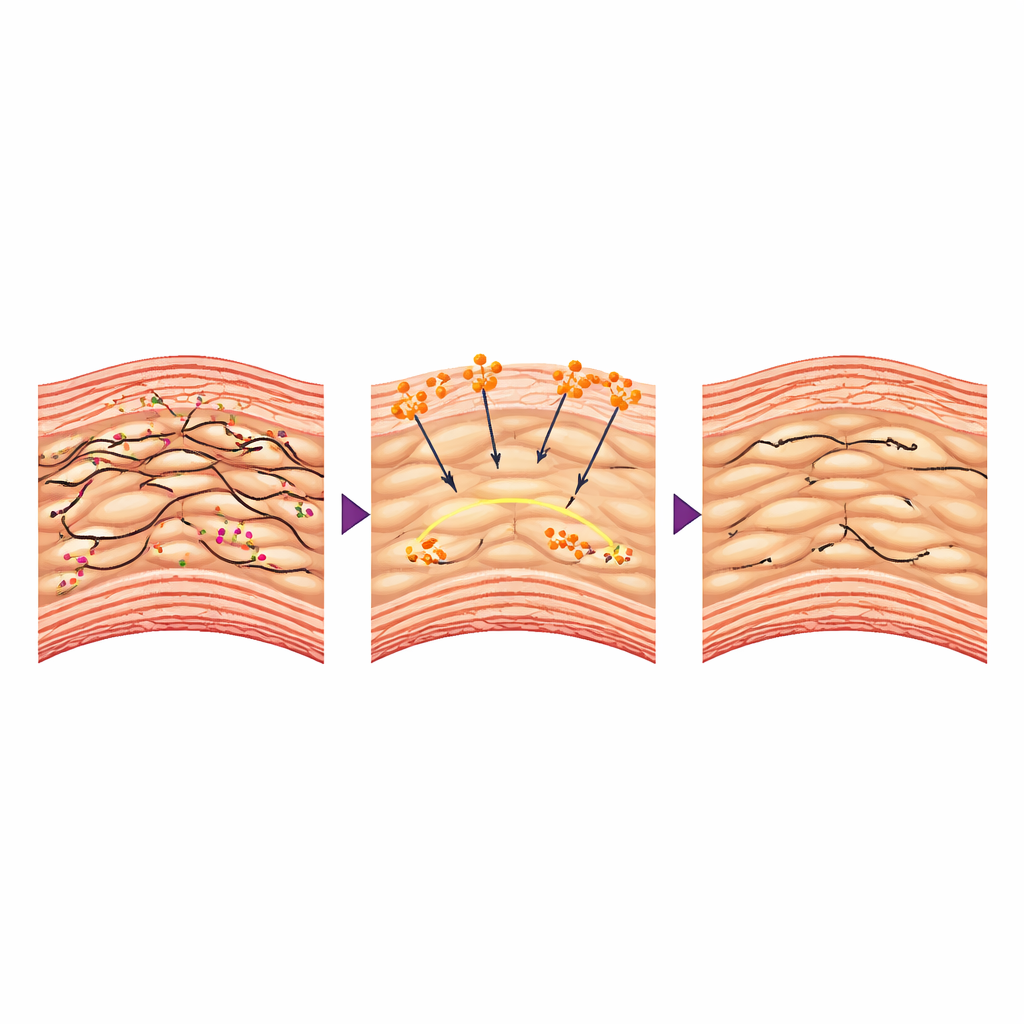
El diálogo oculto entre la proteína sanguínea y las células musculares
¿Cómo podría una proteína de la coagulación proteger la aorta desde el interior? Los autores se centraron en las células del músculo liso vascular, las células contráctiles que forman la capa media de la aorta y actúan como sus “anillos de refuerzo” vivos. En la enfermedad, estas células a menudo pierden su estado contráctil firme y cambian a una forma más laxa y sintética que degrada el tejido circundante. El estudio encontró que cuando el fibrinógeno entraba en la pared aórtica, interactuaba con receptores específicos en estas células y ayudaba a preservar su andamiaje interno de filamentosa actina. Las células del músculo liso de animales tratados eran más rígidas, se contraían con mayor fuerza en pruebas y expresaban más marcadores “contractiles” y menos proteínas que degradan la matriz de sostén. A nivel genético, el fibrinógeno atenuó la actividad de Bmal1, un regulador maestro vinculado al reloj corporal, que en este contexto promovía cambios nocivos en el comportamiento de las células musculares. Forzar la recuperación de Bmal1 anuló los beneficios del fibrinógeno, demostrando que esta vía de señalización era central para el efecto protector.
Del mecanismo al posible tratamiento
Puesto que el fibrinógeno también impulsa la coagulación, el equipo investigó si su beneficio se debía simplemente a formar coágulos más sólidos. Usando un anticoagulante potente para bloquear la trombina—la enzima que convierte el fibrinógeno en un coágulo sólido—demostraron que el fibrinógeno seguía protegiendo la aorta incluso cuando la formación de coágulos estaba mayormente deshabilitada. Finalmente, probaron distintas dosis y hallaron que solo cantidades suficientemente altas de fibrinógeno añadido ralentizaban la enfermedad, reducían las roturas y preservaban la estructura tisular. En conjunto, estos hallazgos presentan al fibrinógeno como una molécula de doble propósito: en niveles más altos, el fibrinógeno intacto puede penetrar en una pared aórtica debilitada, calmar una vía de señalización nociva en las células del músculo liso y ayudar a que permanezcan fuertes y contractiles. Para los pacientes, esto plantea la posibilidad de que infusiones de fibrinógeno cuidadosamente dosificadas puedan algún día actuar como un tratamiento farmacológico para ralentizar la disección aórtica y ampliar de forma segura la ventana para una cirugía programada que salve vidas.
Cita: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
Palabras clave: disección aórtica, fibrinógeno, células del músculo liso vascular, señalización Bmal1, aneurisma aórtico