Clear Sky Science · es
M6A-modificado circArhgap26 atenúa la lesión por isquemia‑reperfusión cardíaca suprimiendo la palmitoilación de plakophilina-1
Por qué importa proteger el corazón tras un infarto
Cuando una persona sufre un infarto, los médicos se apresuran a reabrir la arteria bloqueada y restablecer el flujo sanguíneo. Este paso de rescate salva vidas, pero también tiene un lado oscuro: el retorno súbito de la sangre puede dañar aún más el corazón, un problema conocido como lesión por isquemia–reperfusión. El estudio resumido aquí explora un defensor natural inesperado dentro de las células cardíacas: una pieza circular de ARN llamada circArhgap26 que ayuda a proteger el músculo cardíaco de esta segunda oleada de daño. Comprender cómo actúa esta pequeña molécula podría señalar nuevas vías para tratamientos y análisis de sangre para personas con enfermedad cardíaca.
Un círculo oculto en el guion genético del corazón
La mayoría pensamos en los genes como hebras rectas de ADN y ARN, pero las células también producen moléculas de ARN en forma de anillo, llamadas ARN circulares, que son inusualmente estables y pueden afinar muchos procesos celulares. Los investigadores buscaron en corazones de ratón ARNs circulares que cambian durante la lesión cardíaca y se centraron en uno, circArhgap26, cuyos niveles caían bruscamente cuando se interrumpía y luego se restauraba el flujo sanguíneo. Confirmaron que este ARN circular forma un bucle cerrado, se encuentra principalmente en el compartimento líquido de la célula y no sirve como plantilla para producir una proteína. En cambio, parece actuar como regulador, interactuando con otras moléculas para influir en si una célula cardíaca sobrevive o muere tras el estrés. 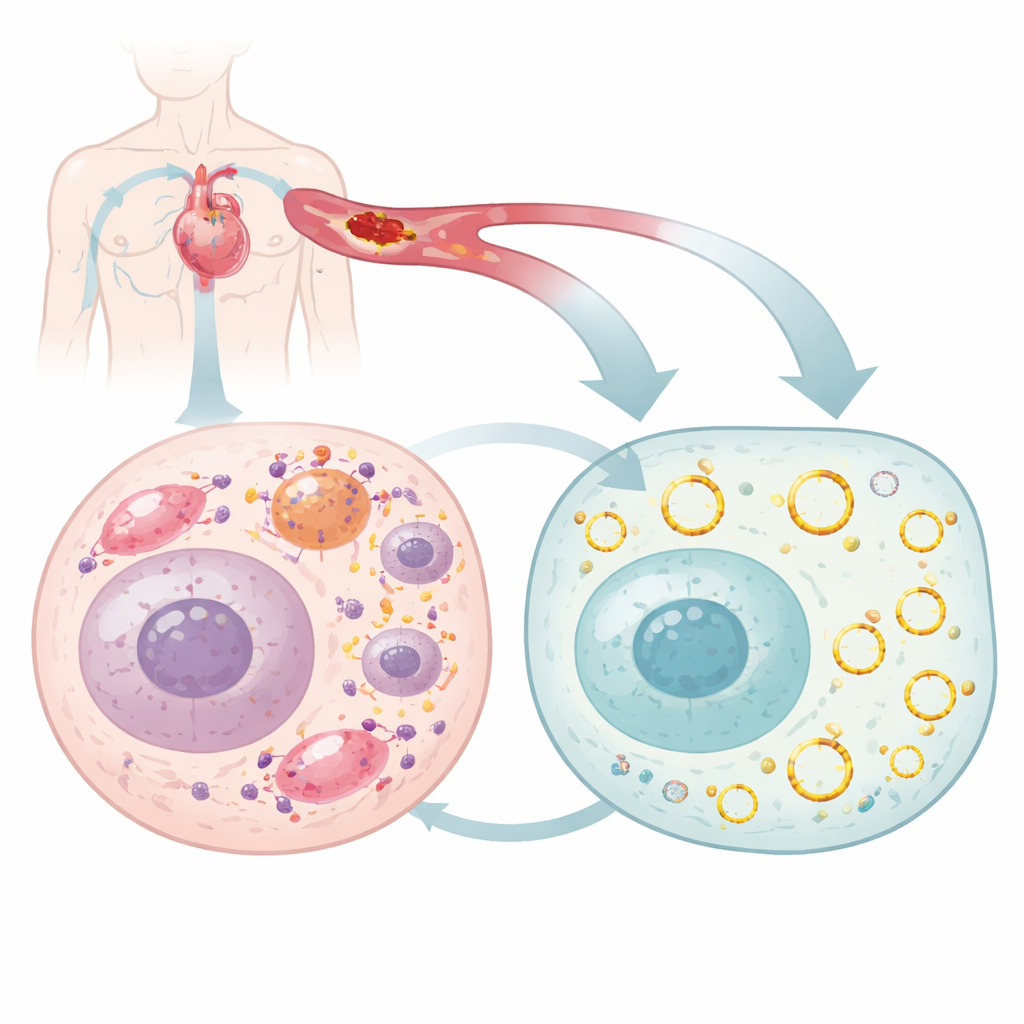
Prueba de que el ARN circular protege el corazón
Para ver qué hace realmente circArhgap26, el equipo aumentó o redujo sus niveles en corazones de ratón. Cuando usaron un virus para elevar circArhgap26 específicamente en las células del músculo cardíaco, los animales sometidos a una oclusión temporal de una arteria coronaria seguida de la restauración del flujo sanguíneo mostraron una contractilidad más fuerte, áreas dañadas menores y menos células moribundas. Los marcadores clásicos de lesión en sangre y tejido cardíaco también fueron más bajos. Lo contrario ocurrió cuando se silenció el ARN circular: incluso sin un infarto inducido, la función cardíaca empeoró y la muerte celular aumentó, y estos problemas se hicieron más graves al añadirse la isquemia–reperfusión. Efectos protectores similares aparecieron en células de tipo cardíaco humanas en laboratorio, lo que sugiere que el mecanismo está conservado entre ratones y personas.
Una proteína asociada dañina puesta bajo control
Indagando más a fondo, los investigadores preguntaron cómo confiere esta protección circArhgap26. Utilizando técnicas bioquímicas de “pesca”, encontraron que se une directamente a una proteína estructural llamada plakophilina‑1 (PKP1), que puede influir en cuán fuertemente se adhieren las células entre sí y en su propensión a sufrir muerte programada. En corazones lesionados y en células cardíacas estresadas, los niveles de PKP1 aumentaron y se asociaron con un daño mayor. Silenciar PKP1 alivió la lesión cardíaca y la muerte celular, mientras que forzar su producción empeoró los resultados. Cuando circArhgap26 se incrementó, la cantidad de proteína PKP1 disminuyó aunque la actividad génica no cambió, lo que apunta a un punto de control posterior a la síntesis del ARN mensajero. Experimentos mostraron que circArhgap26 acelera la degradación de la proteína PKP1 interfiriendo con un proceso de modificación lipídica llamado palmitoilación que normalmente estabiliza a PKP1.
Un tira y afloja molecular sobre las señales de muerte celular
La palmitoilación la llevan a cabo una familia de enzimas; una en particular, ZDHHC1, fue identificada como la que agrega grupos grasos a PKP1 y lo hace más duradero. CircArhgap26 se une a PKP1 en la misma región usada por ZDHHC1, creando un tira y afloja molecular. Cuando el ARN circular gana, PKP1 recibe menos etiquetas grasas, se vuelve menos estable y se elimina más rápidamente. Esto produce un efecto en cascada: PKP1 normalmente potencia la producción de otra proteína, APAF1, al interactuar con un segmento regulador de su ARN. APAF1 es una pieza clave de la maquinaria que activa las enzimas caspasa‑9 y caspasa‑3, los ejecutores centrales de la muerte celular. Con PKP1 menos estable, la producción de proteína APAF1 disminuye, la cascada señalizadora de la muerte se atenúa y las células cardíacas tienen más probabilidades de sobrevivir al estrés del restablecimiento del flujo sanguíneo. 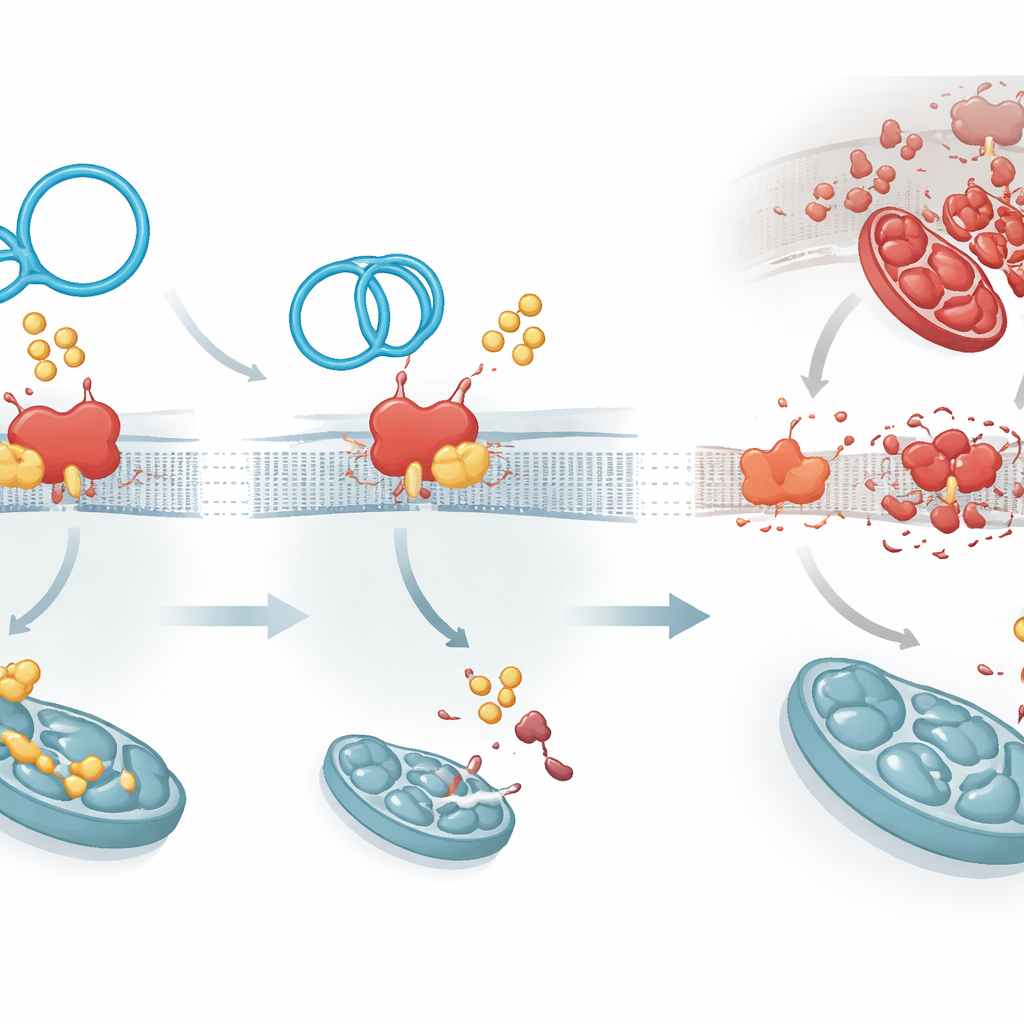
Ajustando el círculo y su promesa para los pacientes
El estudio también revela cómo se reduce circArhgap26 durante la lesión. Una marca química común en el ARN, llamada m6A, se acumula en este ARN circular en corazones estresados. Una proteína lectora llamada YTHDF2 reconoce esta marca y promueve la degradación de circArhgap26, debilitando la defensa natural del corazón precisamente cuando más se necesita. Es importante que la versión humana de este ARN circular es muy similar a la del ratón y su nivel es notablemente más bajo en la sangre de pacientes sometidos a procedimientos de apertura de arterias en comparación con voluntarios sanos. En conjunto, estos hallazgos sugieren que restaurar o imitar circArhgap26 podría servir tanto como marcador sanguíneo de riesgo como terapia novedosa. En términos simples, el trabajo descubre una pequeña molécula circular que actúa como guardiana contra el daño por reperfusión al desactivar una cadena de reacciones letales dentro de las células cardíacas.
Cita: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Palabras clave: lesión por isquemia reperfusión, ARN circular, infarto de miocardio, apoptosis de cardiomiocitos, terapia basada en ARN