Clear Sky Science · es
La sinergia quimio‑fototérmica enciende la inmunidad antitumoral mediante ferroptosis
Convertir el calor y la luz del cuerpo en un arma contra el cáncer
Los fármacos quimioterapéuticos pueden reducir los tumores, pero a menudo provocan efectos secundarios severos y no siempre evitan que el cáncer reaparezca. Este estudio explora una nueva forma de hacer que un fármaco ya existente, el docetaxel, sea más eficaz e inteligente al encapsularlo en diminutas partículas sensibles al calor y activarlas con luz en el infrarrojo cercano. El objetivo no es solo matar las células tumorales con mayor precisión, sino también despertar al sistema inmunitario para que reconozca y persiga el cáncer en todo el organismo y prevenga recaídas futuras. 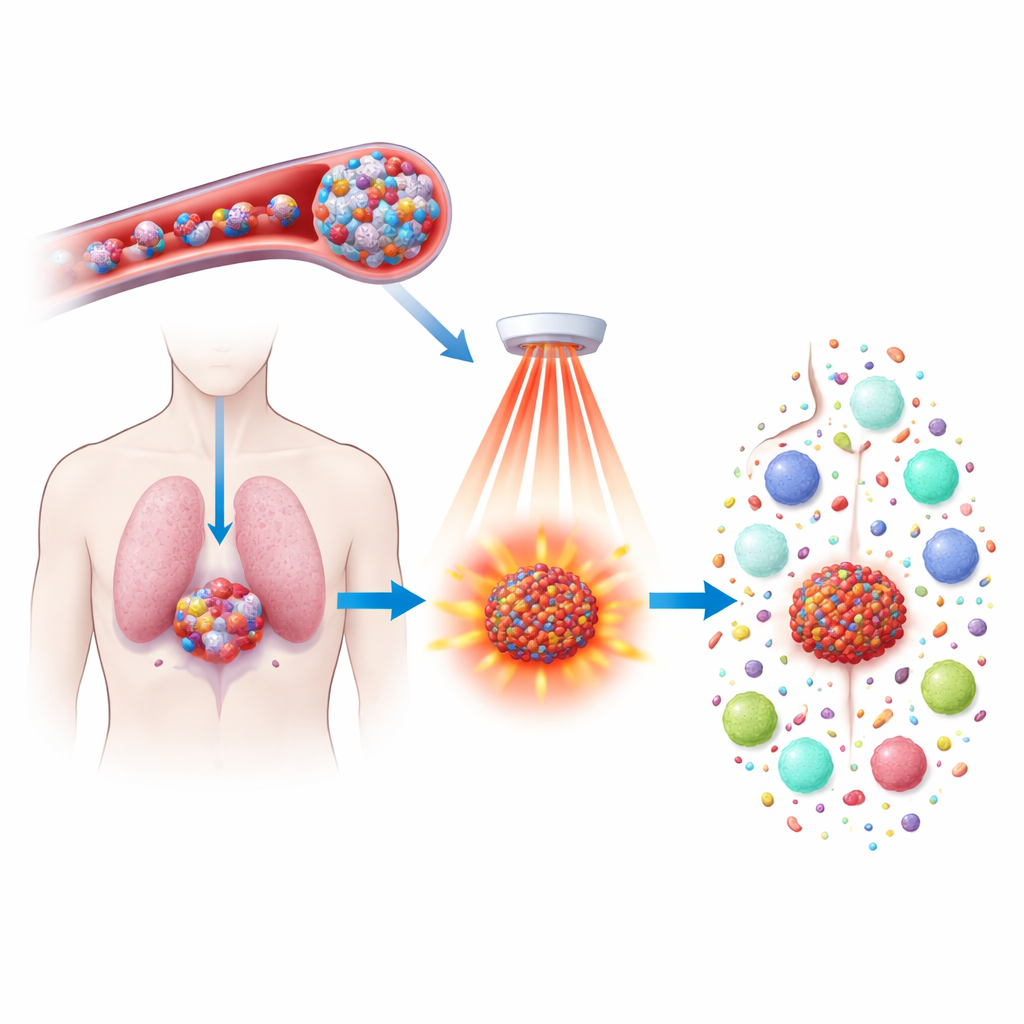
Pequeños mensajeros que saben a dónde ir
Los investigadores desarrollaron un nuevo tipo de nanopartícula a partir de un polímero que contiene ferroceno, una molécula que porta hierro y reacciona intensamente con el peróxido de hidrógeno, un oxidante presente en concentraciones más altas dentro de los tumores que en los tejidos normales. Estos polímeros se autoensamblan en esferas hidrofílicas capaces de transportar tanto docetaxel como un tinte absorbente de luz llamado IR808. Una vez inyectadas en el torrente sanguíneo, las partículas son lo bastante pequeñas y estables para circular y filtrarse en los tumores, donde los vasos sanguíneos permeables y los altos niveles de peróxido de hidrógeno empiezan a debilitar las partículas y liberar lentamente su carga. Este diseño concentra el tratamiento en los tumores y reduce el daño a los órganos sanos.
Usar luz para potenciar el daño local
Se dirige luz en el infrarrojo cercano—capaz de penetrar el tejido de forma segura—hacia la zona tumoral. El IR808 dentro de las nanopartículas absorbe esa luz y la convierte en calor, al tiempo que genera especies reactivas de oxígeno. La combinación del peróxido de hidrógeno producido por el tumor y los oxidantes generados por la luz provoca que las partículas se desintegren más rápido y liberen su carga justo donde se necesita. Al mismo tiempo, el hierro integrado en la fracción de ferroceno ayuda a convertir estos oxidantes en formas especialmente agresivas que atacan los componentes lipídicos de las membranas celulares. Este asalto químico y térmico dirigido aumenta de forma notable la capacidad de matar células en comparación con el docetaxel o el tratamiento con luz por separado. 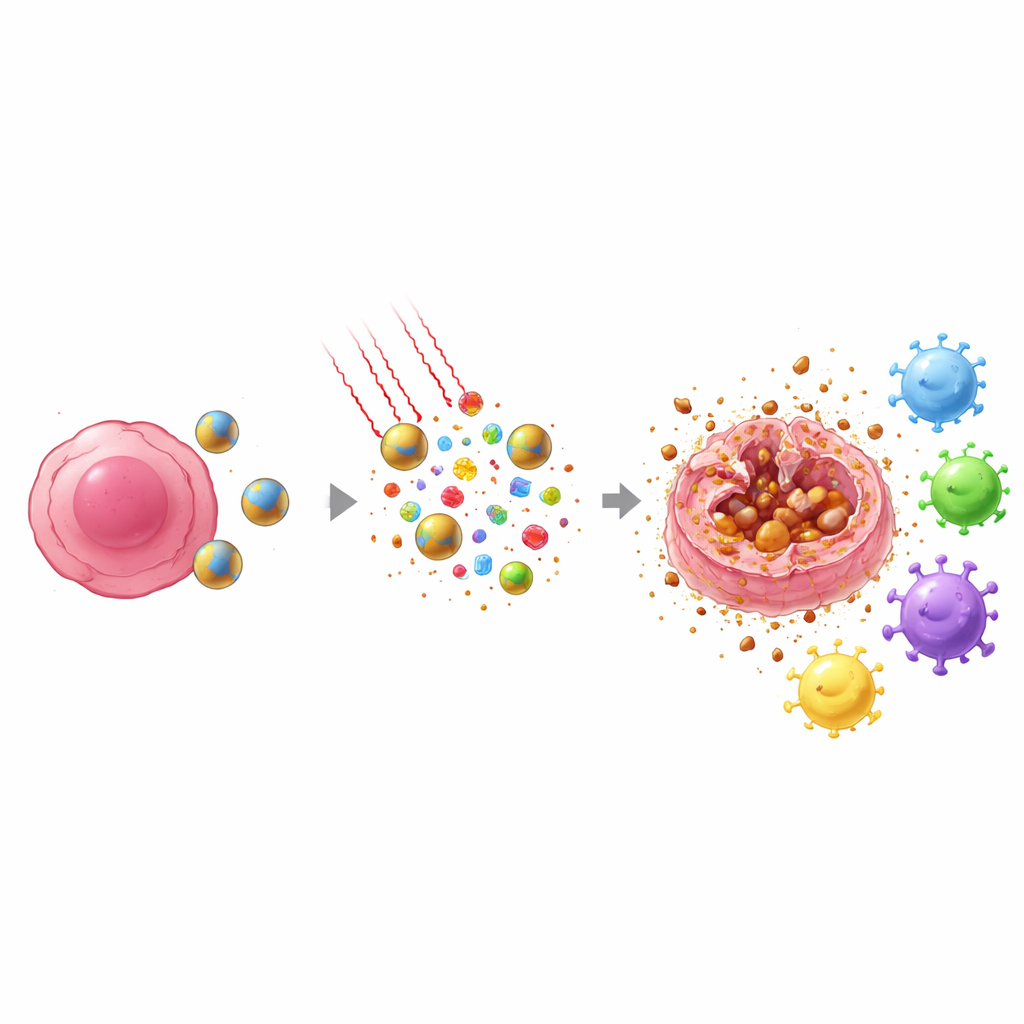
Un fuego controlado que alerta al sistema inmune
Es importante señalar que la forma en que las células tumorales mueren bajo este tratamiento difiere de la quimioterapia convencional. En lugar de descomponerse en fragmentos ordenados de manera silenciosa, muchas células experimentan un proceso llamado ferroptosis, una muerte impulsada por el hierro que daña los lípidos y provoca la ruptura de la membrana exterior. Cuando eso ocurre, las células vierten señales de alarma internas y fragmentos específicos del tumor en el entorno. Al mismo tiempo, el docetaxel empuja una proteína nuclear clave, HMGB1, hacia el borde celular, preparándola para su liberación. En conjunto, el calor, los oxidantes y la acción del fármaco generan una ráfaga de señales de peligro y antígenos que las células centinela cercanas—las células dendríticas—pueden detectar y transportar a los ganglios linfáticos.
De un ataque local a una defensa en todo el cuerpo
En modelos murinos de tumor, este tratamiento combinado quimio‑fototérmico no solo redujo los tumores directamente irradiados de forma más eficaz que cualquier componente por separado, sino que también modificó el paisaje inmunitario. Los tumores mostraron más células dendríticas maduras y un mayor número de linfocitos T citotóxicos, tanto en el propio tumor como en los ganglios linfáticos de drenaje. En algunos ratones inmunocompetentes, los tumores primarios desaparecieron tras solo dos ciclos de tratamiento. Cuando los científicos implantaron posteriormente nuevos tumores en sitios distantes o en el flanco opuesto, estos crecimientos secundarios se ralentizaron o suprimieron, lo que indica que los animales desarrollaron una forma de memoria inmune específica contra el cáncer. Añadir un anticuerpo que bloquea puntos de control y previene la extenuación de las células T redujo aún más las metástasis pulmonares y prolongó la supervivencia, lo que sugiere que este tratamiento local puede combinarse con las inmunoterapias modernas.
Por qué esto importa para la atención futura del cáncer
Para un lector no especializado, la conclusión clave es que este enfoque transforma el docetaxel de un veneno sistémico poco selectivo en parte de una estrategia anticáncer inteligente y por múltiples pasos. Al encapsular el fármaco en nanopartículas activadas por la luz y que contienen hierro y que responden a la química propia del tumor, la terapia produce más daño dentro de los tumores a la vez que preserva el tejido sano. El patrón particular de muerte celular que desencadena actúa como una vacuna desde dentro del tumor, enseñando al sistema inmunitario a reconocer y recordar el cáncer. Si estos hallazgos se traducen a humanos, tales sistemas quimio‑fototérmicos podrían ayudar a convertir tumores “fríos” resistentes en tumores “calientes” que responden mucho mejor a tratamientos basados en la inmunidad, lo que potencialmente reduciría las recaídas y mejoraría el control a largo plazo.
Cita: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Palabras clave: nanomedicina contra el cáncer, terapia fototérmica, ferroptosis, inmunoterapia contra el cáncer, administración de docetaxel