Clear Sky Science · es
Profármacos nanozima de coordinación conductiva desencadenan con precisión piroptosis, cuproptosis y ferroptosis para la vacunación in situ contra el cáncer
Convertir los tumores en sus propias vacunas
El tratamiento del cáncer suele buscar eliminar las células tumorales directamente, pero ¿y si se pudiera convertir un tumor en una vacuna contra sí mismo? Este estudio describe un «profármaco» nanoparticulado inteligente que viaja de forma segura por el cuerpo, se activa solo dentro de los tumores y entonces obliga a las células cancerosas a morir de una manera que alerta de forma potente al sistema inmunitario. El resultado no es solo la reducción del tumor primario, sino también el entrenamiento del organismo para localizar tumores distantes y metástasis.
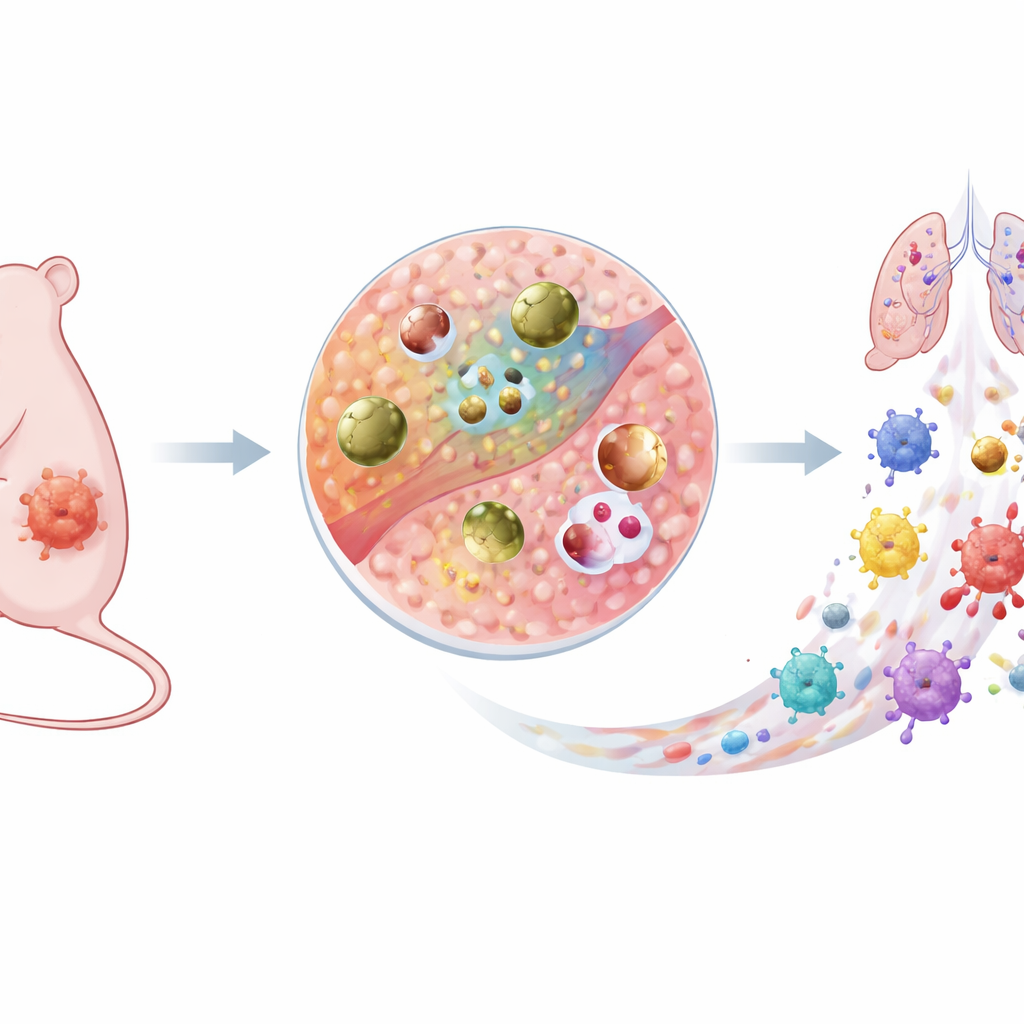
Un nuevo tipo de arma inteligente contra el cáncer
Los investigadores construyeron una pequeña partícula a base de cobre llamada Cu–DHN que se comporta como un medicamento latente durante la circulación y como un agresor contra el cáncer una vez que alcanza el tumor. Está ensamblada a partir de iones de cobre, una molécula precursora inocua (1,5-dihidroxinaftaleno, o DHN) y el aminoácido cisteína. Juntos forman una red de coordinación conductiva, lo que significa que los electrones pueden moverse con facilidad a través de la partícula. Esta «autopista de electrones» interna permite que toda la nanopartícula, no solo su superficie, participe en reacciones químicas. De forma crucial, Cu–DHN está diseñada para responder únicamente a la química inusual del microambiente tumoral, donde el glutatión antioxidante y el peróxido de hidrógeno están ambos anómalamente elevados.
Cómo la química tumoral enciende el interruptor
Dentro de los tumores, Cu–DHN actúa como una enzima artificial. En presencia simultánea de glutatión y peróxido de hidrógeno, primero utiliza el glutatión para restablecer sus iones de cobre a un estado altamente reactivo y luego emplea el peróxido de hidrógeno para generar una descarga continua de oxidantes muy agresivos (radicales hidroxilo). Estos oxidantes cumplen una doble función: dañan componentes celulares y convierten el DHN inocuo encerrado en la partícula en juglona, un compuesto anticancerígeno potente. La juglona, a su vez, suprime las propias defensas antioxidantes del tumor y aumenta aún más los niveles de peróxido de hidrógeno, creando un bucle autoamplificante de estrés oxidativo que permanece confinado al tumor, porque solo los tumores aportan las entradas químicas necesarias para iniciar el ciclo.
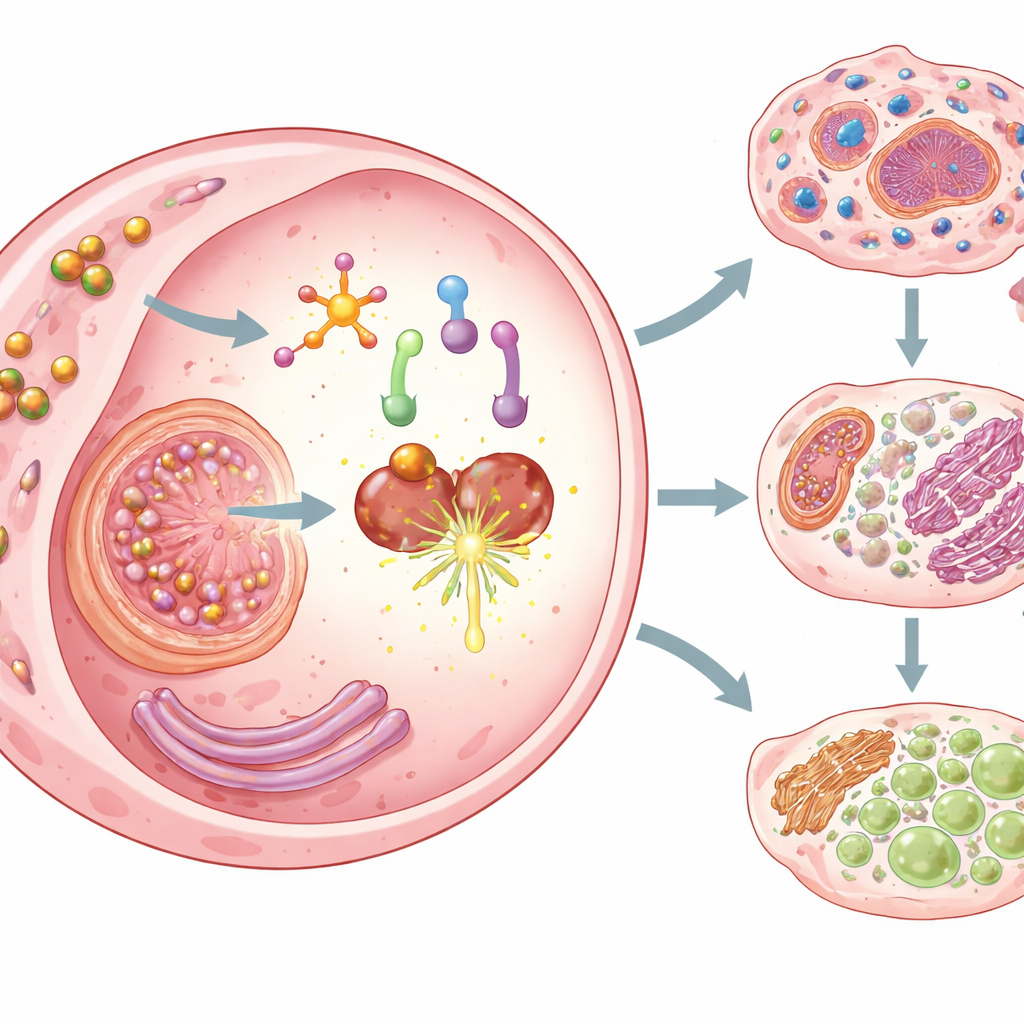
Desencadenando tres formas de muerte celular cancerosa
Una vez activado, Cu–DHN hace más que envenenar las células cancerosas. Desencadena tres formas reguladas de muerte celular que son especialmente visibles para el sistema inmunitario. Primero, la juglona revierte el silenciamiento epigenético de una proteína formadora de poros llamada gasdermina D y activa un complejo sensor inflamatorio, de modo que las células experimentan piroptosis—una forma de muerte dramática y explosiva que rompe la membrana y derrama el contenido interno. Segundo, el cobre transportado por las nanopartículas, captado eficientemente por las células cancerosas, induce cuproptosis, una forma de muerte ligada a la acumulación tóxica de cobre en maquinaria metabólica clave. Tercero, al agotar el glutatión y desactivar una enzima protectora (GPX4), Cu–DHN favorece la ferroptosis, una muerte impulsada por la peroxidación lipídica. En conjunto, estos modos aseguran que las células cancerosas no solo sean eliminadas de forma eficiente, sino que mueran de una manera particularmente inmunogénica.
Del ataque local a la defensa de todo el organismo
La piroptosis y el daño oxidativo concomitante hacen que las células tumorales liberen una avalancha de señales de alarma: antígenos asociados al tumor, moléculas de peligro como ATP y HMGB1, y marcadores de estrés en su superficie. En modelos de ratón de cáncer de mama agresivo, una única inyección de Cu–DHN en tumores primarios condujo a una fuerte activación de células dendríticas en los ganglios linfáticos cercanos y a una oleada de células T CD8 encargadas de atacar el tumor. Estas células inmunitarias viajaron luego a tumores no tratados en el lado opuesto del cuerpo y a los pulmones, donde frenaron o casi impidieron el crecimiento de nuevos tumores y nódulos metastásicos. El bloqueo de las células T CD8 eliminó en gran medida esta protección, confirmando que Cu–DHN convierte el tumor primario en una vacuna in situ que enseña al sistema inmune a reconocer y destruir el cáncer en otros lugares.
Efectos potentes con un perfil más seguro
Una preocupación importante con las terapias basadas en piroptosis es el riesgo de dañar tejidos sanos, que también poseen las mismas proteínas formadoras de poros. Cuando la juglona se administra directamente en su forma activa, los ratones sufren toxicidad significativa en hígado, riñones y sangre. En contraste, Cu–DHN permanece inerte en tejidos sanos, porque estos carecen de la combinación de desencadenantes químicos necesarios para activar la partícula. En ratones, Cu–DHN igualó el poder citotóxico y antimetastásico de la juglona activa mientras evitaba daño orgánico, anomalías sanguíneas y pérdida de peso. En términos sencillos, este trabajo muestra cómo una nanopartícula conductiva y racional puede mantenerse silenciosa en el cuerpo, despertarse solo dentro de los tumores, forzar a las células cancerosas a morir de forma inmunoestimulante y así actuar como una plataforma precisa y autosuficiente de vacuna contra el cáncer.
Cita: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
Palabras clave: inmunoterapia contra el cáncer, nanomedicina, piroptosis, vacunas contra el cáncer, microambiente tumoral