Clear Sky Science · es
La eliminación de DUSP6 restaura la eficacia de las células CAR T afectada por la pérdida tumoral de CD58 mediante la reactivación de la señalización AP-1
Por qué importa potenciar las células que combaten el cáncer
Las células inmunitarias diseñadas, llamadas células CAR T, han transformado el tratamiento de ciertos cánceres hematológicos, pero muchos pacientes aún recaen porque sus tumores aprenden a evadir el ataque. Este estudio descubre una debilidad oculta en algunos tumores que desactiva silenciosamente a las células CAR T desde su interior, y muestra cómo un ajuste genético preciso puede restaurar la resistencia, el suministro de energía y la capacidad de matar de estas células. Para el lector, es una mirada a cómo las terapias celulares de próxima generación podrían volverse más duraderas y eficaces para más personas.
Un mango que falta en las células tumorales
Las células CAR T necesitan un agarre firme con su diana para funcionar bien. Muchas células tumorales exhiben una molécula de superficie llamada CD58 que sirve como un “mango” para las células inmunitarias, ayudándolas a adherirse y formar una zona de contacto estrecho. Trabajos anteriores mostraron que cuando los cánceres pierden CD58, las células CAR T tienen dificultades para formar este contacto y se vuelven menos efectivas. En este estudio, los investigadores plantearon una pregunta más profunda: más allá de este problema mecánico del apretón de manos, ¿cómo reconfigura la pérdida de CD58 la biología interna de las células CAR T para atenuar su rendimiento con el tiempo?
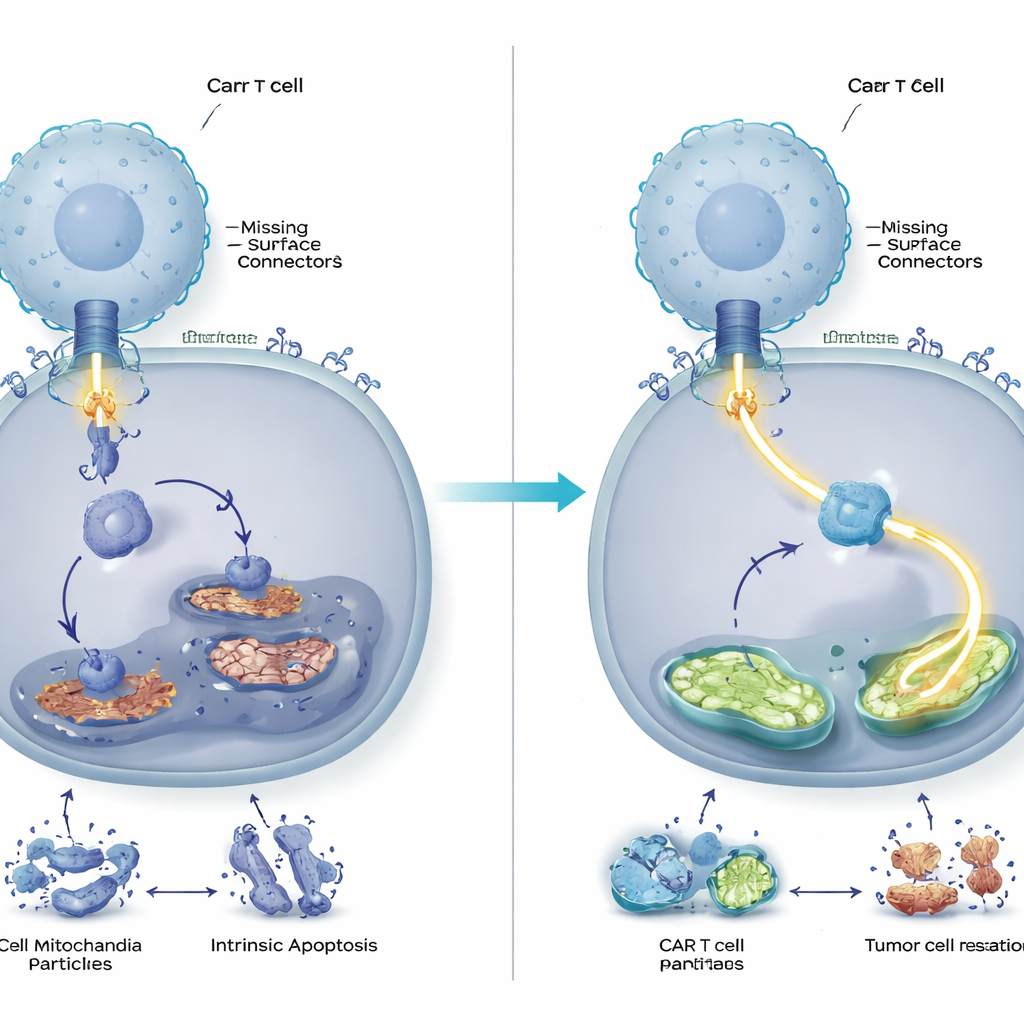
Un cableado interno cortocircuitado en las CAR T
Al comparar células CAR T expuestas a tumores normales con las que se enfrentaban a tumores deficientes en CD58, el equipo encontró que un centro de control clave dentro de las células T —denominado AP‑1— se debilitaba selectivamente, mientras que otras vías de señalización principales permanecían en gran medida intactas. AP‑1 es un conjunto de proteínas que activan genes implicados en la activación y la supervivencia. Cuando la actividad de AP‑1 decaía, las células CAR T mostraban señales inequívocas de una crisis energética interna: menos mitocondrias y de menor tamaño (sus centrales energéticas), disminución de la capacidad para consumir oxígeno y metabolizar la glucosa, y pérdida del potencial eléctrico a través de las membranas mitocondriales. Al mismo tiempo, se acumulaban especies reactivas de oxígeno dañinas. En conjunto, estos cambios empujaron a las células CAR T hacia un programa de autodestrucción basado en el daño mitocondrial, incluso sin señales externas de muerte.
Apagar un freno interno
Para entender por qué AP‑1 estaba tan suprimido, los investigadores buscaron corriente arriba “frenos” moleculares que pudieran estar sobreactivos. Encontraron que las células CAR T frente a tumores negativos para CD58 incrementaban varias fosfatasas —enzimas que apagan vías de señalización—, en particular una llamada DUSP6. Usando fármacos y luego edición genética precisa para bloquear estas enzimas, descubrieron que eliminar DUSP6 reavivaba con mayor fuerza la actividad de AP‑1. Las células CAR T editadas para carecer de DUSP6 se expandieron mejor, formaron más mitocondrias, quemaron combustible de forma más eficiente, produjeron más moléculas citotóxicas y fueron menos propensas a la apoptosis, especialmente cuando eran desafiadas de forma repetida por células tumorales deficientes en CD58.
Control tumoral más fuerte y duradero en animales
El equipo probó luego si este ajuste molecular importaba en sistemas vivos. En ratones portadores de células de cáncer hematológico humano que tenían o carecían de CD58, las células CAR T deficientes en DUSP6 eliminaron los tumores con mayor eficacia y los mantuvieron a raya por más tiempo que las células CAR T convencionales. Las células modificadas se multiplicaron con más robustez, mostraron menos marcadores de agotamiento y secretaron niveles más altos de mensajeros inmunitarios clave. Cabe destacar que los beneficios de eliminar DUSP6 se observaron no solo cuando los tumores carecían de CD58, sino también cuando lo conservaban, lo que sugiere que esta modificación podría potenciar en términos generales las terapias CAR T más que servir como una solución limitada para un subtipo tumoral poco frecuente.
Pistas a partir de datos de pacientes
Para explorar la relevancia en humanos, los investigadores examinaron datos de expresión génica de personas tratadas con células CAR T o con fármacos inhibidores de puntos de control inmunitario. En pacientes con linfoma difuso de células B grandes que recibieron una terapia CAR T de doble diana, niveles más bajos de DUSP6 en las células CD8 antes o poco después de la infusión se asociaron con tasas de respuesta completa más altas. En una cohorte separada de cáncer de piel tratada con anticuerpos anti‑PD‑1, las células CD8 agotadas de los no respondedores tendieron a expresar más DUSP6 que las de los respondedores. En conjunto, estas observaciones sugieren que DUSP6 actúa como un marcador negativo de la aptitud de los linfocitos T a través de distintas inmunoterapias y que reducirlo podría mejorar los resultados.
Qué significa esto para las terapias contra el cáncer futuras
Para un lector no especializado, el mensaje es que algunos tumores escapan al ataque de las células CAR T no solo ocultándose del reconocimiento, sino saboteando los motores internos de las células. La pérdida del “mango” CD58 en las células tumorales reduce silenciosamente la señalización AP‑1 en las células CAR T, agotando sus mitocondrias, elevando subproductos tóxicos y empujándolas hacia la muerte prematura. Al eliminar el freno DUSP6, los científicos pueden restaurar esta señalización perdida, reparar la salud mitocondrial y dotar a las células CAR T de mayor resistencia y capacidad citotóxica, incluso frente a tumores resistentes. Aunque se necesitan más pruebas de seguridad y ensayos clínicos, la ablación de DUSP6 surge como una estrategia de ingeniería prometedora para convertir a estos fármacos vivos contra el cáncer en herramientas más potentes, duraderas y potencialmente eficaces para un abanico más amplio de pacientes.
Cita: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Palabras clave: Células CAR T, CD58, DUSP6, inmunoterapia del cáncer, metabolismo de los linfocitos T