Clear Sky Science · es
Desatando el potencial de la vía STING mediada por nanobombas bimetálicas para potenciar enganchadores T bispecíficos en la fotoinmunoterapia del cáncer colorrectal
Volver el sistema inmunitario contra el cáncer de colon
Los cánceres de colon y recto son comunes y con frecuencia mortales, en parte porque los tumores aprenden a esconderse del sistema inmunitario. Este estudio explora una nueva estrategia que reúne varias herramientas antitumorales en una diminuta "nanobomba" para despertar las defensas del organismo, ayudar a las células inmunitarias a localizar el tumor y evitar que el cáncer reaparezca o se disemine.
Por qué los fármacos inmunitarios actuales necesitan una mejora
Una clase prometedora de fármacos contra el cáncer, llamados enganchadores T bispecíficos, actúa como casamenteros biológicos: un extremo captura una célula T (un componente clave del sistema inmunitario) y el otro se une a un marcador en la célula tumoral, obligándolas a acercarse para que la célula T pueda matar. Aunque son potentes en cánceres sanguíneos, estos fármacos tienen dificultades en tumores sólidos como el colorrectal. Se eliminan rápidamente del organismo, pueden atacar tejidos sanos que comparten el mismo marcador y a menudo se enfrentan a tumores "fríos" que carecen de suficientes células inmunitarias para que el tratamiento funcione. Por ello, médicos e investigadores buscan formas de administrar estos fármacos con más seguridad y convertir tumores fríos en "calientes", repletos de células inmunitarias activadas.
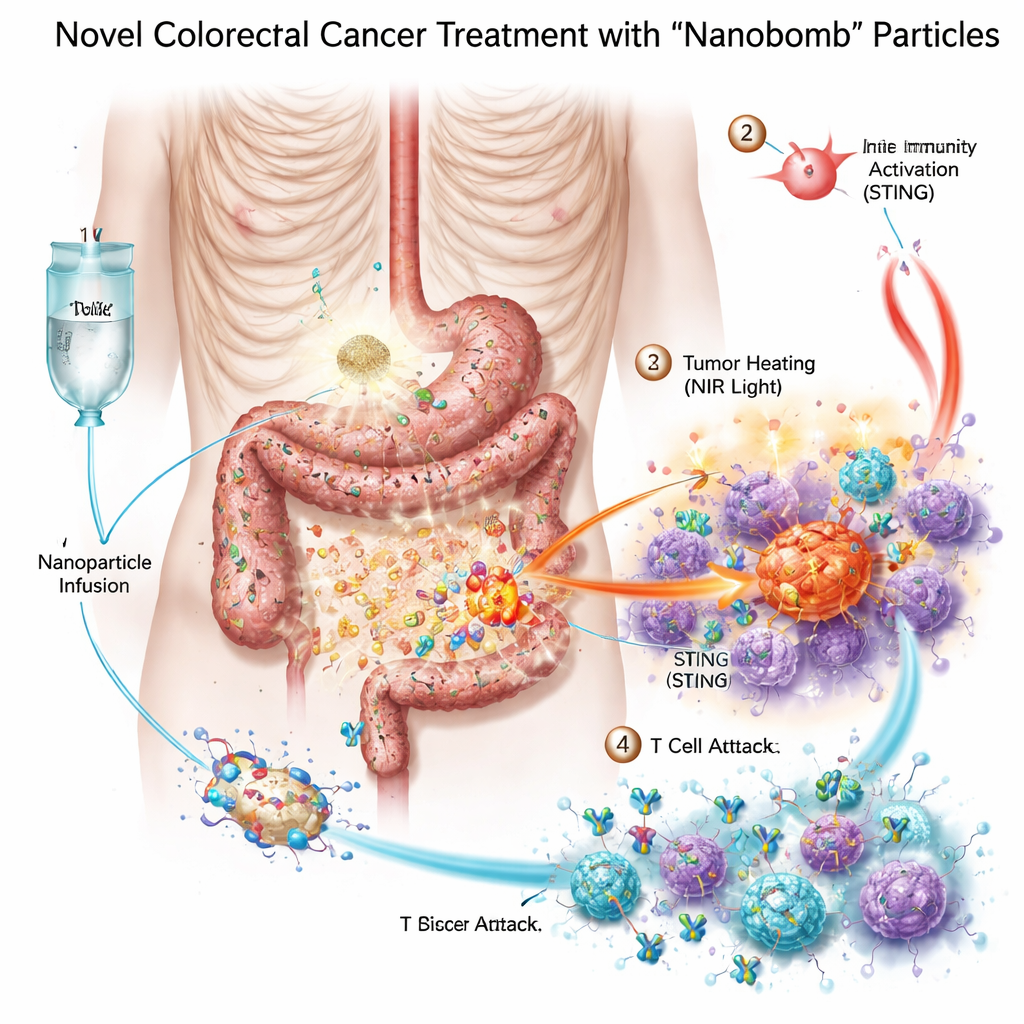
Empaquetando tres armas en una diminuta "nanobomba"
Los investigadores diseñaron una nanobomba bimetálica—denominada científicamente MnO2/Co‑DA@BiTE/HPT—que combina tres modos de tratamiento en una sola partícula. Primero, el núcleo contiene manganeso y cobalto, metales que pueden activar un sistema de alarma celular llamado vía STING, que ayuda al organismo a detectar el peligro y reclutar células inmunitarias. Segundo, la superficie de la partícula está recubierta con un enganchador T bispecífico que conecta las células T con las células cancerosas. Tercero, el material absorbe luz en el infrarrojo cercano, lo que permite calentar el tumor desde fuera mediante fototerapia térmica. Para asegurar que las nanobombas se dirijan a las células del cáncer colorrectal, el equipo añadió un fragmento corto de ADN, un aptámero, que reconoce PD‑L1, una molécula a menudo abundante en estos tumores. Una vez que estas partículas alcanzan el tumor, enzimas naturales en el tejido tumoral ayudan a descomponerlas y liberar su carga exactamente donde se necesita.
Calentar, alertar y reclutar al ejército inmunitario
En placas de laboratorio, las nanobombas mataron las células de cáncer colorrectal con mayor eficacia que cualquiera de sus componentes por separado. Cuando se iluminaron con luz en el infrarrojo cercano, las partículas se calentaron, estresaron y dañaron las células cancerosas, y contribuyeron a generar especies reactivas de oxígeno—moléculas altamente reactivas que lesionan aún más a las células tumorales. Este estrés rompió el ADN de las células y las indujo a una forma de muerte especialmente visible que emite señales de "peligro". Las células inmunitarias cercanas, especialmente las células dendríticas, engulleron el material tumoral en descomposición y activaron la vía STING con la ayuda del manganeso y el cobalto liberados. A continuación produjeron interferones y otros mensajeros inflamatorios que maduran y atraen a las células T. Al mismo tiempo, el enganchador bispecífico presente en la nanobomba unió físicamente las células T a las células tumorales PD‑L1 positivas, mejorando la activación y la capacidad citotóxica de las células T incluso en tumores previamente fríos.
Desde la reducción tumoral hasta la memoria inmunitaria duradera
En varios modelos de ratón—incluidos tumores colorrectales subcutáneos, tumores en ambos lados del cuerpo, metástasis pulmonares y un modelo de recidiva postoperatoria—las nanobombas más luz ralentizaron considerablemente o casi detuvieron el crecimiento tumoral. Los tumores tratados contenían muchas más células T CD8 con capacidad citotóxica y menos células T regulatorias que normalmente suprimen las respuestas inmunitarias. Las células dendríticas dentro de los tumores y en los ganglios linfáticos mostraron signos de maduración, y los análisis sanguíneos revelaron niveles elevados de citocinas estimulantes del sistema inmunitario. De manera importante, los ratones que eliminaron sus tumores tras el tratamiento con nanobombas estuvieron mejor protegidos cuando se reintrodujo el cáncer y desarrollaron menos metástasis pulmonares, lo que demuestra que la terapia ayudó a generar memoria inmunitaria a largo plazo en lugar de solo provocar una reducción tumoral puntual.
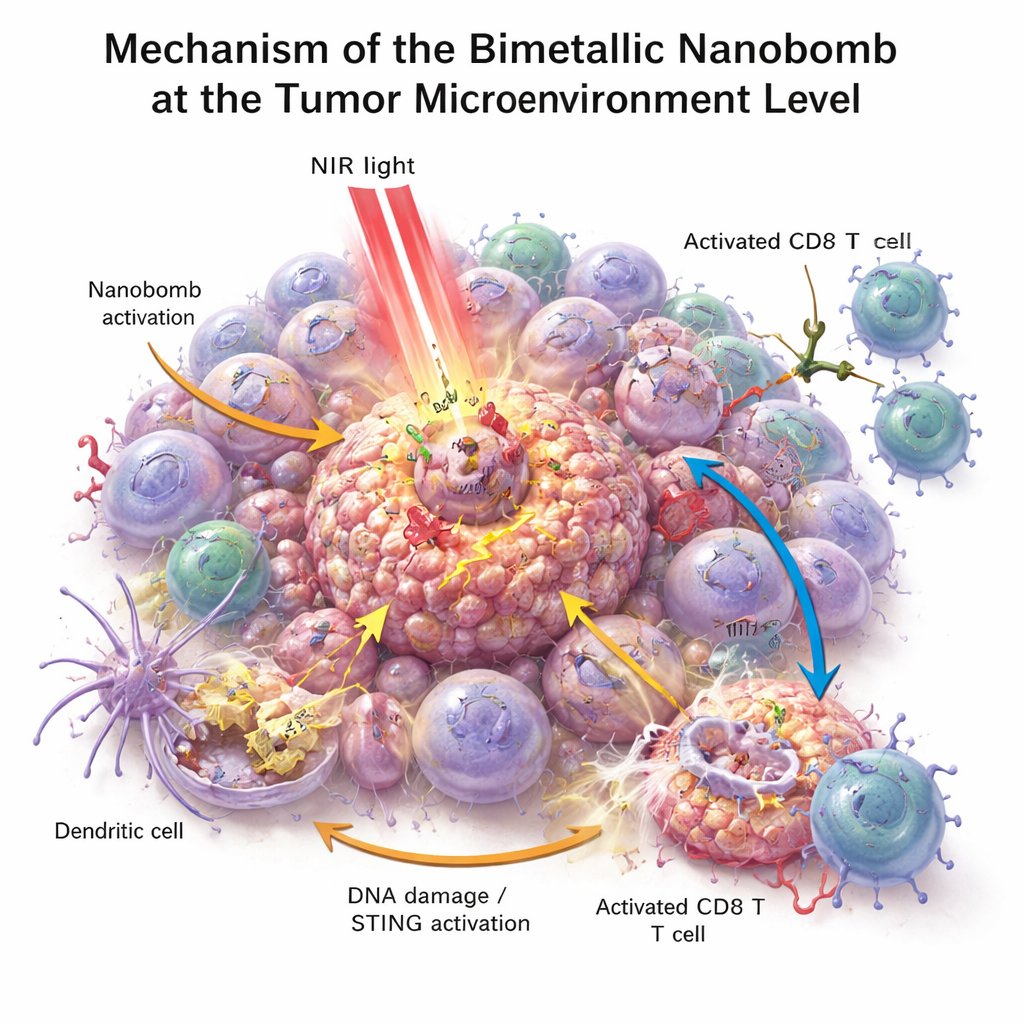
Qué podría significar esto para la atención del cáncer en el futuro
Este trabajo presenta una nanomedicina de "triple impacto" que calienta los tumores, activa una alarma interna de peligro y dirige las células T directamente hacia las células cancerosas, todo dentro de una única partícula dirigida. En ratones, este enfoque no solo transformó tumores colorrectales fríos en tumores calientes e inflamados, sino que también contribuyó a prevenir la recurrencia y la diseminación. Aunque la tecnología aún está lejos del uso clínico—la producción a escala, la seguridad a largo plazo y las pruebas en humanos siguen siendo desafíos importantes—ofrece un modelo para futuros tratamientos que combinen materiales inteligentes con fármacos inmunitarios para proporcionar a los pacientes una respuesta anticancerígena más fuerte y duradera.
Cita: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Palabras clave: cáncer colorrectal, inmunoterapia, nanopartículas, vía STING, enganchador T bispecífico