Clear Sky Science · es
Terapia guiada personalizada por farmacocinética–farmacodinámica mediante una plataforma multi-organoide derivada de células madre pluripotentes inducidas en cáncer de mama con mutación NF1
Por qué esta investigación importa para los pacientes
Muchas personas con cáncer reciben fármacos que funcionan bien en algunos pacientes pero no en otros, y con frecuencia provocan efectos secundarios severos. Este estudio describe una nueva forma de probar tratamientos contra el cáncer fuera del cuerpo usando mini-órganos cultivados en el laboratorio a partir de las propias células del paciente. El trabajo se centra en una forma difícil de tratar del cáncer de mama impulsada por alteraciones en un gen llamado NF1 y muestra cómo combinar una estrategia de corrección genética con un fármaco dirigido podría conducir a una terapia más segura, más eficaz y realmente personalizada.
Construyendo una versión en miniatura del cuerpo del paciente
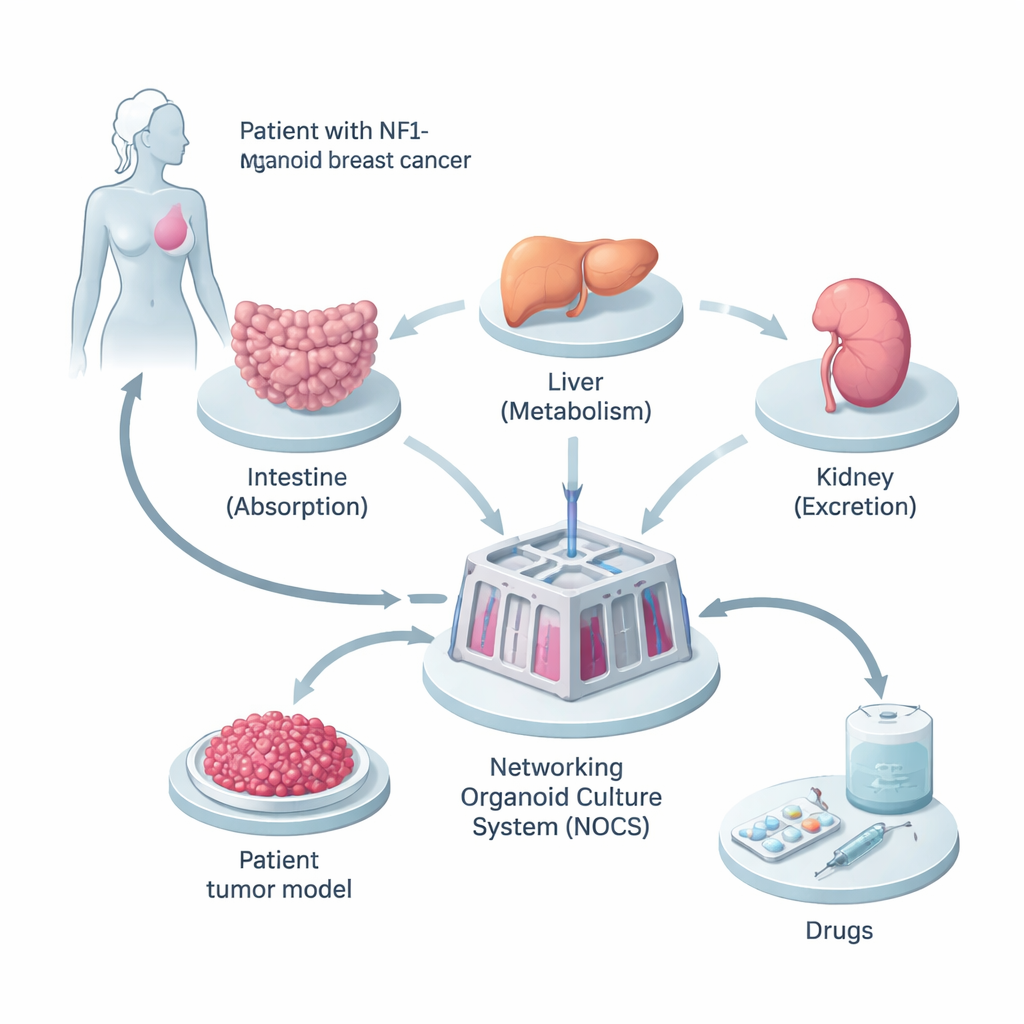
Los investigadores comenzaron con tejido de una mujer cuyo cáncer de mama presentaba una mutación heredada en el gen NF1. Reprogramaron sus células normales con apariencia de piel en células madre pluripotentes inducidas, que pueden convertirse en casi cualquier tipo celular del cuerpo. A partir de estas, crecieron tres tipos de mini-órganos—intestino delgado, hígado y riñón—porque son los sitios clave donde los medicamentos se absorben, metabolizan y eliminan. En paralelo, crearon “esferoides” tumorales 3D a partir de sus células cancerosas, preservando la mezcla de tipos celulares y los cambios genéticos encontrados en el tumor original.
Un circuito vivo para probar fármacos
Para hacer que estos mini-órganos se comportaran más como un cuerpo real, el equipo los conectó en un dispositivo lleno de fluido denominado Sistema de Cultivo de Organoides en Red, o NOCS. En este montaje, el medio líquido fluye entre los compartimentos de intestino, hígado, riñón y tumor, imitando la circulación sanguínea. Los fármacos pueden añadirse de forma que se asemeje a tragar una píldora o a recibir una inyección, y sensores y bombas controlan la velocidad del “fluido sanguíneo” y la frecuencia de renovación. Esto permitió a los científicos seguir cuánto fármaco se absorbe, con qué rapidez se degrada y con qué intensidad actúa sobre el tumor—todo en un modelo humano específico del paciente.
Reparar un gen dañado con salto de exón
El tumor de la paciente llevaba una mutación dañina en NF1 que mantiene activas las vías de crecimiento y hace que muchos fármacos estándar sean ineficaces. El equipo diseñó fragmentos cortos de material genético, llamados oligonucleótidos antisentido, para hacer que la maquinaria de procesamiento del ARN de la célula omita la porción defectuosa (exón 2) del gen NF1. Usando un sistema de entrega viral que funciona durante días, indujeron un “salto de exón” estable en las células cancerosas de la paciente. Esto produjo una proteína NF1 más corta pero funcional, redujo las señales de crecimiento sobreactivadas y aumentó la sensibilidad de las células tumorales al tratamiento.
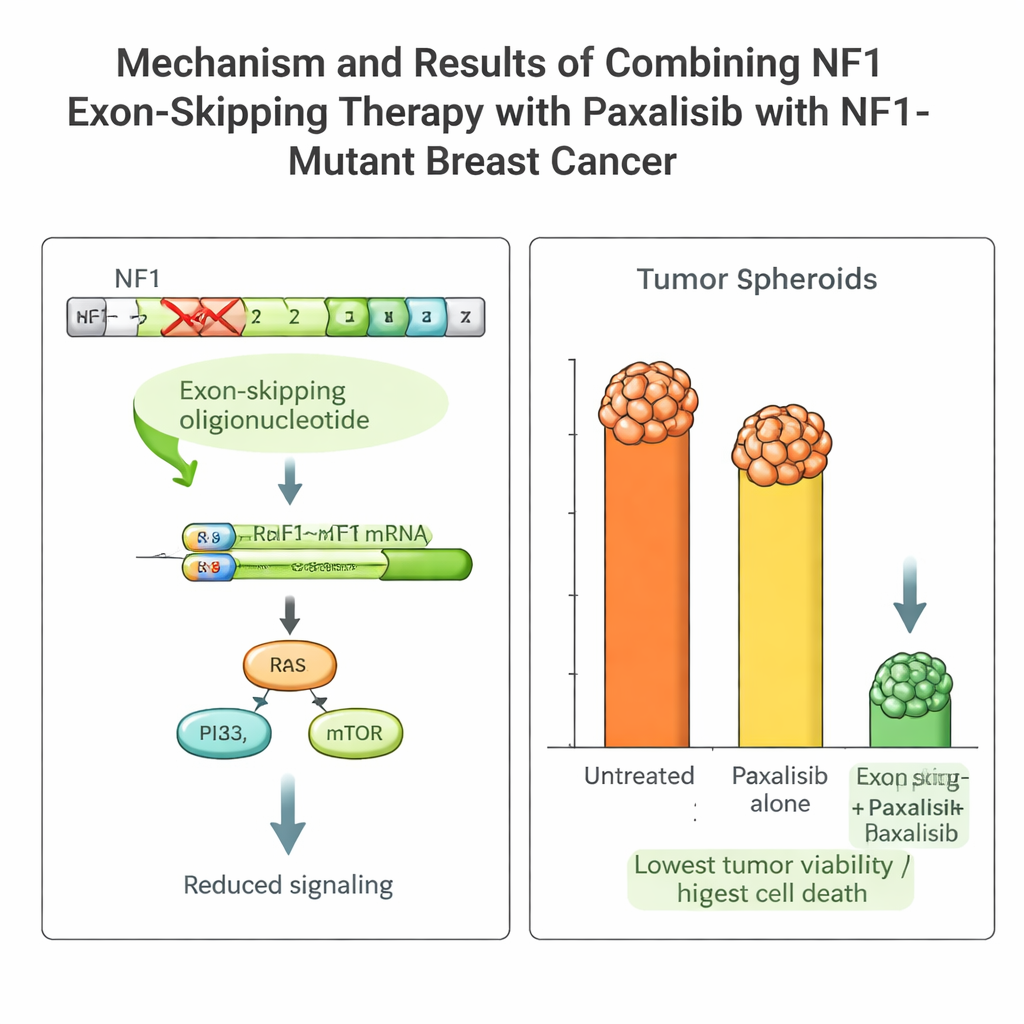
Elegir el fármaco dirigido adecuado con orientación PK/PD
Con esta plataforma, el equipo comparó varios fármacos avanzados que bloquean la vía PI3K–mTOR, que está aguas abajo de NF1. Midiendo farmacocinética (cómo el cuerpo maneja el fármaco) y farmacodinámica (cómo actúa el fármaco sobre el tumor) tanto en ratones como en el NOCS, identificaron un fármaco, Paxalisib, que destacó: se absorbía bien en el intestino, persistía en el sistema a niveles útiles y mostró un comportamiento similar en animales y en el dispositivo de organoides. Combinado con el salto de exón en NF1, el poder citotóxico de Paxalisib contra las células tumorales de la paciente aumentó drásticamente, con fuertes reducciones en el crecimiento y claros signos de muerte celular programada, tanto en el NOCS como en ratones portadores del tumor de la paciente.
Equilibrar beneficio y riesgo entre órganos
Puesto que los modelos de intestino, hígado y riñón formaban parte del mismo circuito, los investigadores también pudieron observar signos tempranos de daño orgánico. Paxalisib provocó respuestas de estrés y un debilitamiento sutil de las barreras en los modelos de intestino y riñón, y señales de tensión en el hígado, pero sin una pérdida mayor de viabilidad celular a la dosis probada. Esta visión de cuerpo entero, usando tejido humano, ofrece una manera de comparar opciones de tratamiento no solo por su capacidad para reducir tumores, sino también por cómo podrían afectar a órganos sanos antes de que un fármaco llegue jamás a un paciente.
Qué podría significar esto para la atención del cáncer en el futuro
En términos sencillos, este estudio demuestra que ya es posible cultivar un “mini cuerpo en un chip” simplificado y específico del paciente que pueda probar cómo se comportarán e interactuarán distintos fármacos—e incluso enfoques de corrección genética. Para esta paciente con cáncer de mama con mutación NF1, la estrategia óptima fue la combinación de la terapia de salto de exón en NF1 y el fármaco oral Paxalisib, que juntos frenaron el crecimiento tumoral mucho más que cualquiera de los dos por separado. Si se desarrolla más y se prueba en más pacientes, este tipo de plataformas podría orientar a los médicos hacia planes de tratamiento adaptados a los genes y la biología de cada persona, mejorando las probabilidades de éxito y reduciendo la toxicidad innecesaria.
Cita: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Palabras clave: oncología personalizada, cáncer de mama, organoides, mutación NF1, terapia dirigida