Clear Sky Science · es
Aprovechamiento de vías inmunometabólicas impulsadas por lípidos en metástasis omentales para mejorar la inmunoterapia en pacientes con cáncer de ovario
Por qué importa la grasa abdominal en el cáncer de ovario
El cáncer de ovario con frecuencia se disemina a un delantal graso del abdomen denominado omento. Esta región está llena de adipocitos y células inmunitarias, y resulta ser mucho más que un mero espectador pasivo. El estudio resumido aquí muestra que la forma en que las células inmunes usan y gestionan los lípidos en estos depósitos omentales puede ayudar a explicar por qué solo una fracción pequeña de pacientes se beneficia de las inmunoterapias modernas. También sugiere nuevas combinaciones de fármacos y pruebas basadas en imagen que podrían hacer que esos tratamientos funcionen para más personas.
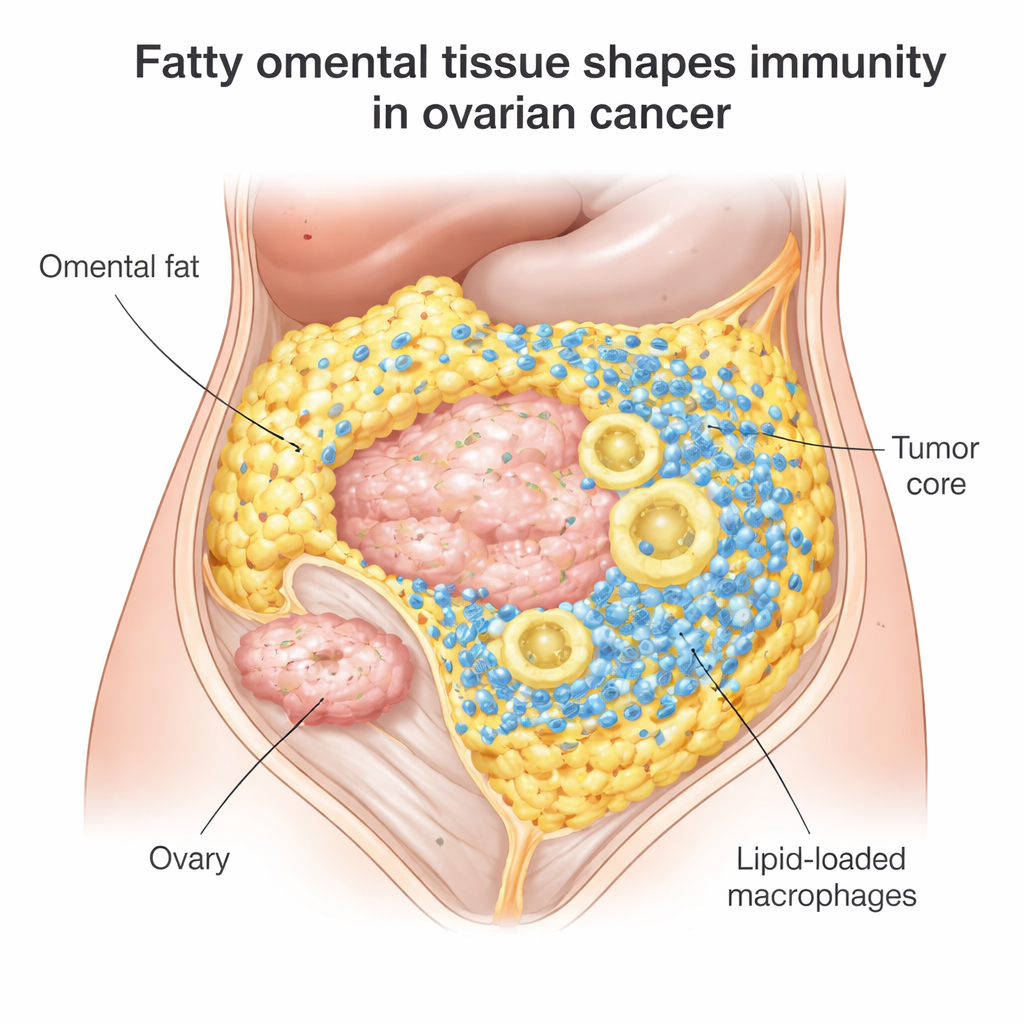
Un campo de batalla oculto en la grasa abdominal
La mayoría de las mujeres con cáncer de ovario epitelial responden inicialmente a la cirugía y la quimioterapia, pero el 70–80% ve volver la enfermedad, y los fármacos inhibidores de puntos de control inmunitario como nivolumab o pembrolizumab solo ayudan a alrededor del 10–15%. Los investigadores se centraron en las metástasis omentales, un sitio frecuente donde el cáncer de ovario se instala entre células grasas. Al examinar más de 100 muestras tumorales, hallaron que los tumores omentales estaban repletos de células inmunitarias: linfocitos T citotóxicos capaces de atacar el cáncer y grandes células fagocíticas llamadas macrófagos. Pero había un problema. Estos linfocitos T tendían a agruparse en el borde donde el tumor encuentra la grasa, en lugar de penetrar en el núcleo tumoral donde más se les necesita.
Grasa que alimenta a algunas células inmunes pero abruma a otras
Al ahondar más, el equipo demostró que los linfocitos T en estos tumores grasos se adaptan al entorno local incorporando lípidos procedentes de las células adiposas cercanas. Eso parece mantenerlos «en forma» metabólicamente: su actividad génica y pruebas de laboratorio mostraron que eran capaces de reconocer y matar las propias células tumorales de la paciente. Al mismo tiempo, muchos macrófagos asociados al tumor en el omento estaban cargados de gotículas lipídicas. Estos macrófagos repletos de lípidos mostraron signos de alto estrés oxidativo —desgaste químico vinculado a especies reactivas de oxígeno— y se desplazaron hacia un estado inmunosupresor que apoya al tumor. En otras palabras, el mismo entorno rico en grasa que puede nutrir linfocitos T eficaces también empuja a los macrófagos a un modo dañino que atenúa el ataque inmunitario global.
Reprogramar macrófagos sobrealimentados con fármacos existentes
Los científicos se preguntaron si podrían convertir de nuevo a esos macrófagos estresados en aliados. Usando fragmentos tumorales frescos cultivados en el laboratorio, probaron dos enfoques. Uno implicó maraviroc, un fármaco contra el VIH que bloquea CCR5, un receptor para la señal inmunitaria CCL5, abundante en el borde tumor–grasa. El otro bloqueó CD36, un receptor «reciclador» clave que permite a los macrófagos importar ácidos grasos. Ambos tratamientos redujeron la carga lipídica dentro de los macrófagos, disminuyeron marcadores de estrés oxidativo y peroxidación lipídica dañina, y desataron oleadas de señales inflamatorias. De forma crucial, permitieron que los linfocitos T citotóxicos se multiplicaran y se desplazaran desde el borde graso hacia el núcleo tumoral, aumentando la actividad inmune local sin añadir células inmunitarias externas.
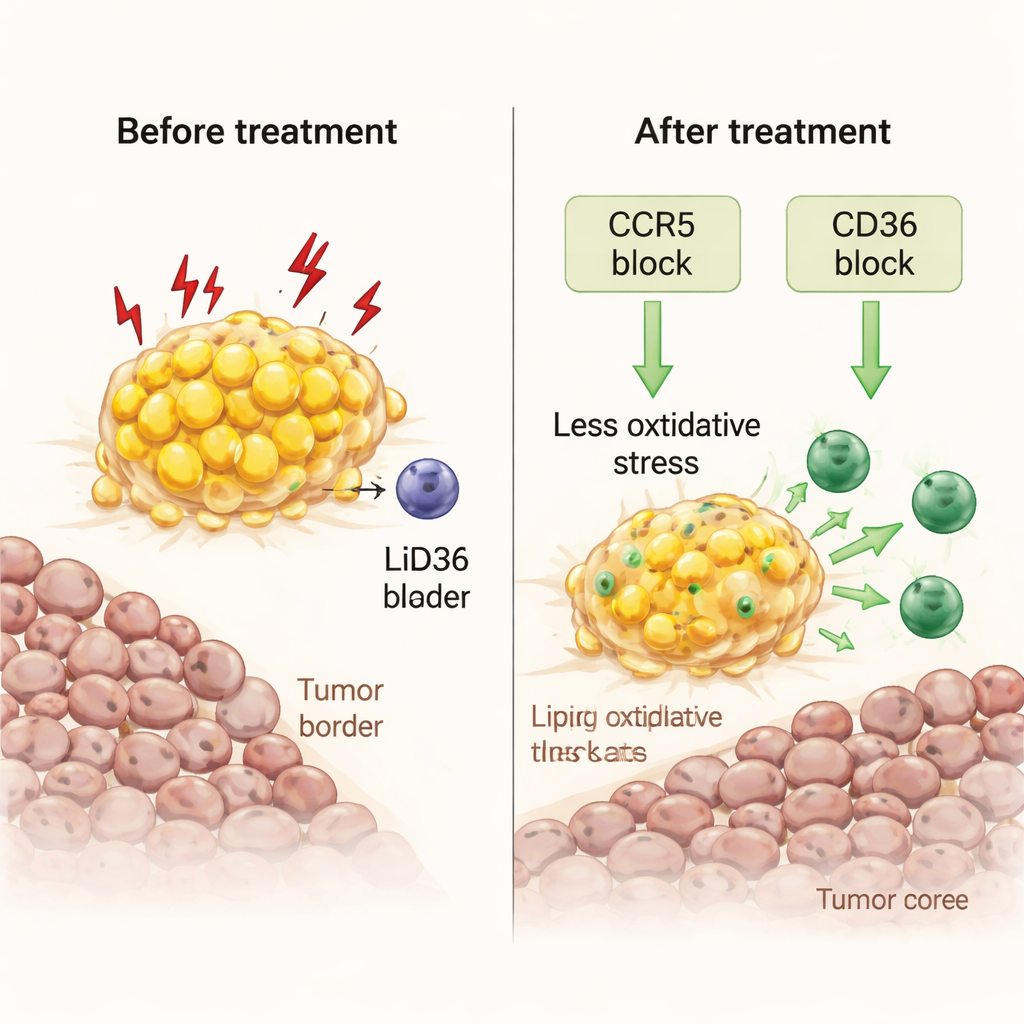
De las vías celulares a modelos y pacientes reales
Para probar estas ideas en un contexto más realista, el equipo empleó ratones humanizados diseñados para portar un sistema inmunitario similar al humano e implantó tumores humanos en tejido rico en grasa. El tratamiento con maraviroc reprogramó los macrófagos humanos en estos animales de formas que reflejaron las muestras derivadas de pacientes: reducción de firmas lipídicas y de estrés, mayor producción de citoquinas y mayor apoyo a las vías relacionadas con los linfocitos T. En el plano clínico, los investigadores reexaminaron un ensayo japonés de nivolumab en cáncer de ovario resistente a la quimioterapia. Todos los pacientes que se beneficiaron del fármaco tenían metástasis omentales visibles en muestras quirúrgicas. Utilizando TAC o resonancia magnética combinadas con análisis por aprendizaje automático de la distribución de la grasa corporal, construyeron un árbol de decisión que podría señalar no invasivamente a los pacientes cuyos tumores probablemente se sitúan cerca de la grasa visceral —y en un caso prospectivo, este método predijo correctamente a una paciente que luego respondió a nivolumab.
Qué podría significar esto para tratamientos futuros
Para un público general, la idea clave es que «dónde» crece el cáncer de ovario en el cuerpo, y cómo la grasa cercana remodela las células inmunes, puede influir con fuerza en si la inmunoterapia funciona. Los depósitos omentales ricos en grasa parecen albergar linfocitos T vigorosos pero también macrófagos sobrealimentados y estresados que amortiguan el ataque. Al aligerar la carga lipídica en esos macrófagos y aliviar su estrés oxidativo —mediante bloqueadores de CCR5 como maraviroc, agentes dirigidos a CD36 u otras estrategias relacionadas— puede ser posible convertir una respuesta inmune parcialmente bloqueada en un asalto a escala completa contra el tumor. Al mismo tiempo, medidas por imagen de la implicación omental podrían ayudar a los médicos a elegir qué pacientes tienen más probabilidades de beneficiarse de inhibidores de puntos de control inmunitario, aportando un enfoque más personalizado y potencialmente más eficaz para tratar el cáncer de ovario.
Cita: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Palabras clave: cáncer de ovario, grasa omental, inmunoterapia, macrófagos asociados al tumor, metabolismo de lípidos