Clear Sky Science · es
La activación del receptor de tromboxano en células dendríticas mitiga la sepsis suprimiendo el reclutamiento de neutrófilos mediado por S100a8/a9
Por qué importa controlar las infecciones desbocadas
La sepsis es una reacción exagerada y potencialmente mortal del organismo frente a una infección, que a menudo se inicia en los pulmones o el intestino y puede conducir a fallo multiorgánico. Incluso con cuidados intensivos modernos, la sepsis mata a millones cada año porque los tratamientos habituales se centran principalmente en sostener los órganos fallidos en lugar de calmar con precisión un sistema inmunitario en avalancha. Este estudio revela un “freno” hasta ahora oculto dentro de un tipo clave de célula inmune —las células dendríticas— que puede reducir la inflamación dañina sin apagar la capacidad del cuerpo para combatir los gérmenes.
Guardianes inmunitarios bajo presión
Las células dendríticas actúan como centinelas del sistema inmune: detectan el peligro, alertan a otras células inmunitarias y ayudan a decidir cuán intensa debe ser la respuesta. En muestras de sangre de pacientes con sepsis, los autores observaron que las células dendríticas no solo eran menos numerosas, sino que también mostraban niveles marcadamente reducidos de un receptor llamado TP, que normalmente responde a una molécula lipídica denominada tromboxano A₂. Los pacientes cuyas células dendríticas presentaban los niveles más bajos de TP tendían a tener más neutrófilos circulantes —un glóbulo blanco de primera línea contra la infección— y una enfermedad más grave, lo que sugiere que cuando falla este freno de las células dendríticas, la inflamación puede salirse de control.
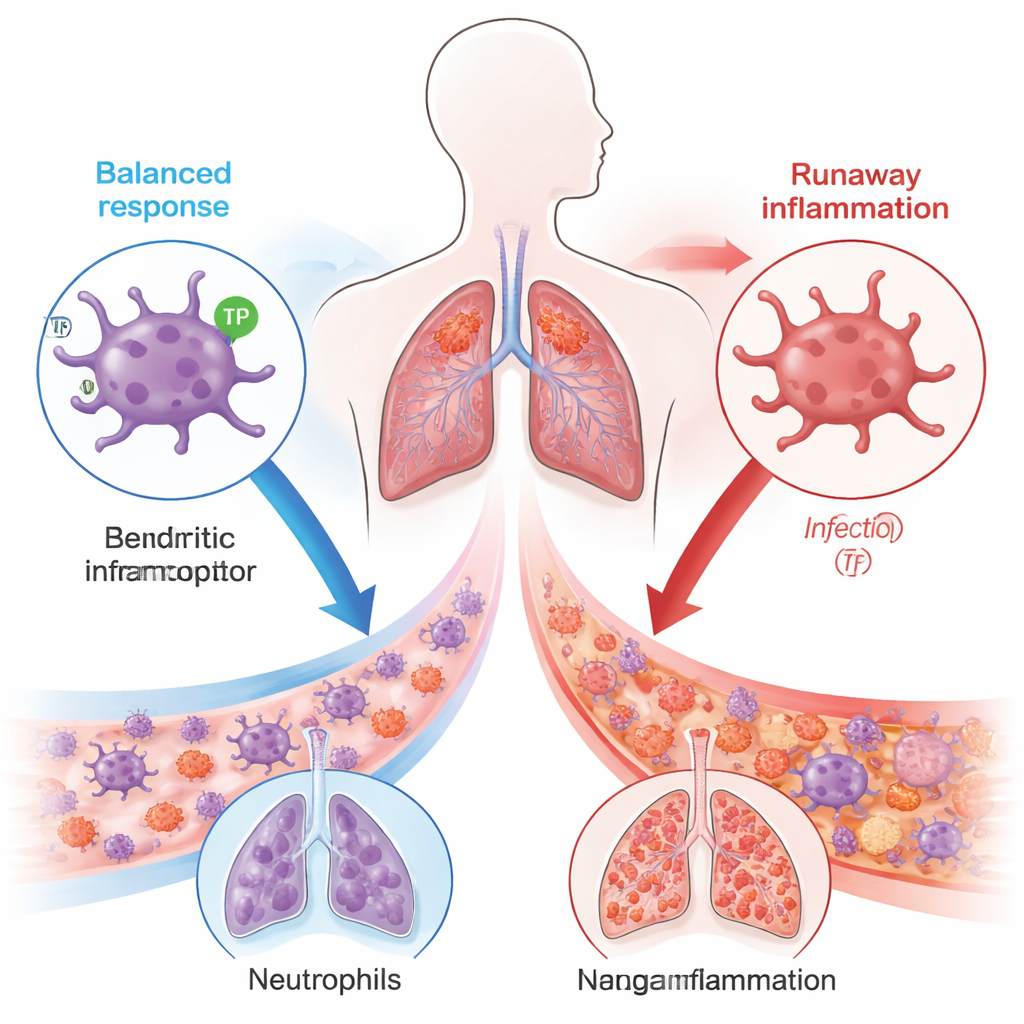
Cuando el freno falla, los neutrófilos inundan los pulmones
Para investigar causa y efecto, el equipo empleó modelos de sepsis en ratones provocados bien por perforación intestinal (un procedimiento que libera bacterias intestinales en la cavidad abdominal) o bien por administración de toxinas bacterianas. Los ratones diseñados para carecer de TP solo en sus células dendríticas evolucionaron mucho peor: murieron con más frecuencia, presentaron pulmones más permeables llenos de líquido y mostraron signos de invasión masiva de neutrófilos y daño tisular. Cuando células dendríticas extraídas de animales carentes de TP se transfirieron a ratones sanos, esos receptores también desarrollaron sepsis más grave, confirmando que una señalización defectuosa en las células dendríticas por sí sola puede inclinar la balanza hacia una inflamación letal.
Una señal de peligro que convoca demasiados defensores
Ahondando más, los investigadores examinaron qué genes cambiaban dentro de las células dendríticas cuando faltaba TP. Dos proteínas asociadas al peligro, S100A8 y S100A9, destacaron por su incremento marcado. Estas moléculas actúan como bengalas que atraen a los neutrófilos hacia tejidos inflamados. El equipo mostró que las células dendríticas de ratones sépticos atraían más neutrófilos en ensayos de laboratorio, y que bloquear S100A8/A9 con un fármaco reducía drásticamente esta atracción. Tanto en ratones como en pacientes, niveles más altos de S100A8/A9 iban de la mano con niveles más bajos de TP. En animales vivos, eliminar S100A9 específicamente en las células dendríticas —o bloquear su receptor principal, el sensor inmune TLR4— redujo el influjo de neutrófilos, disminuyó la formación de redes pegajosas de ADN y proteínas llamadas trampas extracelulares de neutrófilos (NETs) y protegió a los pulmones del daño.
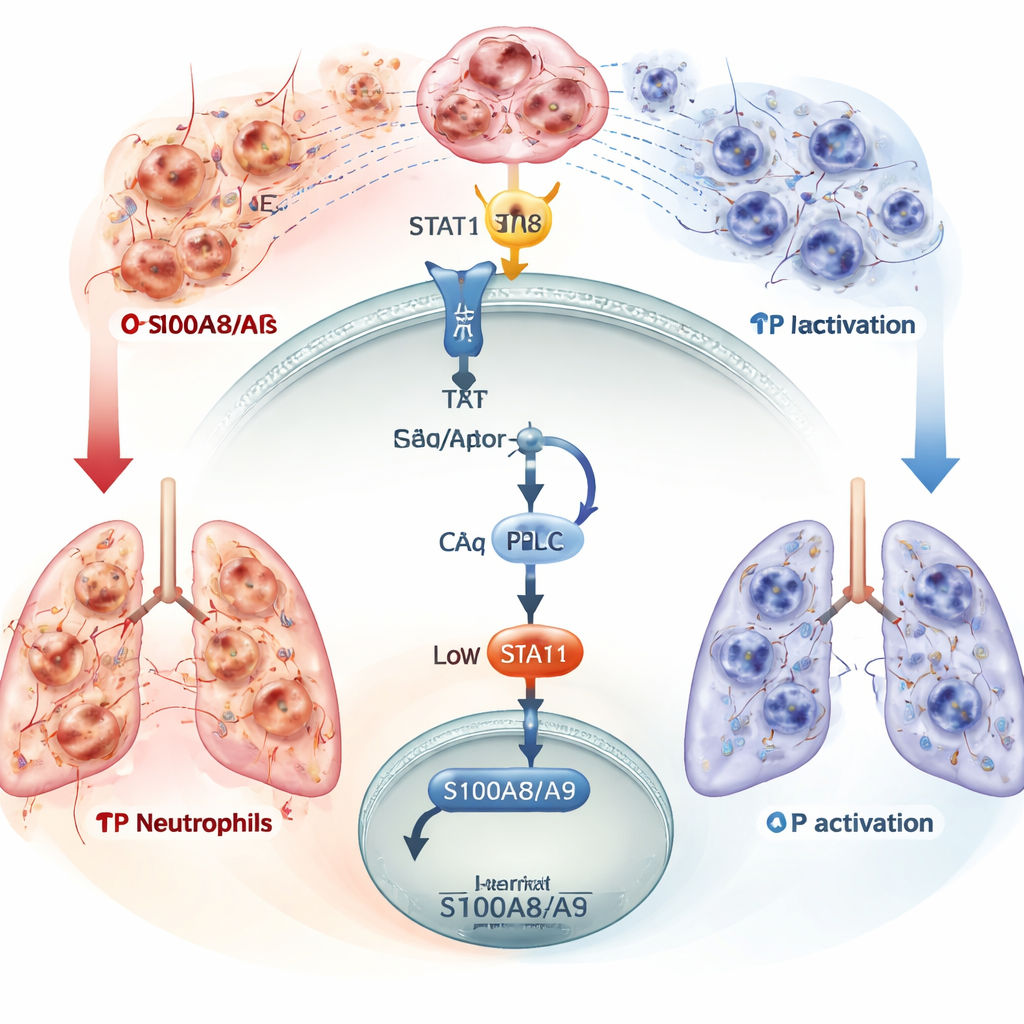
El circuito de señalización detrás de un freno selectivo
Los autores trazaron cómo TP controla la producción de S100A8/A9 dentro de las células dendríticas. La activación de TP desencadenó una cadena interna de eventos que implicaba una proteína quinasa (PKCδ) y un factor de transcripción llamado STAT1, que se desplaza al núcleo para influir en la actividad génica. Cuando esta vía estaba intacta, STAT1 ayudaba a mantener a raya los niveles de S100A8/A9, limitando el reclutamiento de neutrófilos. Bloquear PKCδ o STAT1 rompía este circuito protector, permitiendo que S100A8/A9 se disparara. Finalmente, el equipo construyó un fármaco de tamaño nanométrico que acopla un compuesto activador de TP a un péptido que se dirige específicamente a las células dendríticas. En ratones sépticos, este tratamiento dirigido restauró la señal de TP solo en las células dendríticas, redujo S100A8/A9, disminuyó la acumulación de neutrófilos y NETs en los pulmones y mejoró la supervivencia —todo ello sin suprimir de forma generalizada el sistema inmune.
Convertir un hallazgo en futuras terapias para la sepsis
Para un lector no especializado, el mensaje principal es que no toda inflamación es mala, pero un exceso en el lugar equivocado puede ser mortal. Este trabajo identifica un circuito preciso en las células dendríticas que normalmente evita que los neutrófilos desborden los pulmones durante una infección severa. Cuando se pierde la señalización por TP, las células dendríticas sobreproducen la alarma S100A8/A9, convocando oleadas de neutrófilos que dañan los tejidos en lugar de ayudar. Reactivar TP solo en las células dendríticas —o bloquear la vía S100A8/A9— podría permitir enfriar el lado perjudicial de la inflamación mientras se preserva gran parte de la capacidad del organismo para combatir la infección. Aunque aún en modelos animales, esta estrategia dirigida ofrece una dirección prometedora para tratamientos de sepsis más precisos en el futuro.
Cita: Du, R., Pan, T., Wang, Y. et al. Thromboxane receptor activation in dendritic cells mitigates sepsis by suppressing S100a8/a9-mediated neutrophil recruitment. Sig Transduct Target Ther 11, 75 (2026). https://doi.org/10.1038/s41392-026-02592-w
Palabras clave: sepsis, células dendríticas, neutrófilos, inflamación, regulación inmune