Clear Sky Science · es
GPR54 regula el desarrollo del cáncer de pulmón no microcítico a través de la dopa descarboxilasa
Por qué importa esta historia sobre el cáncer de pulmón
El cáncer de pulmón sigue siendo uno de los cánceres más mortales, y la mayoría de los casos corresponden a una forma llamada cáncer de pulmón no microcítico (CPNMC). Muchos pacientes acaban quedándose sin opciones de tratamiento efectivas porque los tumores se adaptan o desarrollan resistencia a los fármacos actuales. Este estudio descubre un sistema de control dentro de las células del cáncer de pulmón que hasta ahora no se había valorado lo suficiente, centrado en un receptor llamado GPR54 y una enzima llamada dopa descarboxilasa (DDC). Al entender cómo estas moléculas ayudan a los tumores a crecer y a abastecerse de energía, los investigadores señalan nuevas vías para frenar o incluso reducir el CPNMC.
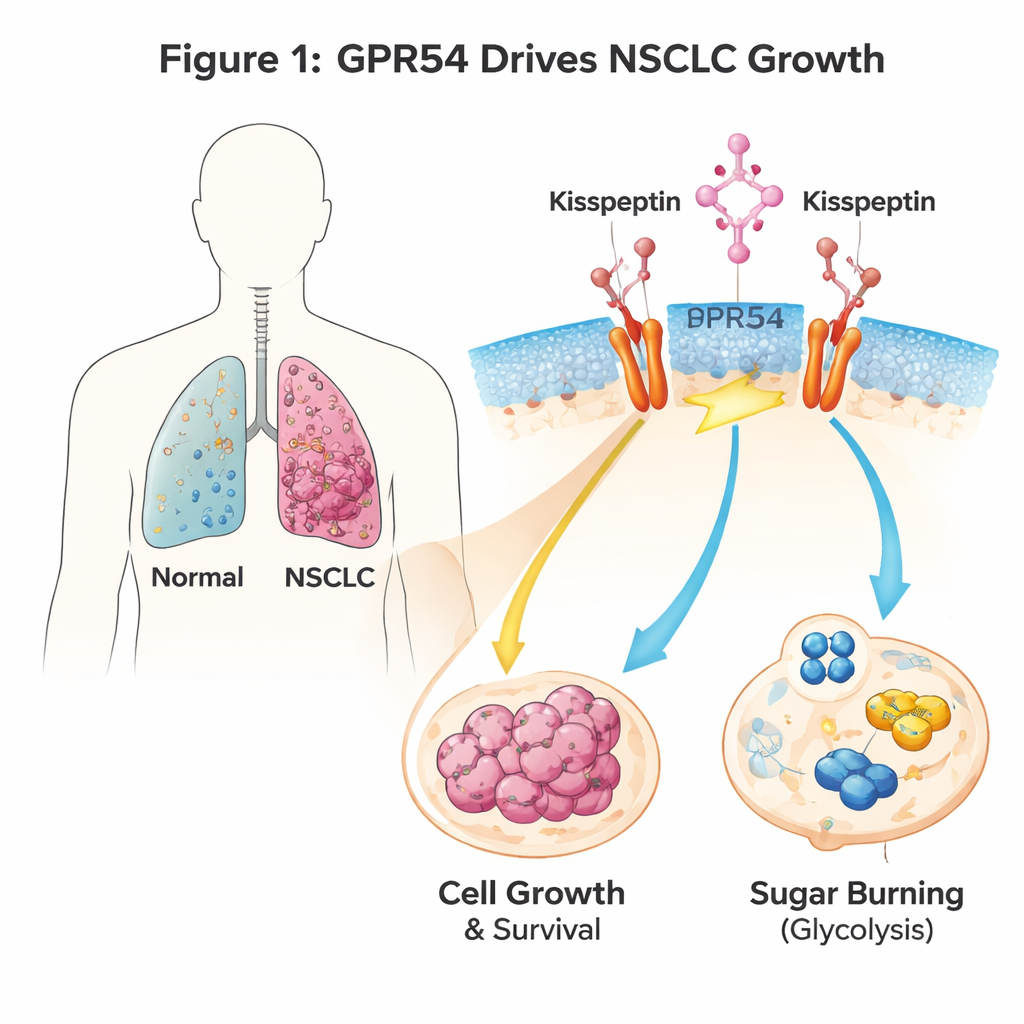
Un interruptor de señales en las células del pulmón
GPR54 es un sensor que se sitúa en la superficie de las células y responde a una señal natural llamada kisspeptina. Es más conocido por su papel en la pubertad y la reproducción, pero también aparece en muchos cánceres. Los autores usaron ratones modificados genéticamente que desarrollan CPNMC cuando se activa en las células pulmonares un gen promotor del cáncer llamado Kras. Cuando eliminaron el gen Gpr54 en estos ratones, los animales vivieron más, desarrollaron menos tumores pulmonares y de menor tamaño, y sus células cancerosas mostraron signos claros de autodestrucción (apoptosis). Las líneas celulares humanas de CPNMC contaron la misma historia: cuando se redujeron los niveles de GPR54, las células tumorales crecieron más despacio, formaron menos colonias y murieron con mayor facilidad, independientemente de sus mutaciones genéticas particulares.
Cómo GPR54 mantiene vivas a las células tumorales
Indagando más a fondo, los investigadores preguntaron qué circuitos internos utiliza GPR54. Encontraron que GPR54 alimenta dos vías de crecimiento principales dentro de la célula, conocidas como AKT y ERK. Ambas son “nodos” comunes que indican a las células cancerosas que se dividan y resistan la muerte. Cuando GPR54 fue bloqueado o eliminado, la actividad de AKT y ERK cayó y las células se volvieron más propensas a la apoptosis. Restaurar señales fuertes de AKT o ERK pudo rescatar parcialmente a las células, confirmando que GPR54 ayuda a las células de CPNMC a sobrevivir apoyándose en estos circuitos de crecimiento.
Reprogramando el uso de azúcar por parte del cáncer
Las células cancerosas a menudo reprograman su uso de nutrientes, favoreciendo la degradación rápida de azúcares (glucólisis) para impulsar el crecimiento. El perfil de actividad génica de tumores de ratón sin Gpr54 mostró que muchos genes implicados en el manejo del azúcar y la producción de energía estaban disminuidos. En células de cáncer de pulmón tratadas con kisspeptina para activar GPR54, las mediciones del uso de oxígeno y la producción de ácido —indicadores del metabolismo energético— revelaron que GPR54 potencia la glucólisis. Bloquear la vía de GPR54 en varios puntos (el interruptor Gαq/11, PI3K, AKT o mTOR) redujo el consumo de glucosa y la producción de lactato y empujó a las células hacia la apoptosis. En términos sencillos, GPR54 ayuda a las células de CPNMC a quemar azúcar más rápido y con mayor eficiencia, sosteniendo su rápido crecimiento.
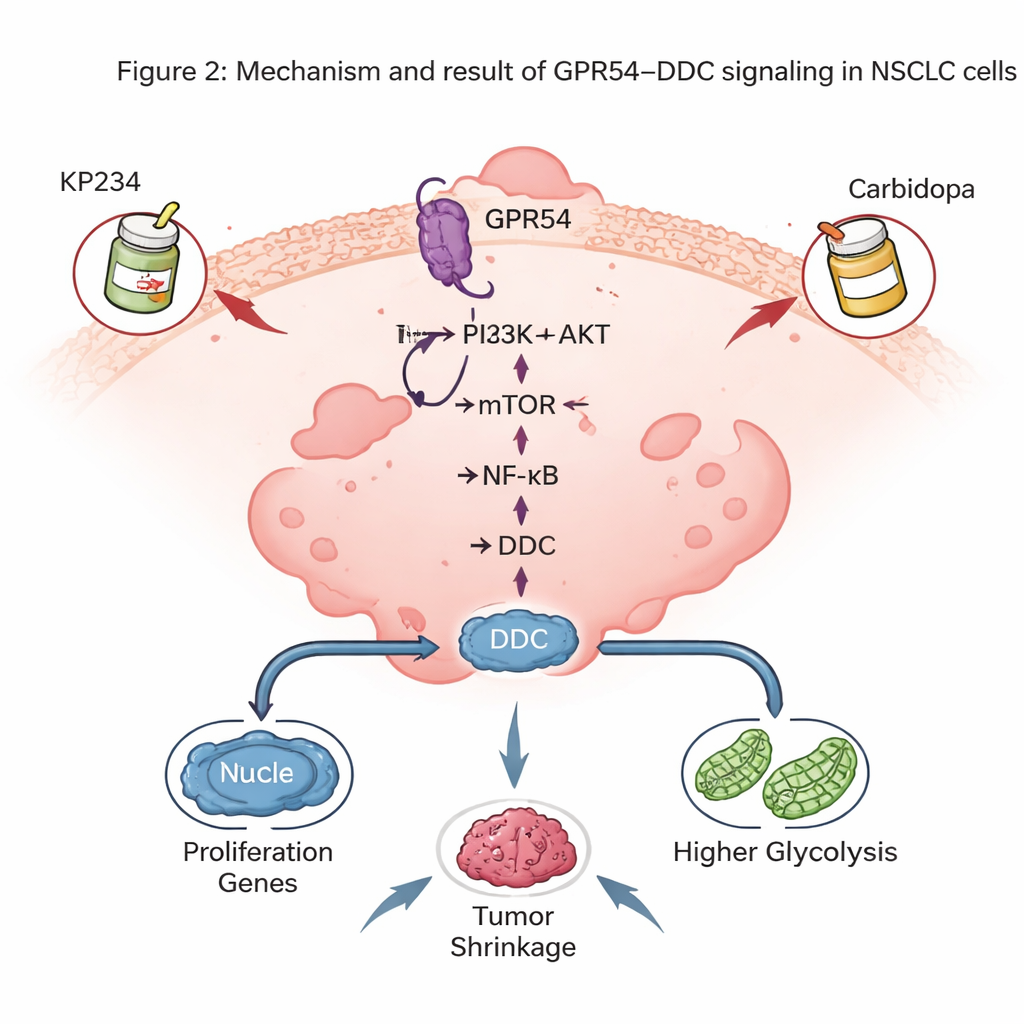
El sorprendente papel de una enzima relacionada con el cerebro
Uno de los hallazgos más llamativos fue que GPR54 controla los niveles de DDC, una enzima más conocida por fabricar los neurotransmisores dopamina y serotonina en el cerebro. En los tumores de ratón, los niveles de DDC siguieron de cerca la cantidad de GPR54: menos GPR54 implicó menos DDC. Los tumores humanos de CPNMC y las líneas celulares también mostraron más DDC que las células pulmonares normales, y los pacientes con más DDC tuvieron peor supervivencia. Reducir DDC en células de cáncer de pulmón ralentizó el crecimiento tumoral en ratones, disminuyó la división celular en cultivo y desencadenó más apoptosis. A nivel molecular, DDC ayudó a mantener la actividad de la vía NF-κB, un regulador maestro que promueve la supervivencia celular tumoral y la inflamación, y también sustentó el estado de alta glucólisis de las células tumorales.
Probando una estrategia de combinación farmacológica
Como DDC ya es blanco terapéutico en la enfermedad de Parkinson mediante un fármaco llamado carbidopa, los autores exploraron si combinar un bloqueador de GPR54 (KP234) con carbidopa podría atacar el CPNMC desde dos frentes. En cultivos celulares y en modelos de ratón donde se implantaron células humanas de CPNMC en el pulmón, el tratamiento dual redujo el crecimiento tumoral más que cualquiera de los fármacos por separado e incrementó la muerte de células cancerosas, sin pérdida de peso evidente en los animales. Estas combinaciones también mostraron potencial junto con algunos fármacos dirigidos modernos orientados a genes RAS mutantes, lo que sugiere que la señalización GPR54–DDC puede sumarse a las terapias de precisión existentes.
Qué significa esto para el futuro del cuidado del cáncer de pulmón
Para un público general, el mensaje clave es que las células de CPNMC dependen de una asociación hasta ahora poco valorada entre un interruptor de superficie (GPR54) y una enzima metabólica (DDC) para mantenerse vivas y quemar combustible rápidamente. Interrumpir esta asociación debilita a los tumores, haciéndolos crecer más despacio y morir con mayor facilidad en modelos experimentales. Aunque queda mucho trabajo antes de que tales estrategias lleguen a la clínica, este estudio posiciona a GPR54 y DDC como posibles biomarcadores para identificar CPNMC agresivos y como objetivos prometedores para nuevas combinaciones terapéuticas que podrían mejorar los resultados de pacientes cuyos cánceres actualmente esquivan las terapias estándar.
Cita: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Palabras clave: cáncer de pulmón no microcítico, GPR54, dopa descarboxilasa, metabolismo del cáncer, terapia dirigida