Clear Sky Science · es
Especies reactivas de oxígeno (ROS) en el cáncer: del mecanismo a las implicaciones terapéuticas
Cuando moléculas útiles se vuelven peligrosas
Dentro de cada célula, pequeñas chispas químicas llamadas especies reactivas de oxígeno, o ROS, se generan constantemente como parte de la vida normal. En niveles adecuados ayudan a las células a crecer, comunicarse y defenderse de gérmenes. Pero esta revisión explica cómo las mismas moléculas también pueden dañar el ADN, desordenar el cableado celular y promover que el cáncer crezca, se disemine y resista el tratamiento. Comprender esta “doble vida” de las ROS está ayudando a los científicos a diseñar nuevas terapias contra el cáncer que o bien calmen el estrés oxidativo perjudicial o deliberadamente lo aumenten para matar a las células tumorales.
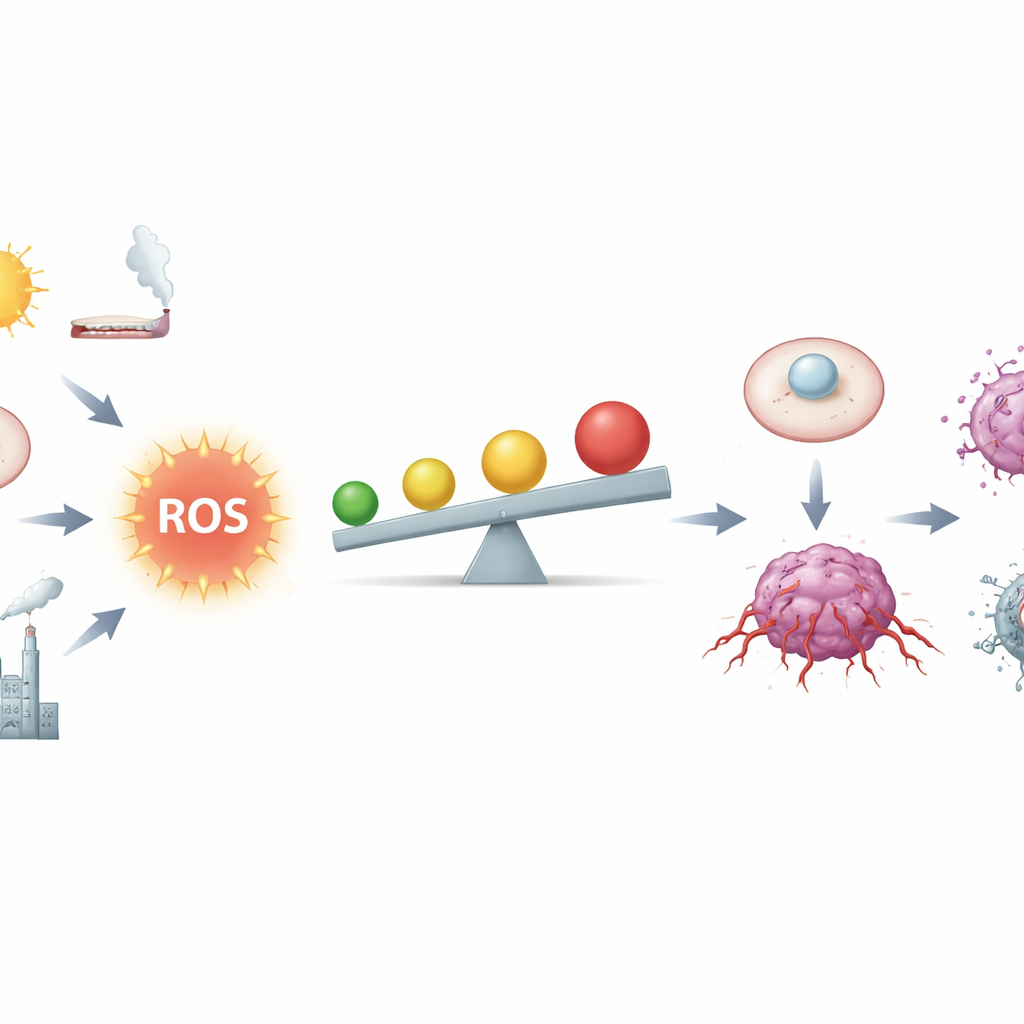
La delgada línea entre combustible y fuego
Los autores describen las ROS como subproductos químicos de la respiración y el metabolismo, pero también como mensajeros potentes. En tejidos sanos, cantidades bajas de ROS ayudan a controlar el ciclo celular, reparar daños y afinar la inmunidad. Las células mantienen estas señales bajo control mediante una red antioxidante compleja, que incluye moléculas como el glutatión y enzimas reguladas por un interruptor maestro llamado Nrf2. Sin embargo, las células cancerosas viven más cerca de la zona de peligro: genes defectuosos, mitocondrias sobrecargadas, inflamación crónica, humo de tabaco, radiación y ciertos metales aumentan las ROS. En niveles moderadamente altos, las ROS pueden provocar roturas en el ADN, desestabilizar cromosomas y activar de forma crónica circuitos de crecimiento y supervivencia, facilitando que una célula normal se convierta en cancerosa.
Cómo el estrés oxidativo moldea el comportamiento tumoral
Una vez establecido un tumor, las ROS siguen condicionando su biología. Un estrés oxidativo moderado activa muchas vías de crecimiento que fomentan la división celular, la formación de vasos sanguíneos, la invasión de tejidos cercanos y la resistencia a la quimioterapia. Las ROS pueden reprogramar el uso de azúcares, grasas y aminoácidos por parte de las células cancerosas, redirigiendo el combustible hacia rutas que generan mayor poder antioxidante y bloques de construcción para nuevas células. También influyen en las decisiones sobre el destino celular: según la intensidad y el contexto, las ROS pueden inclinar la balanza hacia señales de supervivencia o hacia varias formas de muerte celular programada, incluida la apoptosis clásica y formas más recientes como la ferroptosis, la necroptosis y la cuproptosis. Esto convierte a las ROS en cómplices de la progresión tumoral y, al mismo tiempo, en posibles desencadenantes de la autodestrucción tumoral.
Reconfigurar la inmunidad y la respuesta a fármacos
La revisión subraya que las ROS no actúan solo dentro de las células cancerosas: remodelan el vecindario tumoral. Un alto estrés oxidativo puede agotar o matar a las células T y a las células asesinas naturales que combaten el cáncer, al tiempo que favorece células supresoras que protegen al tumor del ataque. Las ROS también ayudan a los tumores a aumentar señales de “no me mates” como las proteínas de control inmunitario, atenuando los efectos de la inmunoterapia. Al mismo tiempo, niveles moderados de ROS pueden impulsar la resistencia a fármacos al potenciar bombas de expulsión de fármacos y respuestas al estrés, permitiendo que las células cancerosas eliminen la quimioterapia o reparen el daño que esta provoca. Sin embargo, en otras circunstancias, llevar las ROS más allá de un umbral crítico puede desmantelar estas defensas y resensibilizar a los tumores al tratamiento.
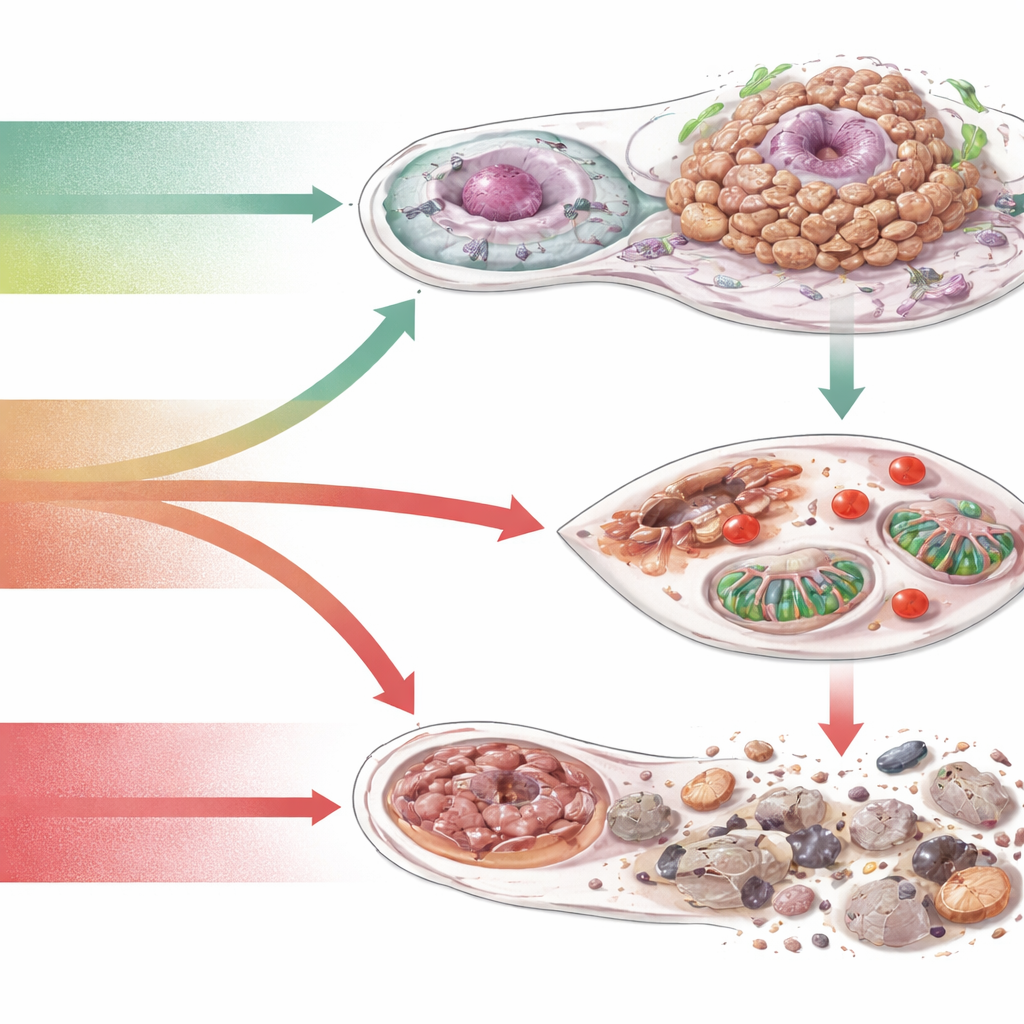
Convertir la debilidad redox en estrategia terapéutica
Puesto que las células cancerosas caminan por una cuerda floja entre usar las ROS y ser envenenadas por ellas, los autores ven el equilibrio de las ROS como una palanca terapéutica. Una estrategia amplia es reducir las ROS dañinas o reforzar los antioxidantes, principalmente para prevención o para proteger el tejido sano durante el tratamiento. Otra es hacer lo contrario en los tumores: inhibir sistemas antioxidantes o aumentar la producción de ROS hasta que las células cancerosas crucen un umbral letal, especialmente en combinación con radiación, fármacos dirigidos o inmunoterapia. Una tercera aproximación es mantener los niveles de ROS pero bloquear los interruptores sensibles a ROS específicos —proteínas de señalización, enzimas metabólicas o vías de muerte— de los que dependen los tumores. A lo largo de estas ideas corre el tema de la personalización: distintos cánceres presentan diferentes “firmas redox”, por lo que las terapias futuras podrían requerir pruebas en sangre o tejido sobre daño oxidativo, capacidad antioxidante y genes relacionados con ROS para elegir el tratamiento redox adecuado para cada paciente.
Qué significa esto para los pacientes
En términos sencillos, este artículo sostiene que las ROS no son ni totalmente malas ni totalmente buenas; son herramientas potentes que usan las células y los cánceres. Las células cancerosas tienden a operar más cerca de un punto de inflexión de estrés oxidativo que las células sanas, lo que puede crear una ventana terapéutica. Sin embargo, dado que antioxidantes y prooxidantes pueden ayudar o perjudicar según la dosis, el momento y el tipo de tumor, el uso generalizado de suplementos o fármacos que aumenten las ROS es arriesgado. Los autores concluyen que el futuro está en terapias y diagnósticos cuidadosamente diseñados que evalúen el estado redox de cada tumor y luego ajusten las ROS y los sistemas antioxidantes lo justo —ya sea para reducirlos y proteger tejidos normales, o aumentarlos para llevar a las células cancerosas más allá de su punto de ruptura.
Cita: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Palabras clave: especies reactivas de oxígeno, estrés oxidativo, metabolismo del cáncer, terapia redox, microambiente tumoral