Clear Sky Science · es
Análisis de concordancia entre perfiles de ADN y ARN: el estudio IMPACT2 del MD Anderson en oncología de precisión
Por qué esta investigación importa para los pacientes con cáncer
El tratamiento del cáncer se guía cada vez más por la composición genética del tumor de cada persona. Los médicos ya utilizan pruebas de ADN para encontrar mutaciones que pueden ser tratadas con fármacos específicos, pero estas pruebas no cuentan toda la historia sobre el comportamiento de un tumor. Este estudio del MD Anderson Cancer Center plantea una pregunta práctica: si además examinamos el ARN —las “copias de trabajo” de los genes que muestran qué genes están realmente activados o desactivados—, ¿podremos entender mejor el cáncer de un paciente y sus probabilidades de supervivencia?
Dos capas de información: ADN y ARN
Cada célula cancerosa lleva cambios en su ADN, pero el ADN es en su mayoría un plano estático. El ARN, en contraste, captura lo que la célula está haciendo activamente en un momento dado. En el ensayo IMPACT2, más de 800 pacientes con cánceres avanzados tuvieron un perfil genético de sus tumores. Para 253 de ellos, los investigadores dispusieron de datos tanto de ADN como de ARN. Compararon qué genes estaban alterados a nivel de ADN (como mutaciones o copias adicionales) y qué genes mostraban niveles de ARN inusualmente altos o bajos, preguntándose con qué frecuencia estas dos capas contaban la misma historia y si esa información se relacionaba con la supervivencia de los pacientes.
Cuando los cambios genéticos y la actividad coinciden
El equipo primero buscó eventos “concordantes”: casos en los que el mismo gen era anómalo tanto en su ADN como en su ARN. Entre los 253 pacientes, 50 tuvieron al menos una coincidencia de este tipo, sumando un total de 58 eventos en 23 genes. La mayoría de estos implicaron copias extra o ausentes de un gen que también mostraba niveles de ARN más altos o más bajos, y esta alineación fue más fuerte para genes impulsores del cáncer conocidos como CDKN2A, AR, ESR1, KRAS, PIK3CA, AKT2, TP53 y CCND1. Estos hallazgos respaldan la idea de que, para algunos genes clave en el cáncer, los cambios estructurales en el ADN se traducen efectivamente en un aumento o disminución de la actividad génica, reforzando su importancia como dianas terapéuticas.
Relaciones ocultas reveladas por señales de ARN
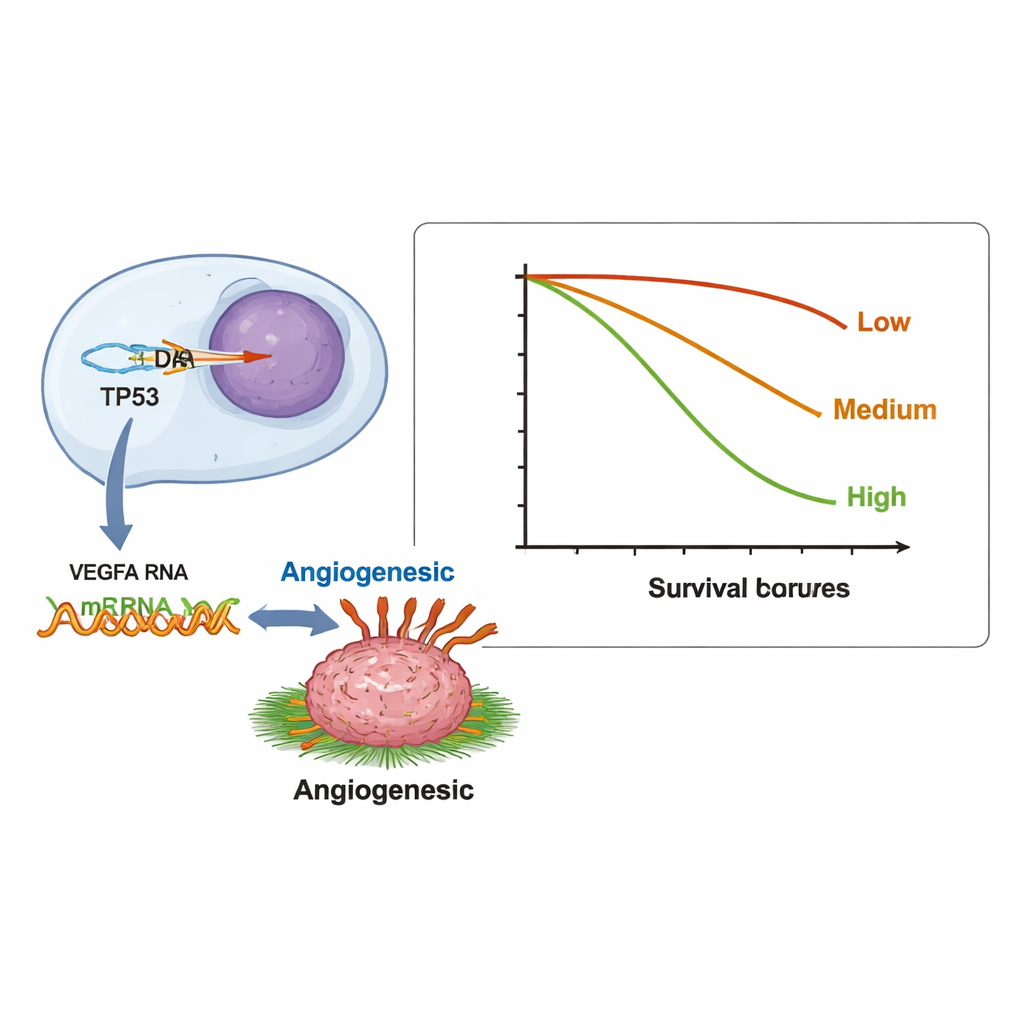
Más allá de las coincidencias uno a uno, los investigadores examinaron más de 12.000 pares de genes para ver si un cambio en el ADN de un gen estaba consistentemente vinculado con niveles anormales de ARN en otro. Encontraron 123 pares significativos. Muchos de estos se agruparon en una red principal de crecimiento y supervivencia conocida como la vía PI3K/AKT, un objetivo frecuente de fármacos dirigidos. Un patrón especialmente notable conectó cambios en el gen supresor tumoral TP53 con señales de ARN hiperactivas de VEGFA, un gen que ayuda a los tumores a construir nuevos vasos sanguíneos. Esta relación podría ayudar a explicar por qué algunos pacientes cuyos tumores presentan alteraciones en TP53 responden a bevacizumab, un fármaco que bloquea el crecimiento vascular, e ilustra cómo los datos de ARN pueden exponer interacciones gén-gén clínicamente relevantes que el ADN por sí solo puede pasar por alto.
Carga de actividad génica y supervivencia del paciente
Los investigadores también preguntaron si la cantidad global de actividad génica anómala en un tumor —lo que denominaron carga transcripcional tumoral, o TTB— se vinculaba con la duración de la supervivencia de los pacientes. Contaron cuántos genes mostraban niveles de ARN alterados en cada paciente y los agruparon en bajo (0–2 genes), intermedio (3–5) y alto (6 o más). Los pacientes en el grupo alto vivieron una mediana de 6,7 meses, en comparación con 9,8 y 11,9 meses en los grupos con menos genes alterados. En otras palabras, los tumores con muchos genes que se comportan mal a nivel de ARN tendieron a ser más agresivos. Los tumores que carecían de PD-L1, un marcador usado con frecuencia para seleccionar pacientes para inmunoterapia, también tendieron a tener más genes con expresión anormal, lo que sugiere un posible vínculo entre la extensa alteración génica y un entorno tumoral que resiste el ataque inmune.
Qué significa esto para la atención del cáncer en el futuro
Este estudio muestra que el perfilado de ARN añade información útil y complementaria a las pruebas de ADN en pacientes reales con cánceres avanzados. En algunos genes, los cambios en el ADN y la actividad del ARN coinciden y refuerzan dianas terapéuticas conocidas; en otros, los patrones de ARN descubren nuevas relaciones que podrían orientar la elección de fármacos, como el vínculo entre TP53 y VEGFA. Lo más importante para los pacientes es que una alta carga de actividad génica anómala se asoció con una menor supervivencia, lo que sugiere que las medidas basadas en ARN podrían ayudar a los médicos a evaluar la agresividad de un tumor y afinar el pronóstico. Aunque las pruebas de ARN aún no se usan de forma rutinaria para escoger terapias, estos hallazgos respaldan su promesa como siguiente paso en la oncología de precisión, especialmente a medida que estudios más amplios y mejores herramientas analíticas faciliten la incorporación del perfilado transcriptómico a la atención oncológica cotidiana.
Cita: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
Palabras clave: oncología de precisión, perfilado de ARN, secuenciación de ADN, carga transcripcional tumoral, biomarcadores del cáncer