Clear Sky Science · es
Los subtipos moleculares de consenso del carcinoma escamoso de esófago
Por qué esta investigación importa para los pacientes
El carcinoma escamoso de esófago es un cáncer mortal de la garganta con pocas opciones de tratamiento a medida y una supervivencia generalmente pobre. Los médicos saben que no todos los tumores se comportan igual, pero hasta ahora no había una forma clara y unificada de clasificar estos cánceres en grupos biológicamente significativos. Este estudio integra múltiples capas de datos genéticos e imágenes para definir cuatro tipos principales de este cáncer y demuestra que una simple imagen de un portaobjetos al microscopio a menudo puede revelar el tipo que tiene un paciente. Eso abre la puerta a tratamientos más precisos y menos basados en prueba y error.
Poniendo orden en un panorama tumoral confuso
En la última década, distintos equipos de investigación propusieron al menos siete formas de dividir este cáncer según mutaciones en el ADN, cambios en el número de copias, actividad génica u otras medidas moleculares. Cada sistema usó datos y métodos diferentes, lo que generó subtipos superpuestos pero no idénticos y dificultó su uso en la práctica clínica. Los autores reanalizaron primero un grupo bien caracterizado de 152 pacientes chinos con múltiples capas de datos disponibles, incluidos secuenciación del genoma completo, actividad génica, metilación del ADN y perfiles de microARN. Usando un método llamado fusión de redes de similitud (similarity network fusion), combinaron todos estos datos en una sola imagen e identificaron cuatro subtipos multi-ómicas. Luego construyeron una “red de subtipos” estadística que vinculó sus nuevos grupos con 21 subtipos previamente publicados, revelando conexiones sólidas entre los estudios.
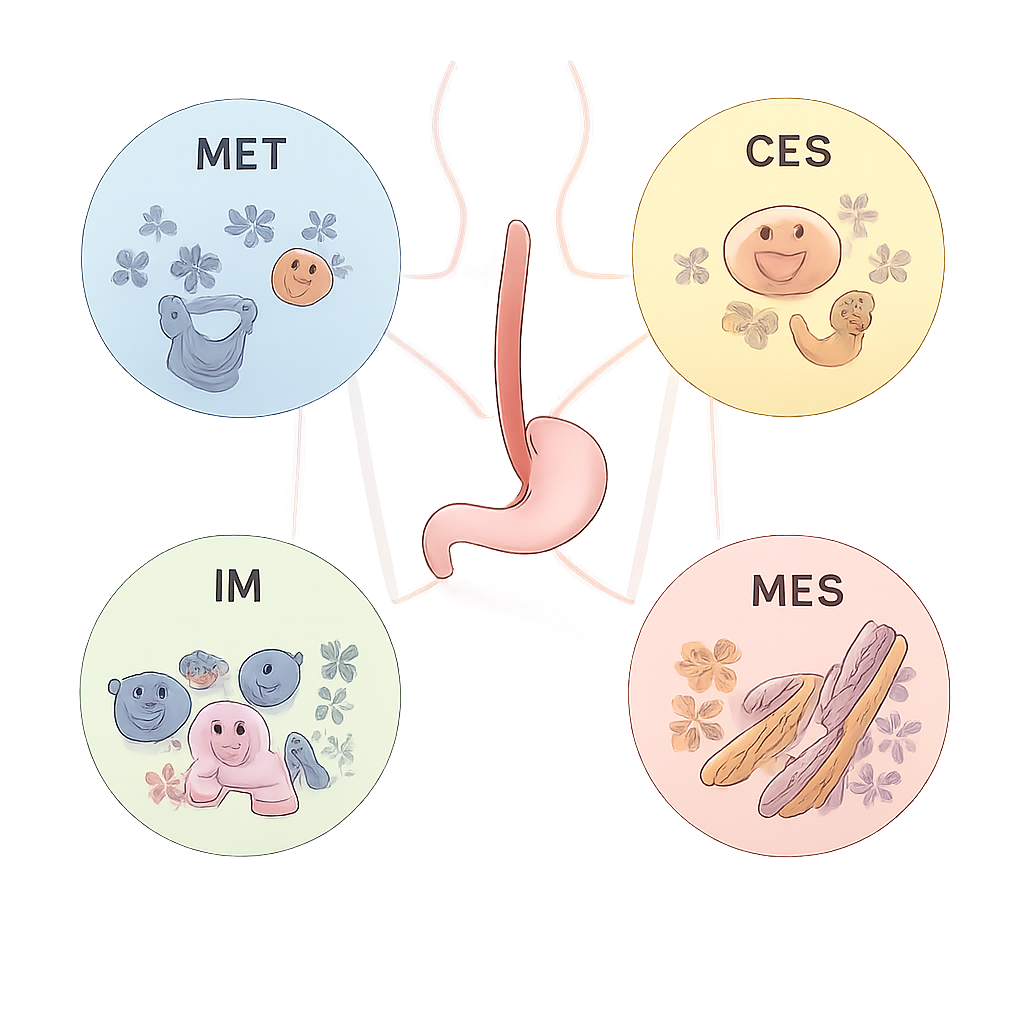
Cuatro personalidades biológicas principales del tumor
A partir de esa red, el equipo destiló cuatro subtipos moleculares de consenso, nombrados ECMS1 a ECMS4, cada uno con un comportamiento distinto. ECMS1, el tipo metabólico (MET), muestra alta actividad en vías que procesan fármacos y nutrientes y activación frecuente del gen NFE2L2, lo que puede impulsar la resistencia a la quimioterapia y la radioterapia. ECMS2, el tipo clásico (CLS), está dominado por una fuerte actividad del ciclo celular y de señales de crecimiento, y con frecuencia presenta copias adicionales del gen ERBB2 (HER2). ECMS3, el tipo inmune (IM), tiene una carga mutacional global más baja pero una activa respuesta inmunitaria, incluyendo altos niveles de la vía de control PD-1. ECMS4, el tipo mesenquimal (MES), muestra señales de remodelado tisular, crecimiento vascular y transformación de células hacia un estado más móvil e invasivo, características asociadas a peores resultados.
Vinculando subtipos con pronóstico y elecciones terapéuticas
Cuando los investigadores compararon estos cuatro grupos con los datos clínicos de los pacientes, surgieron patrones claros. Los pacientes con tumores mesenquimales ECMS4 presentaron el mayor riesgo de recurrencia y la peor supervivencia global y libre de enfermedad. El grupo inmune ECMS3, a pesar de su entorno inmune activo, respondió mal a la quimiorradioterapia estándar pero mostró una mayor tasa de beneficio con un medicamento de inmunoterapia anti–PD-1. Los tumores clásicos ECMS2 parecieron más sensibles a quimioterapias comunes como cisplatino y taxanos, y su frecuente amplificación de HER2 sugiere que podrían beneficiarse de fármacos dirigidos contra HER2. Los tumores metabólicos ECMS1, enriquecidos en la actividad de NFE2L2 y ciertos receptores de factores de crecimiento, podrían tratarse mejor con fármacos que apunten a esas vías metabólicas y de señalización. En resumen, los cuatro subtipos sugieren vulnerabilidades distintas y diferentes respuestas probables a las terapias.
Enseñar a un ordenador a ver pistas moleculares en portaobjetos rutinarios
Dado que la caracterización molecular completa es cara y no está disponible en muchos hospitales, el equipo se preguntó si los portaobjetos patológicos rutinarios teñidos con hematoxilina y eosina (H&E) podrían servir como proxy. Entrenaron un sistema de aprendizaje profundo con decenas de miles de fragmentos de imagen anotados para reconocer elementos tisulares básicos como células tumorales, estroma, linfocitos, glándulas y músculo. A partir de imágenes de portaobjetos completos, calcularon luego “características de organización espacial”: cuánto hay de cada tipo de tejido, cómo están dispuestos y cómo se mezclan o separan. Estos patrones derivados de la imagen reflejaron la biología de los cuatro subtipos: por ejemplo, el tipo inmune ECMS3 mostró más linfocitos y estructuras normales, mientras que el tipo mesenquimal ECMS4 mostró más estroma de soporte. Usando estas características, construyeron un clasificador basado en imágenes, llamado imECMS, que pudo asignar portaobjetos a MET, CLS, IM o MES con buena precisión en varios grupos independientes de pacientes.
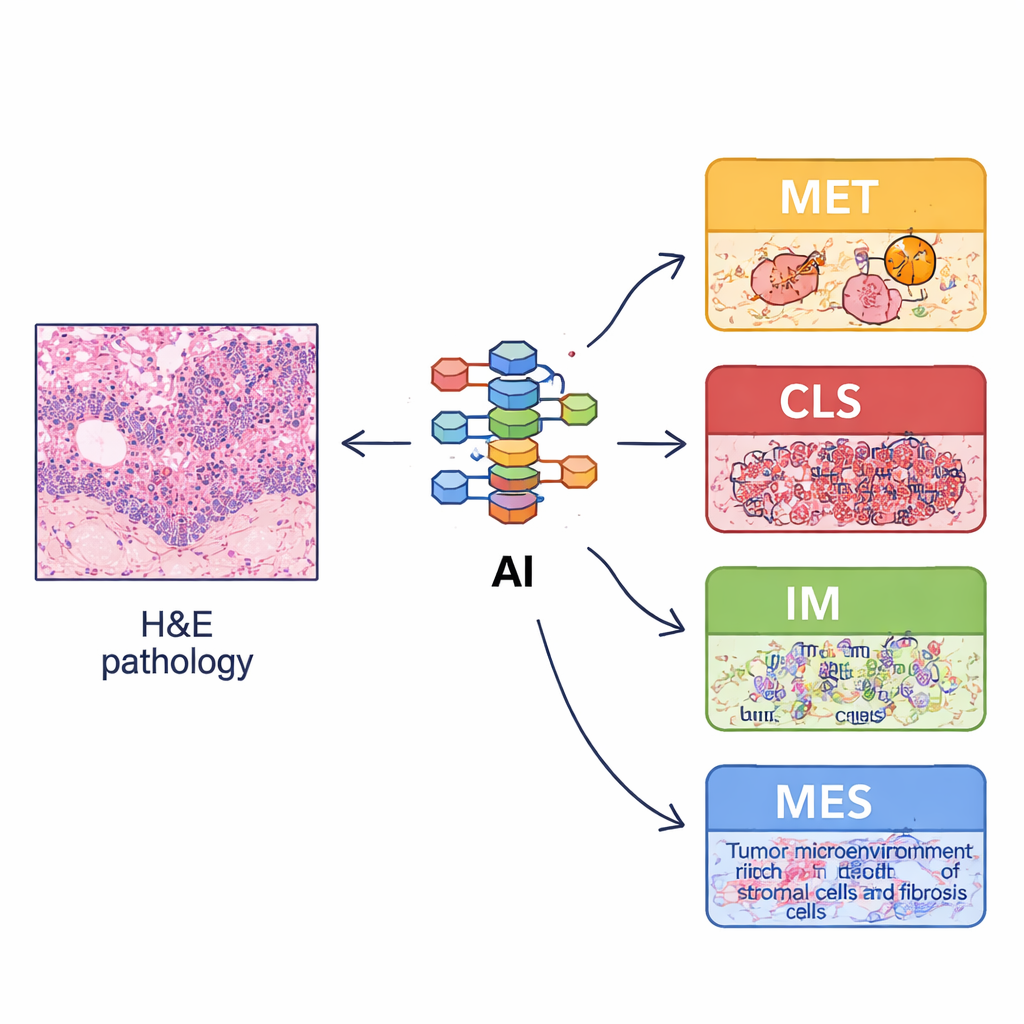
Qué significa esto para la atención futura
Para quienes no son especialistas, la conclusión es que este estudio transforma un cáncer aparentemente uniforme en cuatro enfermedades biológicamente distintas, cada una con su curso probable y sus mejores estrategias terapéuticas. Aún más importante, muestra que gran parte de esta información puede extraerse automáticamente de las imágenes microscópicas estándar que ya tiene todo paciente, sin necesidad de costosas secuenciaciones. Con una validación adicional en poblaciones más grandes y diversas, los sistemas ECMS e imECMS podrían ayudar a los médicos a emparejar a los pacientes con carcinoma escamoso de esófago con las terapias de las que tienen más probabilidad de beneficiarse, al tiempo que se les evita tratamientos poco probables de ser eficaces.
Cita: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Palabras clave: cáncer de esófago, subtipos tumorales, oncología de precisión, patología con aprendizaje profundo, inmunoterapia