Clear Sky Science · es
El antígeno nuclear 1 exógeno del virus de Epstein-Barr induce resistencia tumoral impulsada por ADAR1 frente a la inmunoterapia
Por qué un virus común importa para el tratamiento del cáncer
Hoy muchos cánceres se tratan con fármacos de inmunoterapia que liberan el propio sistema inmunitario del organismo. Sin embargo, la mayoría de los pacientes aún no se benefician porque sus tumores aprenden a esconderse del ataque inmunitario. Este estudio revela cómo un virus muy común, el virus de Epstein-Barr (VEB), ayuda a los tumores a apagar las defensas inmunitarias y a resistir estos potentes fármacos, y cómo un nuevo tipo de molécula diseñada podría reactivar esas defensas.
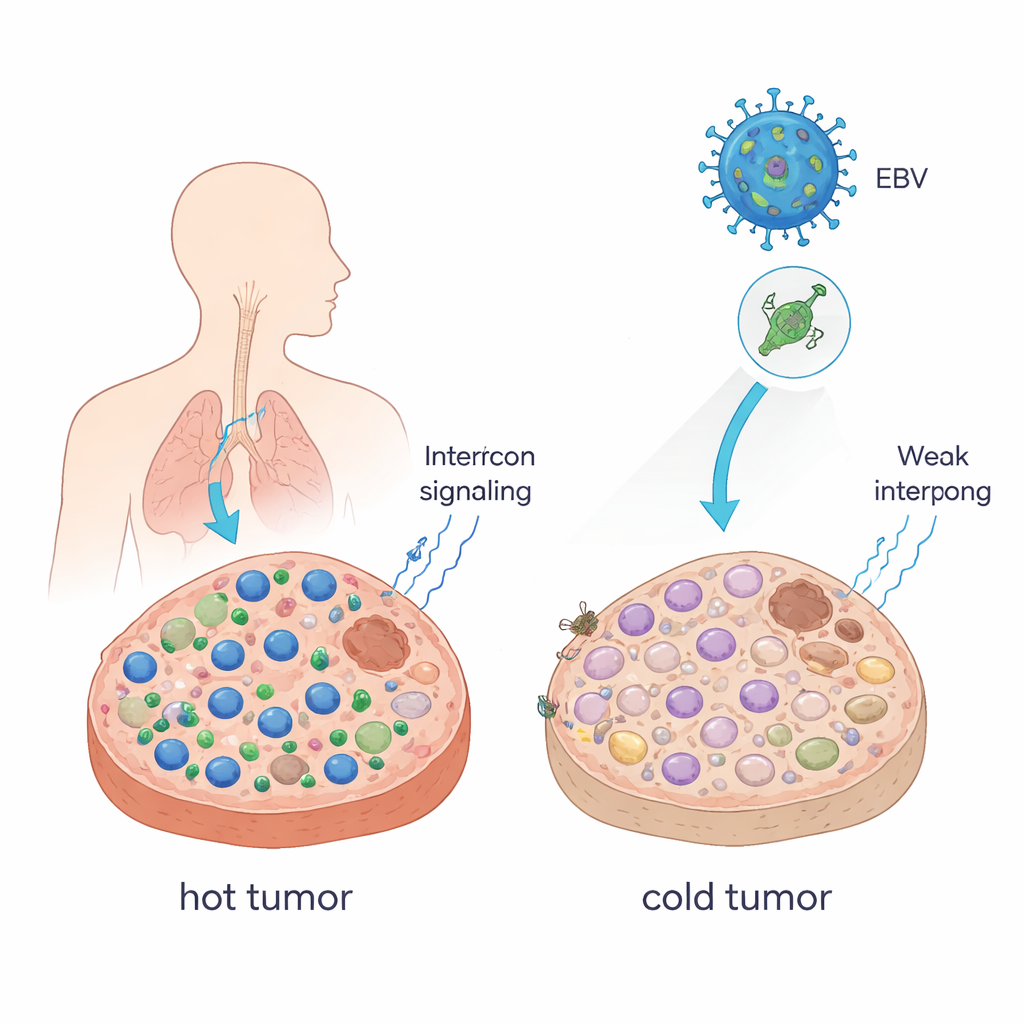
Convertir tumores calientes en fríos
Los médicos suelen describir los tumores como “calientes” cuando están llenos de células T que matan el cáncer, y “fríos” cuando esas células son escasas. Los tumores calientes suelen responder bien a los inhibidores de puntos de control inmunitario (ICB), como los anticuerpos anti–PD-1; los tumores fríos a menudo no. Los autores demostraron que una sola proteína del VEB, llamada EBNA1, puede empujar a los tumores hacia ese estado más frío y evasivo. Cuando forzaron a células tumorales de ratón a producir EBNA1 y las hicieron crecer en ratones con sistemas inmunitarios intactos, los tumores crecieron más, contenían menos células CD8+ y células asesinas naturales, y tenían más macrófagos inmunosupresores. Las señales llamadas interferones —mensajeros clave que ayudan a movilizar las células inmunitarias— también se redujeron de forma marcada. En muestras de pacientes con carcinoma nasofaríngeo, un cáncer estrechamente ligado al VEB, los tumores que expresaban EBNA1 mostraron de manera similar menos células CD8+ que el tejido normal.
Un atajo viral hacia la maquinaria de control del ARN de la célula
Para entender cómo EBNA1 remodela el entorno tumoral, los investigadores buscaron proteínas humanas que interaccionaran físicamente con ella. Se centraron en una proteína llamada IGF2BP3, que reconoce pequeñas marcas químicas (m6A) en los ARNm y puede aumentar su estabilidad o su traducción en proteína. EBNA1 se unió fuertemente a IGF2BP3 en varios tipos celulares, incluidas células cancerosas positivas para VEB. Datos de tumores de pacientes mostraron que niveles elevados de IGF2BP3 iban acompañados de una débil actividad de genes relacionados con interferón y de menor infiltración de células T CD8+, lo que sugiere que esta alianza virus-huésped podría atenuar la inmunidad antitumoral.
Potenciar un editor de ARN que silencia señales de peligro
Un análisis más profundo destacó un objetivo clave de esta interacción: ADAR1, una enzima que edita ARN de doble cadena cambiando ciertas letras “A” por “I”. Esta edición puede hacer que el ARN de apariencia viral dentro de las células parezca menos peligroso para los sensores internos, reduciendo las respuestas por interferón. Los autores encontraron que EBNA1, IGF2BP3 y un factor de traducción llamado EIF4G1 forman un complejo trímero sobre el ARNm de ADAR1. Este complejo incrementa el marcado m6A, recluta la maquinaria de traducción y aumenta selectivamente la producción de la proteína ADAR1 sin elevar sus niveles de ARN. Como resultado, las células tumorales realizan más edición de ARN en elementos genéticos repetidos situados cerca de genes relacionados con interferón. Estas ediciones reducen el conjunto de ARN de doble cadena sin editar que normalmente alertaría a sensores como MDA5 y PKR, atenuando la producción de interferón y ayudando a los tumores a ocultarse del ataque inmunitario.
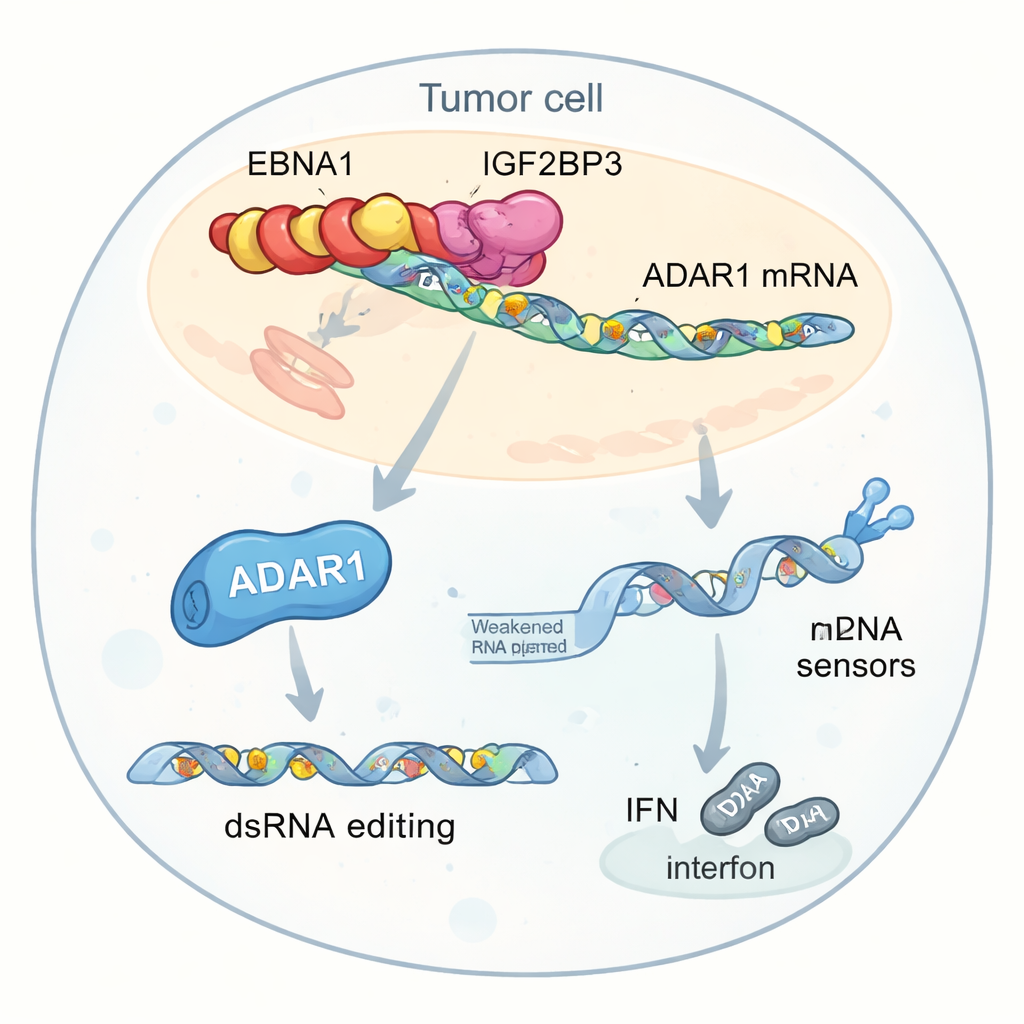
Menos interferón, inmunoterapia más débil
Cuando las células tumorales que expresaban EBNA1 se expusieron en el laboratorio a células T y a anticuerpos anti–PD-1, fueron más difíciles de matar que las células control y liberaron menos interferón. Incluso tratadas directamente con interferón, las células con EBNA1 mostraron menor sensibilidad y sus sensores de ARN internos se activaron menos. Reducir los niveles de ADAR1 revirtió parcialmente esos efectos, restaurando la actividad de los sensores y la señalización por interferón. Experimentos genéticos y de secuenciación confirmaron que las células que expresan EBNA1 mostraron más eventos de edición de A a I en regiones específicas de ARN, particularmente tras la estimulación con interferón, lo que respalda la idea de que el impulso viral de ADAR1 ayuda a neutralizar señales de peligro que de otro modo desencadenarían fuertes respuestas inmunitarias.
Un degradador diseñado que reaviva el ataque inmunitario
El equipo se preguntó entonces si despojar a los tumores de EBNA1 podría restaurar su vulnerabilidad a la inmunoterapia. Diseñaron una molécula PROTAC, EP-1215, que etiqueta a EBNA1 para su destrucción por el propio sistema de eliminación de la célula. A dosis bajas, EP-1215 degradó de manera eficiente EBNA1 y redujo los niveles de proteína ADAR1. En experimentos en ratones, EP-1215 por sí solo tuvo un impacto limitado en tumores positivos para EBNA1, y el anti–PD-1 solo también fue débil. Pero combinados, ambos tratamientos redujeron drásticamente los tumores, aumentaron la infiltración de células T CD8+ y elevaron las células T productoras de interferón. En modelos de ratón humanizados que portaban células inmunitarias humanas y tumores relacionados con VEB, la combinación volvió a superar a los tratamientos individuales, sin toxicidad evidente en hígado o riñones.
Qué significa esto para la atención oncológica futura
Para no especialistas, el mensaje es que un virus común puede reconfigurar silenciosamente las células cancerosas para atenuar los sistemas de alarma internos, apagando señales químicas que de otro modo atraerían y activarían a las células inmunitarias. EBNA1 hace esto secuestrando un lector de ARN del hospedador (IGF2BP3) y un factor de traducción (EIF4G1) para sobreproducir el editor de ARN ADAR1, que edita las mismas estructuras de ARN que los sensores inmunitarios están diseñados para reconocer. Al degradar EBNA1 con un PROTAC a medida como EP-1215, los autores lograron restaurar estas señales de peligro y volver a hacer que tumores resistentes respondieran a los fármacos de bloqueo de puntos de control existentes. Si estrategias similares demuestran ser seguras y eficaces en humanos, dirigir a ayudantes virales como EBNA1 podría ofrecer una nueva forma de convertir tumores fríos vinculados al VEB en objetivos calientes que la inmunoterapia moderna pueda finalmente atacar.
Cita: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Palabras clave: Virus de Epstein-Barr, resistencia a la inmunoterapia, ADAR1, edición de ARN, carcinoma nasofaríngeo