Clear Sky Science · es
Mecanismo molecular de la fusión de membranas dependiente del colesterol en la entrada de SARS-CoV-2
Por qué el colesterol importa para un virus respiratorio
El virus que causa la COVID-19, SARS-CoV-2, entra en nuestras células fusionando su capa externa con las membranas celulares. Este artículo aborda una pregunta aparentemente sencilla pero de gran alcance: ¿hasta qué punto el colesterol —una sustancia grasa más conocida por su papel en las enfermedades cardiacas— condiciona ese paso de fusión? Los autores muestran que el colesterol en la membrana viral no solo modula la eficiencia de la infección; en realidad ayuda a organizar las proteínas espiga del virus en plataformas de acoplamiento potentes que facilitan y hacen más fiable la entrada.
Construyendo un modelo mínimo de entrada viral
Para desentrañar este proceso, los investigadores reconstruyeron el encuentro virus–célula en una probeta usando pequeñas burbujas grasas llamadas liposomas. Un conjunto de liposomas portaba la proteína espiga de SARS-CoV-2 y representaba la membrana viral; el otro llevaba el receptor ACE2, imitando la superficie de la célula hospedadora. Al mezclarlos y activarlos con enzimas específicas que “cortan” la espiga dejándola lista para fusionar, estas membranas artificiales se fusionaron, permitiendo que un tinte fluorescente pasara de una burbuja a la otra. Este sistema simplificado permitió al equipo ajustar con precisión la composición lipídica —incluidos los niveles de colesterol— en cada lado y observar cómo se desarrollaba la fusión paso a paso. 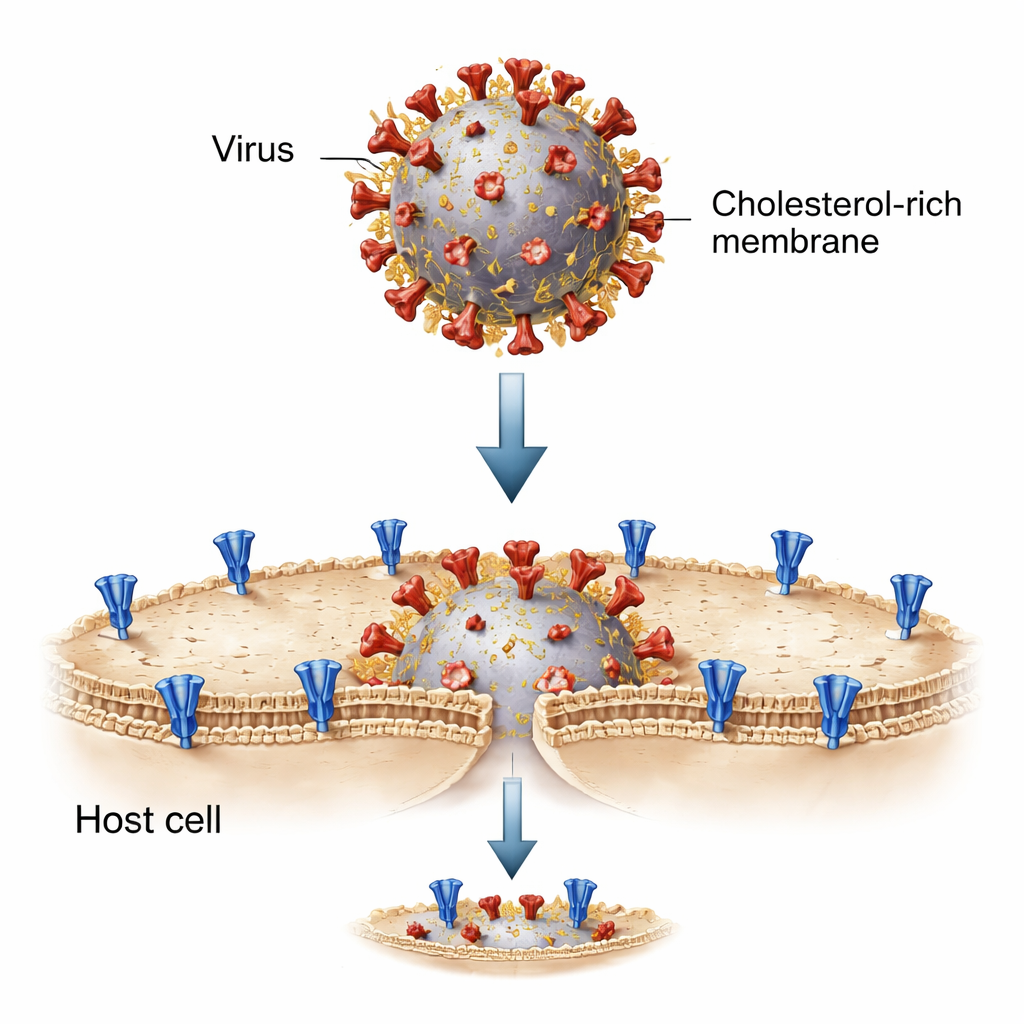
El colesterol potencia el acoplamiento más que la fusión
Al regular el colesterol hacia arriba y hacia abajo, el equipo descubrió que añadir colesterol a la membrana portadora de la espiga aumentaba la frecuencia de fusión, pero no de la manera que podría esperarse. Un alto contenido de colesterol no cambió de forma drástica la probabilidad de que dos membranas ya adheridas se fusionaran. En cambio, incrementó de forma marcada la frecuencia con la que las vesículas con espiga se acoplaban inicialmente a las vesículas con ACE2. La imagen a nivel de partícula única mostró muchos más eventos de acoplamiento exitosos cuando la espiga estaba en membranas ricas en colesterol, mientras que la probabilidad de que un par acoplado llegara a fusionarse completamente se mantuvo aproximadamente constante. Curiosamente, cargar colesterol en el lado de ACE2 aportó poco beneficio e incluso, en niveles muy altos, dificultó la fusión, lo que apunta al colesterol viral —y no al del hospedador— como el principal impulsor.
De membranas modelo a células vivas
Los investigadores preguntaron luego si el mismo patrón se mantenía en células vivas. Modificaron células humanas para que expresaran o bien la espiga o bien ACE2 y observaron que formaban grandes estructuras fusionadas, o sincitios, al mezclarlas. Eliminar el colesterol de las células que expresaban la espiga casi abolió la formación de sincitios, mientras que restaurar el colesterol rescató la fusión. En experimentos paralelos con “pseudovirus” de SARS-CoV-2 (partículas virales inocuas que usan la espiga del coronavirus para entrar en células), eliminar el colesterol de la membrana viral redujo drásticamente la infección, y volverlo a añadir la aumentó de forma dependiente de la dosis. En contraste, alterar el colesterol únicamente en las células que expresan ACE2 produjo pocos cambios. En todos los ensayos, el mensaje fue coherente: el colesterol en la membrana que contiene la espiga es esencial para una entrada eficiente.
Agrupaciones de espiga: el arma secreta del colesterol
¿Por qué importaría tanto el colesterol del lado viral? Imágenes de alta resolución de membranas celulares revelaron que las proteínas espiga tienden a formar cúmulos densos cuando el colesterol es abundante, pero permanecen más dispersas cuando éste está agotado. Mediciones de molécula única fueron más allá y mostraron que estos cúmulos contienen más copias de la espiga en condiciones ricas en colesterol. Los autores rastrearon este efecto hasta una región rica en cisteínas (RRC) en la cola de la espiga, dentro de la membrana viral. Este segmento se modifica por palmitoilación —un tipo de “ancla” grasa que favorece los parches ricos en colesterol. Cuando el equipo truncó la cola de la espiga o mutó las diez cisteínas para bloquear la palmitoilación, la espiga dejó de agruparse con el colesterol y desapareció el impulso en el acoplamiento y la fusión inducido por colesterol. 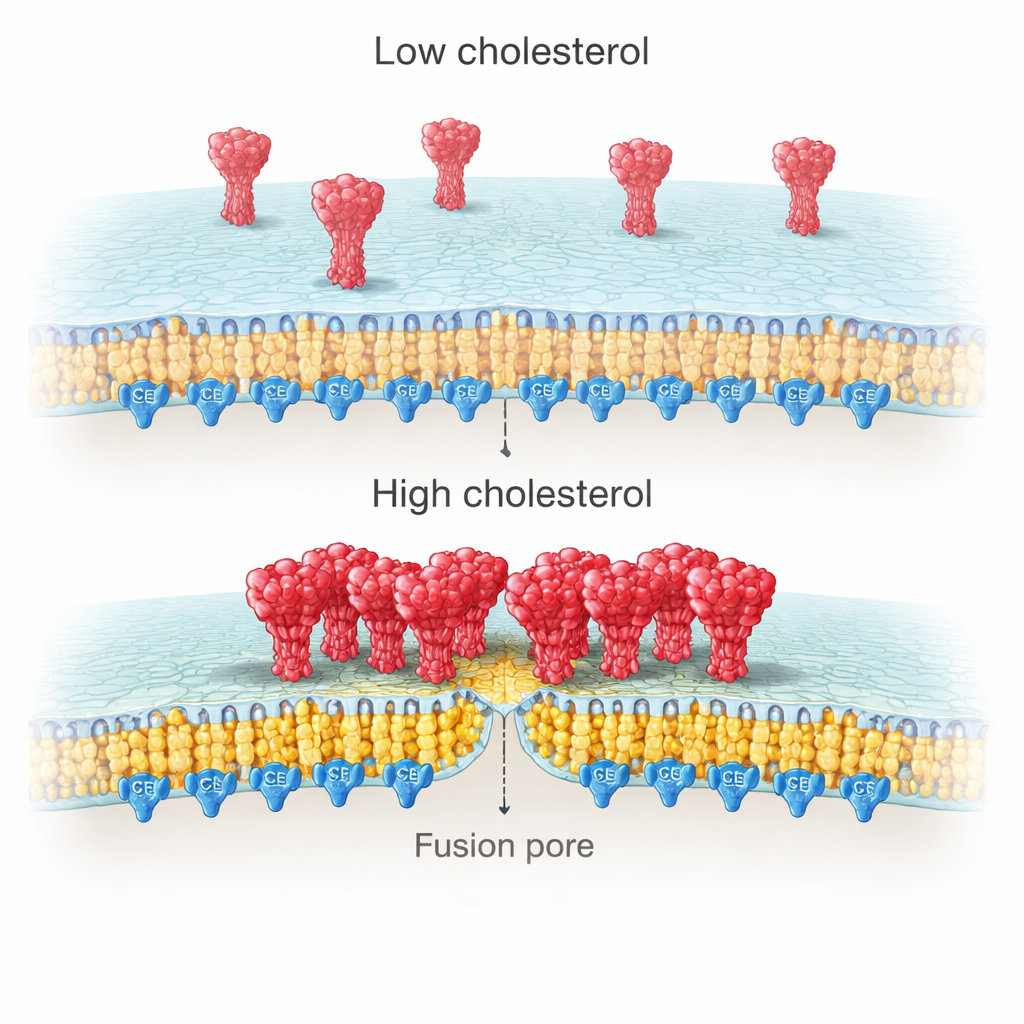
Cómo esto podría ayudar a futuros tratamientos
En términos sencillos, el estudio concluye que el colesterol convierte la membrana viral en una plataforma de fusión al reunir muchas proteínas espiga en cúmulos compactos mediante su región de cola palmitoilada. Estos cúmulos se acoplan con mayor eficiencia a ACE2 en las células hospedadoras, aumentando las probabilidades de que cualquier encuentro concreto conduzca a una fusión e infección exitosas. Para el lector no especialista, la idea clave es que el colesterol no es solo un ingrediente pasivo del envoltorio viral; es un organizador activo de la maquinaria de la espiga. Esto convierte a la cola rica en cisteínas, sensible al colesterol, y a las enzimas que la palmitoilan, en dianas prometedoras para estrategias antivirales de amplio espectro que podrían funcionar frente a distintas variantes de coronavirus.
Cita: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Palabras clave: colesterol, espícula de SARS-CoV-2, fusión de membranas, entrada viral, palmitoilación