Clear Sky Science · es
PKC-eta promueve la metástasis del cáncer de mama al regular la vía de señalización Hippo–YAP
Por qué importa esta investigación
El cáncer de mama triple negativo (TNBC) es una de las formas más peligrosas de cáncer de mama porque se disemina pronto y carece de tratamientos dirigidos. Este estudio descubre cómo una enzima específica dentro de las células cancerosas, llamada PKC‑eta (PKCη), actúa como un interruptor maestro que ayuda a los tumores a desprenderse, viajar por el cuerpo y sembrar nuevos tumores. Al comprender este interruptor, los investigadores también identifican un pequeño péptido natural que puede apagarlo, lo que apunta a una posible nueva vía de tratamiento para esta enfermedad agresiva. 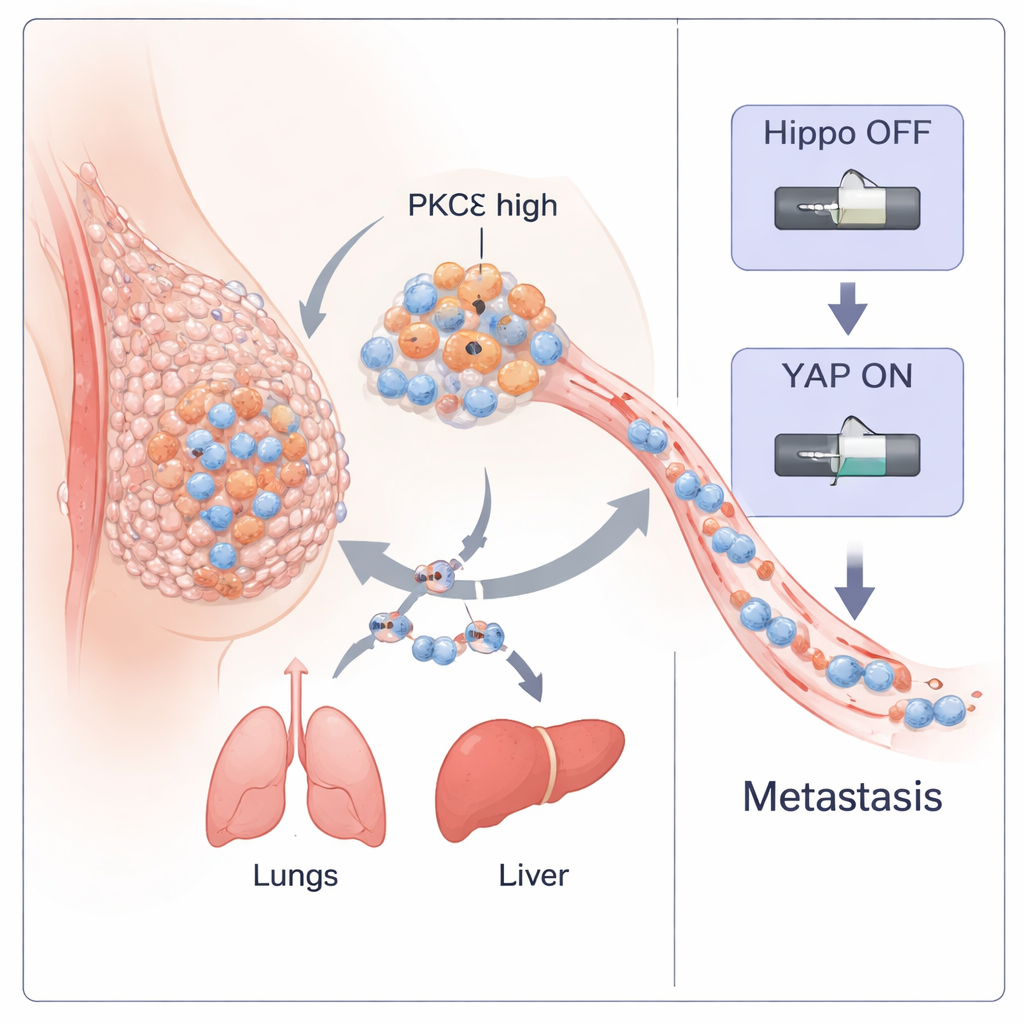
Un conductor oculto en tumores mamarios agresivos
El equipo comenzó analizando amplias colecciones de datos de pacientes con cáncer de mama. Encontraron que el gen que codifica PKCη (PRKCH) está especialmente alto en un subtipo de tumores conocido como “claudin‑low”, que se solapa de forma importante con el TNBC y es rico en células de tipo madre y altamente móviles. En múltiples cohortes de pacientes, los tumores con PRKCH elevado mostraron fuertes firmas de transición epitelio‑mesénquima (EMT): un proceso en el que células antes ordenadas aflojan sus adhesiones, cambian de forma y se vuelven más invasivas. Los niveles de PRKCH también fueron más altos en muestras metastásicas que en los tumores primarios originales, y la tinción proteica de tejidos humanos de TNBC mostró PKCη activo y perinuclear en cánceres de mayor grado y estadio avanzado. En conjunto, estos hallazgos sugirieron que PKCη está estrechamente ligado a la agresividad tumoral y a la diseminación.
Del plato de cultivo al ratón: demostrando que PKCη impulsa la diseminación
Para probar causa y efecto, los investigadores emplearon edición génica CRISPR para eliminar PKCη de dos líneas celulares TNBC altamente metastásicas, una de ratón (4T1) y otra humana (MDA‑MB‑231). Sin PKCη, las células se desplazaron hacia un estado más “epitelial”: aumentaron proteínas de adhesión como E‑cadherina y EpCAM, y redujeron marcadores mesenquimales clásicos como vimentina y N‑cadherina. Estas células deficientes en PKCη formaron colonias más pequeñas y en menor número, migraron e invadieron con menos eficiencia, fueron más sensibles a la muerte celular al desprenderse y mostraron una caída marcada en rasgos de células madre cancerosas, incluyendo menos células CD44high/CD24low y positivas para ALDH, y menor capacidad de formar esferas. Cuando se inyectaron en ratones, las células sin PKCη produjeron tumores primarios más pequeños y muchas menos metástasis en pulmones, hígado, cerebro y otros órganos; además, los ratones vivieron más tiempo. Restaurar PKCη revirtió estos cambios, confirmando que la enzima promueve activamente la progresión y la diseminación del TNBC.
Cómo PKCη secuestra una vía de control del crecimiento
El estudio se centró luego en cómo PKCη ejerce este poder prometastásico. Los datos de pacientes revelaron que los niveles de PKCη suben y bajan en paralelo con YAP, una potente proteína reguladora controlada por la vía Hippo—un “freno de seguridad” celular que normalmente restringe el crecimiento. Altos niveles de PRKCH o YAP1 predijeron peores resultados en pacientes, y niveles elevados de ambos a la vez se asociaron con una supervivencia libre de metástasis a distancia particularmente mala. En células TNBC, eliminar PKCη redujo los niveles totales de YAP y lo desplazó del núcleo al citoplasma, donde está inactivo. Experimentos bioquímicos mostraron que PKCη se une físicamente a YAP y añade específicamente un grupo fosfato en la posición Ser128. Esta modificación estabiliza YAP y facilita su entrada al núcleo para activar genes que impulsan la EMT, la capacidad de tipo madre y la metástasis. Cuando PKCη está ausente, YAP se fosforila en otros sitios (Ser127 y Ser397) que hacen que se una a proteínas 14‑3‑3, quede atrapado en el citoplasma y sea degradado. PKCη además aumenta PTEN—un freno natural sobre la enzima AKT—mantuviendo así baja la actividad de AKT y suprimiendo las quinasas Hippo aguas arriba que de otro modo inactivarían YAP. De este modo, PKCη activa directamente a YAP e indirectamente mantiene el “freno” Hippo desactivado. 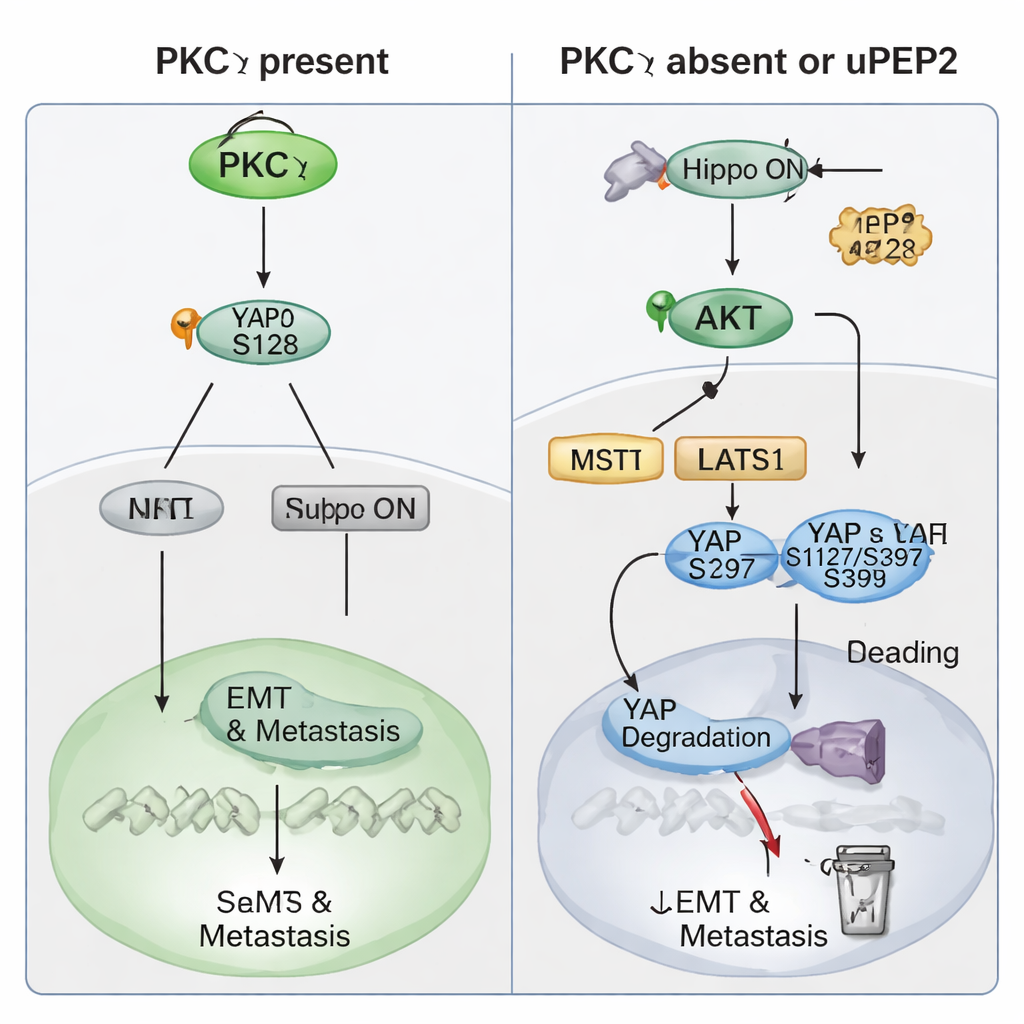
Un pequeño péptido que desactiva el interruptor del cáncer
De forma intrigante, el gen de PKCη contiene un pequeño marco de lectura abierto aguas arriba (uORF) que codifica un micropéptido llamado uPEP2. Trabajos anteriores mostraron que uPEP2 puede unirse e inhibir a PKCη y enzimas relacionadas. Aquí, el tratamiento de células TNBC con uPEP2 sintético imitó los efectos del borrado de PKCη: la migración, la invasión y el comportamiento de tipo madre disminuyeron, los marcadores de EMT se desplazaron hacia un perfil menos agresivo, y los niveles de YAP cayeron mientras aumentaban sus marcas fosforiladas de inactivación. En tumores de ratón, uPEP2 redujo PKCη y YAP en los tumores primarios, aumentó la inactivación de YAP y se asoció con menos micrometástasis en hígado y pulmones. Mecánicamente, uPEP2 promueve la degradación de PKCη, reactivando la vía Hippo y empujando a YAP hacia la retención citoplasmática y la degradación.
Qué significa esto para tratamientos futuros
Para un lector no especializado, el mensaje clave es que los investigadores han identificado a PKCη como una pieza central que ayuda a los cánceres de mama más agresivos a desprenderse, desplazarse y colonizar órganos distantes al desactivar un sistema natural de control del crecimiento y activar el “acelerador” YAP. Al eliminar PKCη o usar el pequeño péptido natural uPEP2 para degradarla, lograron restaurar el freno de seguridad Hippo, silenciar a YAP y reducir considerablemente la metástasis en modelos preclínicos. Aunque este trabajo sigue en fase experimental y se realizó en líneas celulares y ratones inmunodeficientes, destaca a PKCη y su interacción con YAP como dianas prometedoras para nuevas terapias contra el TNBC, y sugiere que fármacos tipo uPEP2 podrían algún día ayudar a prevenir o limitar la diseminación de este cáncer de difícil tratamiento.
Cita: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Palabras clave: cáncer de mama triple negativo, PKC-eta, vía Hippo-YAP, transición epitelio‑mesénquima, metástasis del cáncer