Clear Sky Science · es
Serpina3c protege frente a la enfermedad hepática esteatótica asociada a disfunción metabólica en la descendencia inducida por la exposición prenatal a prednisona
Por qué esta investigación importa para los futuros niños
Muchas mujeres necesitan prednisona durante el embarazo para controlar enfermedades autoinmunes e inflamatorias graves. Los médicos saben que puede salvar la vida de las madres, pero se comprende mucho menos cómo moldea la salud a largo plazo de sus hijos. Este estudio plantea una pregunta urgente: ¿puede el uso de prednisona durante el embarazo predisponer silenciosamente el hígado del niño a desarrollar enfermedad del hígado graso más adelante en la vida, especialmente cuando se combina con una dieta poco saludable? Y si es así, ¿hay alguna forma de revertir ese riesgo?
Un problema hepático en aumento en todo el mundo
La enfermedad hepática esteatótica asociada a disfunción metabólica, o MASLD, es ahora una de las afecciones hepáticas crónicas más comunes, afectando aproximadamente a un tercio de la población mundial y con previsiones de aumento. Incluye desde la simple acumulación de grasa en el hígado, la “hepatitis grasa” inflamatoria, hasta la fibrosis, la cirrosis e incluso el cáncer de hígado. La MASLD está fuertemente vinculada con la obesidad, la hipertensión y la diabetes tipo 2. Cada vez más, los científicos se han dado cuenta de que las semillas de esta enfermedad pueden sembrarse antes del nacimiento, cuando el feto en desarrollo está expuesto a estresores como la mala nutrición, la contaminación o los medicamentos. Esta idea —que los entornos de la primera infancia configuran el riesgo de enfermedad de por vida— se conoce como los “orígenes del desarrollo de la salud y la enfermedad”. 
La prednisona prenatal como el primer golpe
Para examinar cómo afecta la prednisona prenatal al hígado, los investigadores trataron a ratas y ratones embarazados con dosis escogidas para imitar dosis clínicas bajas usadas en humanos. Luego siguieron a la descendencia desde antes del nacimiento hasta la juventud. Por sí solos, los animales recién nacidos expuestos a prednisona en el útero eran más pequeños y ya mostraban signos de manejo anómalo de las grasas en el hígado: más gotas de grasa, triglicéridos hepáticos elevados y menor uso de las grasas como fuente de energía. A medida que crecieron, sus hígados siguieron almacenando más grasa de lo normal, incluso con una dieta habitual. Cuando más tarde se desafió a los animales con una dieta alta en grasas —el equivalente a un patrón occidental de comida rápida— las diferencias se volvieron dramáticas. La descendencia expuesta a prednisona desarrolló hígado graso más severo, inflamación y, en los machos, signos claros de fibrosis. Su control de la glucemia también empeoró, indicando un problema metabólico más amplio.
Una proteína protectora del hígado desaparece
Profundizando, el equipo empleó perfiles génicos a gran escala para buscar cambios moleculares comunes en los hígados de machos y hembras. Un gen destacó: Serpina3c, que codifica una proteína secretada perteneciente a una familia de inhibidores naturales de enzimas. En ambos sexos, la exposición prenatal a prednisona redujo de forma marcada y persistente Serpina3c en el hígado y en la circulación sanguínea, desde la vida fetal tardía hasta la edad adulta. Cuando los científicos redujeron deliberadamente Serpina3c solo en el hígado de ratones sanos, esos animales también se volvieron propensos al hígado graso y al mal manejo de la glucosa, especialmente con una dieta alta en grasas. Por el contrario, aumentar Serpina3c en los hígados de la descendencia expuesta a prednisona tras el nacimiento los rescató en gran medida: sus hígados almacenaron menos grasa, gestionaron mejor la glucosa y mostraron menos inflamación y fibrosis.
Cómo la prednisona reprograma los interruptores de control del hígado
Los investigadores preguntaron luego cómo la prednisona prenatal suprime Serpina3c. Hallaron que la forma activa de la prednisona, la prednisolona, sobreactiva el receptor de glucocorticoides —una proteína detectora de fármacos presente en las células hepáticas. Este receptor se asocia con otra proteína, HDAC3, que compacta el empaquetamiento del ADN al eliminar pequeñas etiquetas “acetilo” de las histonas. Tanto en hígados animales como en células hepáticas en cultivo, la prednisolona aumentó la actividad del receptor de glucocorticoides y de HDAC3 directamente en el gen Serpina3c, eliminando marcas de acetilación en un sitio clave llamado H3K27. Con estas marcas eliminadas, la actividad del gen descendió y los niveles de proteína Serpina3c cayeron. Bloquear el receptor o HDAC3, o inhibir la desacetilación, restauró estas marcas de acetilo, elevó Serpina3c y mejoró el manejo de grasas y glucosa en células hepáticas.
Una reacción en cadena dañina dentro del hígado
La baja de Serpina3c desencadenó una segunda cascada dañina. En condiciones normales, Serpina3c ayuda a contener enzimas como la quimasa que generan la hormona angiotensina II directamente dentro de los tejidos. Cuando Serpina3c era escasa, los niveles y la actividad de la quimasa aumentaron, produciendo más angiotensina II en el hígado y sobreactivando su receptor, AT1R, en las células hepáticas. Este aumento local de la hormona se sabe que impulsa el estrés oxidativo, la resistencia a la insulina, la acumulación de grasa, la inflamación y la formación de cicatrices. Tanto en animales expuestos a prednisona como en ratones con reducción específica de Serpina3c en el hígado, la vía quimasa–angiotensina II–AT1R se activó, y los genes clave que normalmente favorecen la quema de grasas y la captación de glucosa quedaron suprimidos. Restaurar Serpina3c después del nacimiento silenció esta vía y reavivó un metabolismo más saludable. 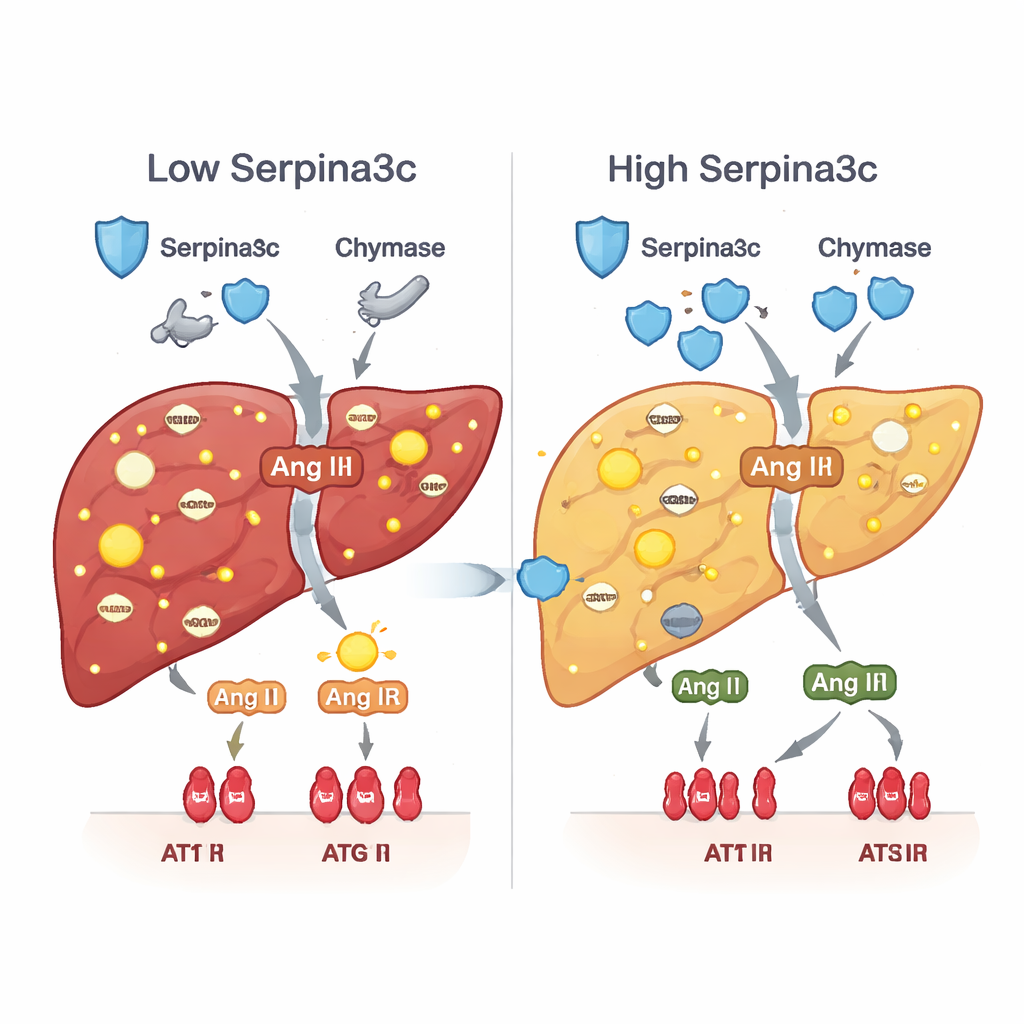
Qué significa esto para pacientes y familias
Para quienes no son especialistas, el mensaje principal es que los fármacos tomados durante el embarazo pueden dejar una huella molecular en el hígado en desarrollo que perdura hasta la edad adulta. En este estudio, la prednisona actuó como un “primer golpe”, reduciendo una proteína protectora (Serpina3c) mediante cambios epigenéticos —marcas químicas en las proteínas que empaquetan el ADN— de modo que un “segundo golpe” posterior, como una dieta alta en grasas, desencadenó con mayor facilidad la enfermedad del hígado graso. La cara alentadora es que este riesgo no era irreversible: volver a aumentar Serpina3c en el hígado tras el nacimiento redujo de forma notable el daño hepático. Aunque estos resultados proceden de roedores, plantean preguntas importantes sobre cómo monitorizar y apoyar a los niños cuyas madres necesitaron prednisona en el embarazo, y señalan a Serpina3c y al sistema quimasa–angiotensina II como dianas prometedoras para prevenir o tratar la enfermedad del hígado graso que se inicia antes del nacimiento.
Cita: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
Palabras clave: prednisona prenatal, enfermedad del hígado graso, epigenética, Serpina3c, orígenes del desarrollo