Clear Sky Science · es
Osteoartritis: patogenia molecular y opciones terapéuticas potenciales
Cuando el dolor articular cotidiano se convierte en una historia de todo el cuerpo
Las rodillas doloridas o los dedos rígidos suelen descartarse como una parte inevitable del envejecimiento. Sin embargo, la osteoartritis—la enfermedad articular más común en el mundo—no es solo “desgaste”. Este artículo de revisión levanta el telón sobre lo que realmente ocurre dentro de las articulaciones dolorosas, desde neuronas del dolor que disparan mal hasta maquinaria celular sobrecargada, y explora una nueva generación de tratamientos que van mucho más allá de los analgésicos simples.
Una enfermedad común con un alto coste personal
La osteoartritis afecta a casi el 8% de la población mundial, con cientos de millones de personas que conviven con dolor crónico y movilidad reducida. La enfermedad aparece con mayor frecuencia en mujeres, en personas mayores de 55 años y en quienes tienen sobrepeso o realizan trabajos o deportes que someten las articulaciones a estrés repetido y fuerte. Los cuidados actuales—ejercicio, pérdida de peso, ortesis, antiinflamatorios, inyecciones articulares y, en casos graves, reemplazo articular—pueden aliviar los síntomas, pero rara vez detienen el empeoramiento progresivo de la enfermedad. Esta brecha entre la necesidad y los tratamientos disponibles ha impulsado a los científicos a indagar mucho más sobre cómo comienza la osteoartritis y por qué duele tanto.
Por qué duele la articulación: cables, químicos y señales
El dolor en la osteoartritis no se explica solo con radiografías: algunas personas con daño moderado sienten mucho dolor, mientras que otras con cambios severos reportan poco malestar. El artículo sigue el rastro del dolor desde la articulación de la rodilla, a través de la médula espinal, hasta el cerebro. Las terminaciones nerviosas en la articulación—especialmente las fibras finas Aδ y C—están bañadas en un cóctel de químicos inflamatorios, incluidas interleucinas y factor de necrosis tumoral, así como factor de crecimiento nervioso. Estas sustancias activan canales especiales en las terminaciones nerviosas que permiten el paso de sodio y calcio, haciendo que los nervios se disparen con más facilidad y con mayor frecuencia. Con el tiempo, las vías del dolor en la médula espinal y el cerebro pueden volverse hiper‑responsivas, de modo que un movimiento normal o un frío leve se perciben como sensación intensa y ardiente.
La carga de trabajo oculta dentro de las células de la articulación
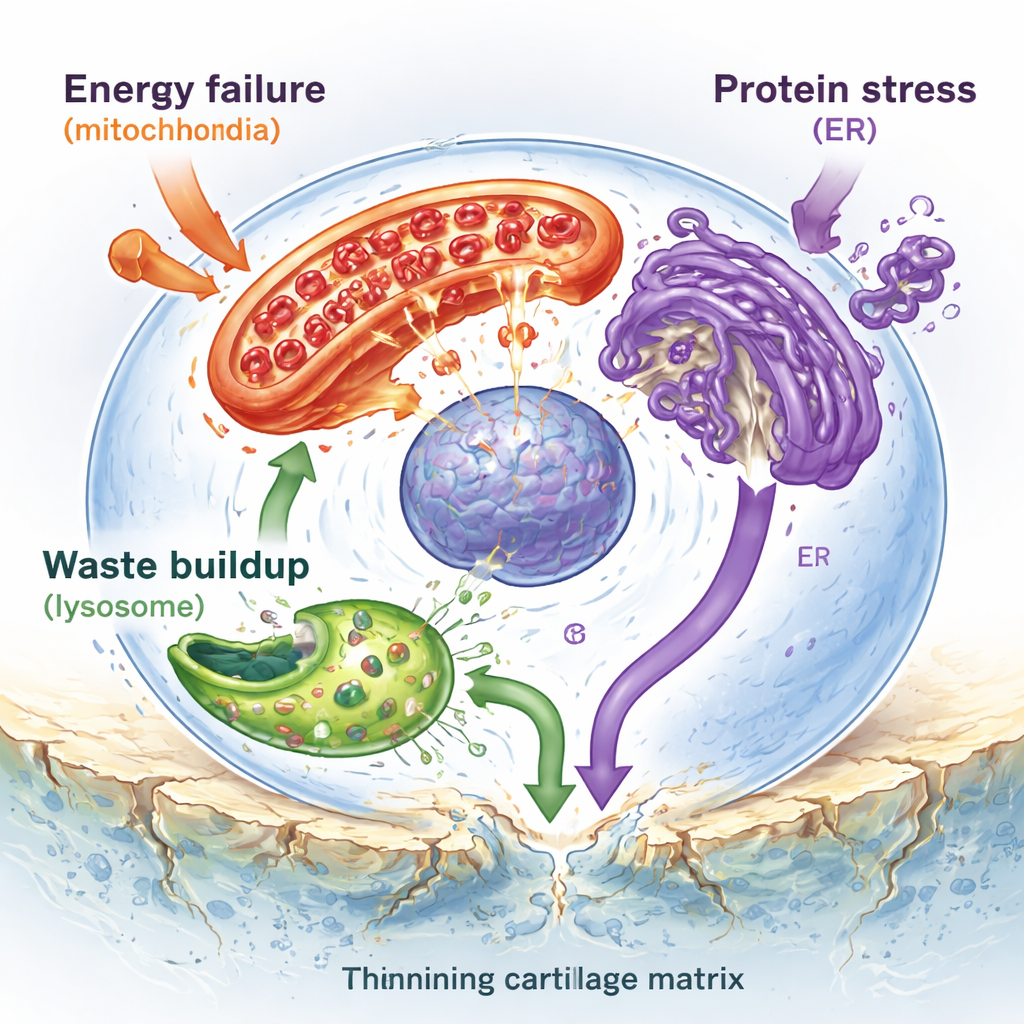
En lo profundo del cartílago, las únicas células residentes—los condrocitos—intentan mantener una matriz lisa y elástica que permita el deslizamiento de los huesos. Los autores muestran que estas células están asediadas en varios frentes. Las mitocondrias, las pequeñas centrales energéticas de la célula, se dañan y funcionan menos eficientemente, produciendo poca energía y demasiadas moléculas reactivas de oxígeno que lesionan el ADN y las proteínas. Los lisosomas, los centros de reciclaje celular, se sobrecargan por cristales minerales duros, debilitando sus membranas de modo que enzimas destructivas se filtran al interior y desencadenan la muerte celular. El retículo endoplásmico, un laberinto membranoso donde se pliegan las proteínas nuevas, se atasca con moléculas mal plegadas, provocando una respuesta crónica de “estrés” que finalmente empuja a las células hacia la autodestrucción. En conjunto, estos orgánulos estresados alimentan la inflamación y aceleran la pérdida y calcificación del cartílago.
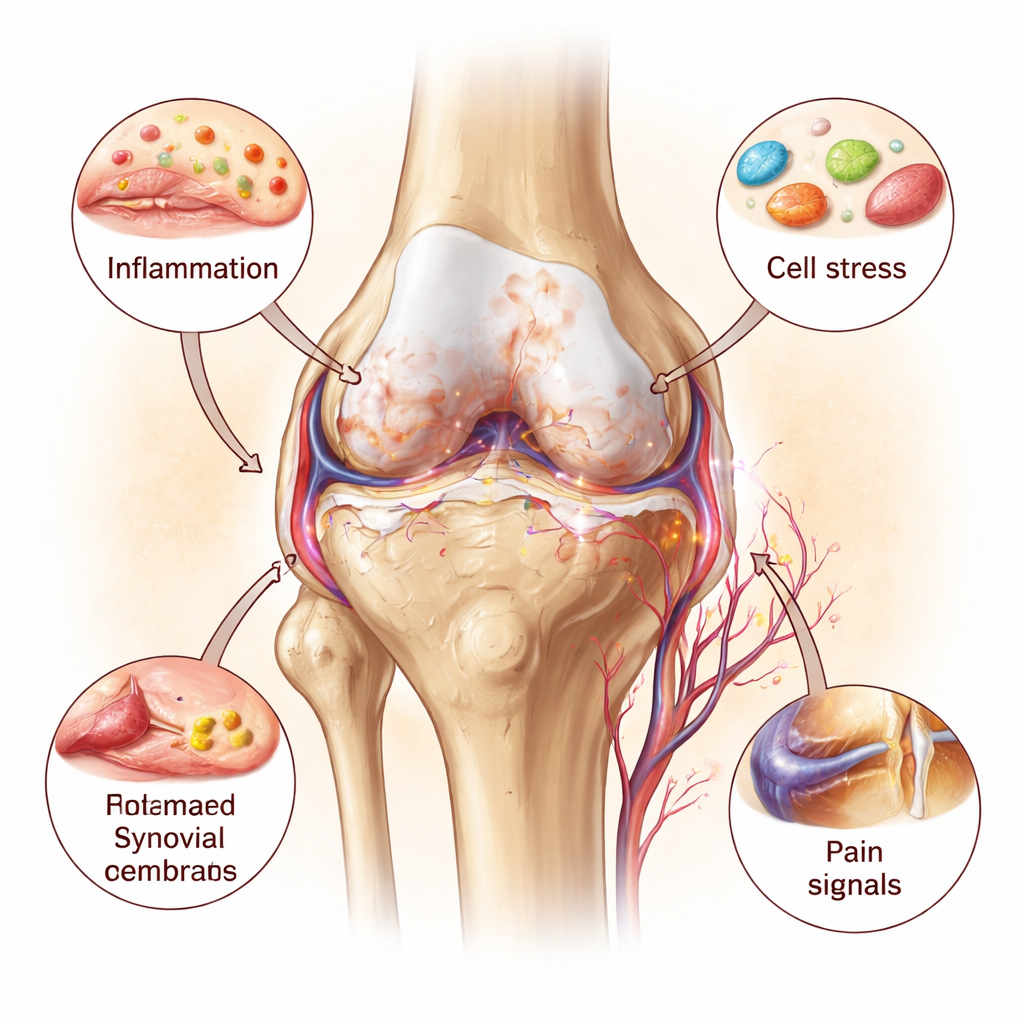
Inflamación: combustible para el fuego
Las moléculas mensajeras inflamatorias actúan como altavoces de este proceso. Tres en particular—interleucina‑1, interleucina‑6 y el factor de necrosis tumoral‑alfa—forman un círculo vicioso con el daño a los orgánulos. Impulsan a los condrocitos a producir enzimas que degradan el cartílago y fomentan el crecimiento óseo anómalo bajo la superficie articular. Al mismo tiempo, mitocondrias lesionadas y lisosomas con fugas liberan sus propias señales de alarma, que activan aún más los sensores inmunitarios dentro de la articulación. Vasos sanguíneos y fibras nerviosas crecen en áreas de cartílago que normalmente están silenciosas y sin nervios, aumentando la sensibilidad al dolor. Esta visión de la articulación en su conjunto pinta la osteoartritis como una enfermedad inflamatoria de progresión lenta pero auto‑reforzada, no como un simple deshilachamiento mecánico pasivo del cartílago.
Nuevas ideas terapéuticas: de los canales iónicos a las centrales celulares
Armados con este mapa mecanicista, los investigadores están probando nuevos fármacos y sistemas de administración. En el lado del dolor, medicamentos experimentales bloquean o desensibilizan suavemente canales nerviosos como TRPV1 (el receptor de la capsaicina), TRPA1, TRPM3/8 y canales de sodio específicos (Nav1.7 y Nav1.8), o neutralizan el factor de crecimiento nervioso para evitar que los nervios se vuelvan hiper‑sensibles. En el lado modificador de la enfermedad, anticuerpos dirigidos intentan reducir citocinas inflamatorias clave, mientras pequeñas moléculas y agentes “senolíticos” buscan restaurar un comportamiento celular más saludable. Una frontera especialmente prometedora es la terapia dirigida a orgánulos: compuestos que estimulan la limpieza mitocondrial (mitofagia), estabilizan la acidez y las membranas lisosomales o alivian el estrés del retículo endoplásmico. Nanopartículas sofisticadas, liposomas y exosomas diseñados se están desarrollando para dirigirse a los condrocitos e incluso a orgánulos específicos, entregando fármacos con precisión donde se necesitan.
Qué significa esto para las personas que viven con osteoartritis
El artículo concluye que la osteoartritis debe verse y tratarse como un trastorno biológico complejo que implica metabolismo celular desordenado, inflamación crónica de bajo grado y cableado del dolor maladaptativo. Aunque muchos de los fármacos y sistemas de administración propuestos aún están en pruebas de laboratorio o en modelos animales tempranos, apuntan a un futuro en el que el tratamiento será tanto multimodal como personalizado: aliviando el dolor al calmar nervios hiperactivos, y al mismo tiempo protegiendo o rejuveneciendo las propias células de la articulación y su maquinaria interna. Para los pacientes, esto podría significar eventualmente terapias que no solo hagan el movimiento menos doloroso, sino que también ralenticen o incluso reviertan el daño estructural que hoy en día a menudo se considera inevitable.
Cita: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
Palabras clave: osteoartritis, dolor articular, cartílago, inflamación, mitocondrias