Clear Sky Science · es
Micronúcleos: orígenes, ensayos, mecanismos, enfermedades y tratamientos
Burbujas ocultas dentro de nuestras células
En lo profundo de nuestras células, pequeñas “burbujas satélite” de ADN llamadas micronúcleos resultan ser mucho más que rarezas al microscopio. Antes se pensaba que eran restos inofensivos de la división celular, pero estas pequeñas esferas llenas de ADN están ahora asociadas al desarrollo del cáncer, a reacciones inmunitarias e incluso a posibles tratamientos nuevos. Comprender qué crea los micronúcleos, qué les sucede y cómo afectan a nuestros genes está cambiando la manera en que los científicos consideran el daño genómico y las enfermedades.
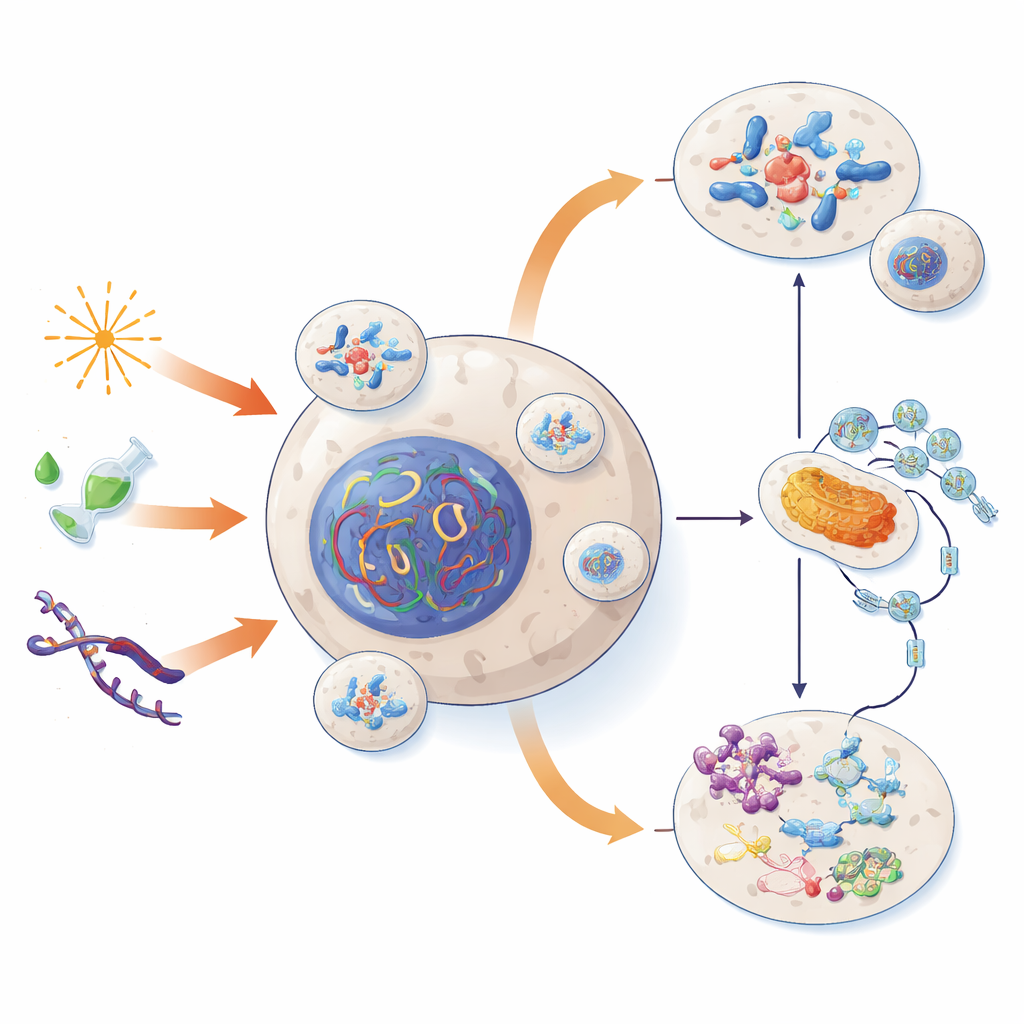
Cómo nacen las pequeñas burbujas de ADN
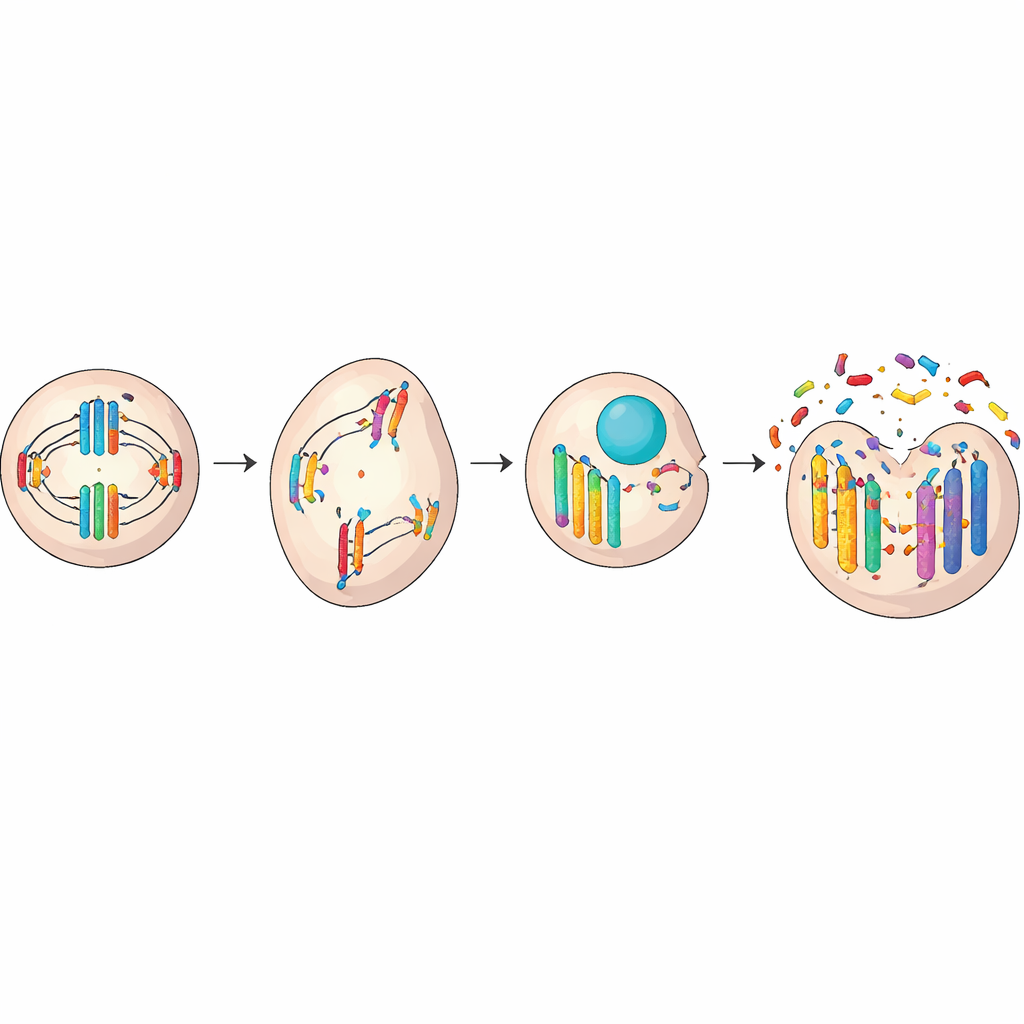
Los micronúcleos suelen aparecer cuando algo falla durante la división celular. Normalmente, los cromosomas se alinean y son repartidos de forma equitativa entre las dos nuevas células. Pero si la maquinaria de la división es defectuosa o el ADN está dañado, un cromosoma entero o un fragmento puede quedarse rezagado y quedar aislado en su propia cubierta fuera del núcleo principal. Daños por radiación o químicos tóxicos, extremos de cromosomas desgastados (telómeros) o errores en los “ganchos” proteicos que separan los cromosomas pueden desencadenar este mal reparto. En algunos casos, el núcleo incluso emite brotes de ADN durante las fases de reposo entre divisiones, formando micronúcleos sin que se produzca una división completa de la célula.
Qué ocurre con las islas de ADN perdidas
Una vez formados, los micronúcleos pueden seguir varias trayectorias, cada una con distintas consecuencias para la célula. Algunos son reabsorbidos por el núcleo principal en divisiones posteriores, reintegrando silenciosamente su ADN —a veces con cambios sutiles y duraderos en la actividad génica. Otros persisten como cuerpos separados y se transmiten solo a una de las dos células hijas, incrementando la diversidad genética entre las células de un tejido. Algunos micronúcleos son digeridos mediante procesos celulares de “autolimpieza”, mientras que otros son expulsados físicamente de la célula por completo. Pero quizá el destino más dramático es la rotura: su frágil envoltura exterior a menudo se rompe, derramando ADN dañado en el interior celular y exponiéndolo a fuerzas destructivas.
De cromosomas hechos añicos al caos
Cuando un micronúcleo se rompe o su ADN se copia de forma incorrecta, el cromosoma atrapado en su interior puede hacerse añicos en docenas o cientos de fragmentos. Esos fragmentos son luego cosidos de nuevo de una manera precipitada y propensa a errores, un fenómeno conocido como cromotrisis. En lugar de una acumulación gradual de pequeñas mutaciones a lo largo de años, una célula puede sufrir una alteración genética masiva y localizada en una sola crisis. Genes importantes pueden perderse, mezclarse o copiarse muchas veces. Pueden formarse piezas adicionales de ADN en forma circular que llevan múltiples genes que impulsan el crecimiento, otorgando a la célula nuevas ventajas potentes. Si este cambio beneficia o perjudica a la célula depende de qué genes se vean afectados, pero en muchos cánceres estos eventos favorecen el crecimiento tumoral, la diseminación o la resistencia a los tratamientos.
Señales que despiertan al sistema inmune
El ADN filtrado de micronúcleos rotos también actúa como una alarma. Nuestras células suelen mantener su ADN protegido en el núcleo, por lo que el ADN libre en el fluido circundante resulta sospechoso, parecido al de un virus o una bacteria. Una proteína sensor llamada cGAS puede unirse a ese ADN suelto y activar a una pareja llamada STING, desencadenando respuestas inflamatorias y antivirales. En situaciones saludables, esto ayuda a eliminar células dañadas o peligrosas. Pero en muchos cánceres avanzados, las células tumorales encuentran maneras de atenuar o reconfigurar este sistema de alarma. En lugar de provocar un ataque inmunitario, señales crónicas de bajo nivel procedentes de micronúcleos frecuentes pueden ayudar a las células cancerosas a volverse más invasivas y a evadir mejor las defensas del organismo.
Medir y aprovechar los micronúcleos
Porque los micronúcleos marcan visiblemente el daño del ADN, se han convertido en herramientas útiles en medicina y salud pública. Pruebas sencillas de tinción en células sanguíneas, células de la mejilla o glóbulos rojos pueden revelar cuánto estrés genético ha sufrido una persona por contaminación, exposiciones laborales, tabaquismo o enfermedad. Personas con ciertos cánceres, insuficiencia cardíaca, enfermedad renal o trastornos hereditarios de reparación del ADN suelen mostrar recuentos elevados de micronúcleos. Los investigadores están ahora utilizando métodos de imagen y clasificación de alto rendimiento para purificar micronúcleos, catalogar sus contenidos proteicos y de ADN, y mapear cómo distintos tipos de estrés dejan huellas “epigenéticas” y estructurales específicas en su interior.
Nuevos riesgos y nuevas oportunidades
Los micronúcleos están en una encrucijada entre daño y defensa: pueden tanto impulsar reordenamientos genómicos peligrosos como activar la protección inmune. Algunas terapias experimentales contra el cáncer aumentan deliberadamente la mala segregación cromosómica o bloquean vías específicas de reparación del ADN para forzar a las células tumorales a formar micronúcleos, con la esperanza de provocar fuertes ataques inmunitarios o empujar a las células inestables más allá de sus límites. Sin embargo, esta estrategia camina sobre una línea fina, ya que los mismos procesos también pueden generar clones más agresivos y resistentes al tratamiento. Los autores concluyen que los micronúcleos no son ni puramente dañinos ni puramente beneficiosos. En cambio, son indicadores y agentes de cambio poderosos cuyo impacto global depende del contexto. Para convertir con seguridad a los micronúcleos en aliados contra la enfermedad, los científicos necesitarán mejores formas de medir, controlar y moldear selectivamente su formación y destino dentro del organismo.
Cita: Duan, H., Peng, X., Qin, S. et al. Micronuclei: origins, assays, mechanisms, diseases and treatments. Sig Transduct Target Ther 11, 114 (2026). https://doi.org/10.1038/s41392-025-02538-8
Palabras clave: micronúcleos, inestabilidad genómica, cromotrisis, cGAS-STING, biomarcadores de cáncer