Clear Sky Science · es
Linfocitos CD4+ citotóxicos: origen, funciones biológicas, enfermedades y dianas terapéuticas
Cuando las células colaboradoras se convierten en asesinas
El sistema inmunitario suele describirse con roles sencillos: unas células detectan el peligro y otras realizan la lucha. Este artículo se centra en un grupo sorprendente que difumina esa línea: los linfocitos CD4 citotóxicos. Durante mucho tiempo conocidos principalmente como células “colaboradoras” que coordinan la defensa, ciertos linfocitos CD4 pueden convertirse en asesinos armados. Comprender cómo surgen estas células camaleónicas, qué hacen y cómo contribuyen a enfermedades como el cáncer, infecciones virales, trastornos autoinmunes y enfermedades cardíacas podría abrir nuevas vías para potenciar la inmunidad y calmar la inflamación dañina. 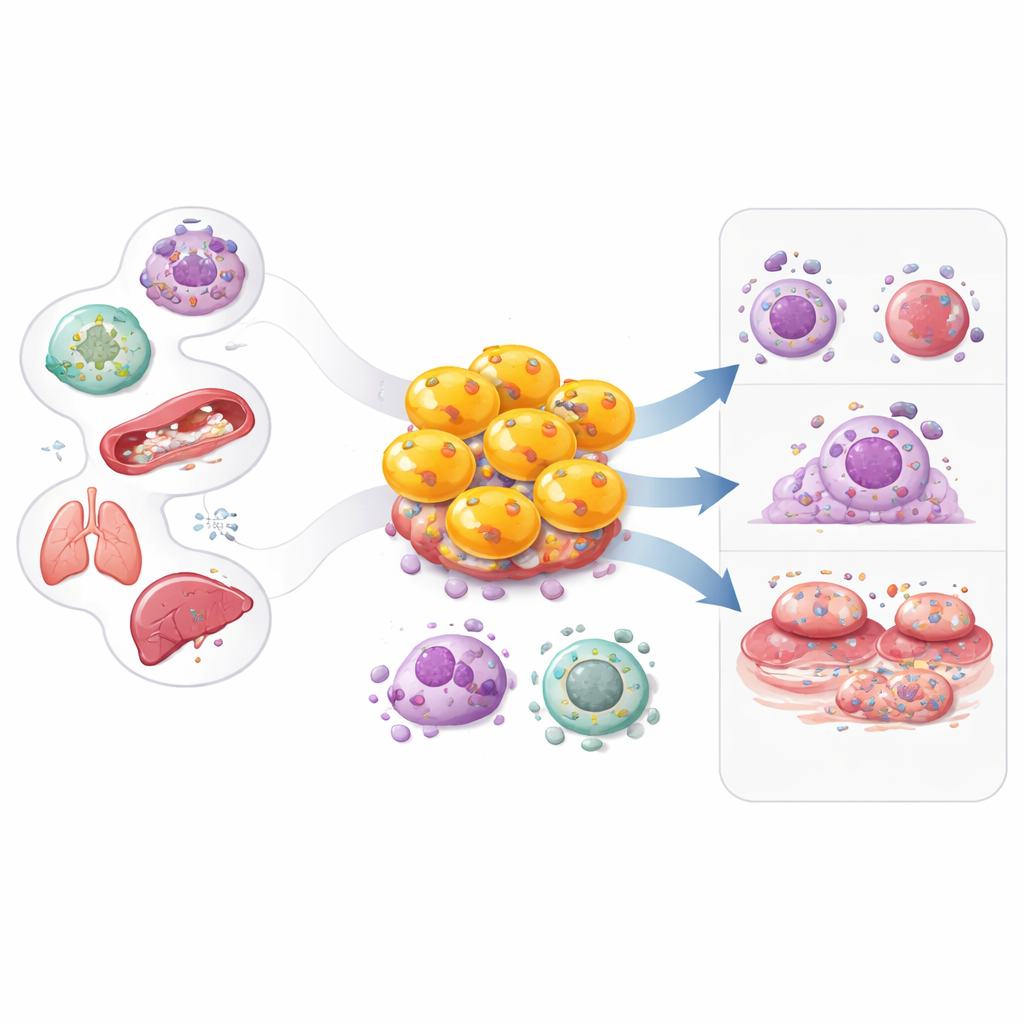
Cómo emergió un defensor flexible
Los trabajos iniciales a finales de los años setenta y en los ochenta mostraron que una fracción de los linfocitos CD4 podía eliminar directamente a otras células que presentaban las señales inmunitarias adecuadas, de forma similar a los clásicos linfocitos CD8 “asesinos”. Al principio, muchos científicos descartaron estos hallazgos como artefactos de cultivo. En las décadas siguientes, modelos animales de gripe y estudios en personas con artritis reumatoide, enfermedad cardíaca, infecciones virales crónicas y cáncer confirmaron que los CD4 citotóxicos existen y tienen importancia clínica. Herramientas modernas, como citometría de flujo y secuenciación de ARN unicelular, han cartografiado su diversidad, revelando que estas células se expanden en infecciones crónicas, tumores, envejecimiento y diversas enfermedades inflamatorias, donde pueden persistir durante largos periodos.
De dónde proceden estos ayudantes asesinos
La revisión explica que los linfocitos CD4 citotóxicos probablemente surgen por dos vías principales. Una idea es que se parecen en parte a las células NK porque comparten muchos de los mismos receptores de superficie y moléculas citotóxicas, lo que sugiere una vía de desarrollo relacionada. Sin embargo, la evidencia acumulada favorece otra visión: la mayoría de estas células comienzan como linfocitos CD4 colaboradores ordinarios—especialmente células con perfil Th1—que, bajo exposición crónica al antígeno y señales inflamatorias intensas, se “reforman” hacia un estado citotóxico y terminalmente diferenciado. Este cambio está controlado por una red de señales externas (como las interleucinas 2, 7 y 15) y conmutadores internos (incluyendo Runx3, T-bet, Eomes, Blimp-1 y Hobit) que en conjunto activan genes de perforina, granzimas y ligandos inductores de muerte.
Cómo matan y moldean la inflamación
Funcionalmente, los linfocitos CD4 citotóxicos actúan por dos rutas principales de ataque. En la vía de gránulos, forman un contacto estrecho con la célula diana y liberan paquetes que contienen perforina y granzimas, que perforan la membrana y desencadenan la muerte programada desde el interior. En la vía de ligandos de muerte, muestran en su superficie moléculas como Fas ligand y TRAIL, que se unen a receptores coincidentes en la célula diana para activar un programa suicida interno. Más allá de la citotoxicidad directa, estas células secretan mediadores inflamatorios como interferón gamma, factor de necrosis tumoral y factores de crecimiento que reclutan y activan otras células inmunitarias, remodelan vasos sanguíneos y alteran el comportamiento del tejido local. A diferencia de las auxiliares clásicas, suelen ser resistentes a los “frenos” habituales como las células T reguladoras y son menos proclives a la apoptosis, lo que les permite acumularse en enfermedades crónicas. 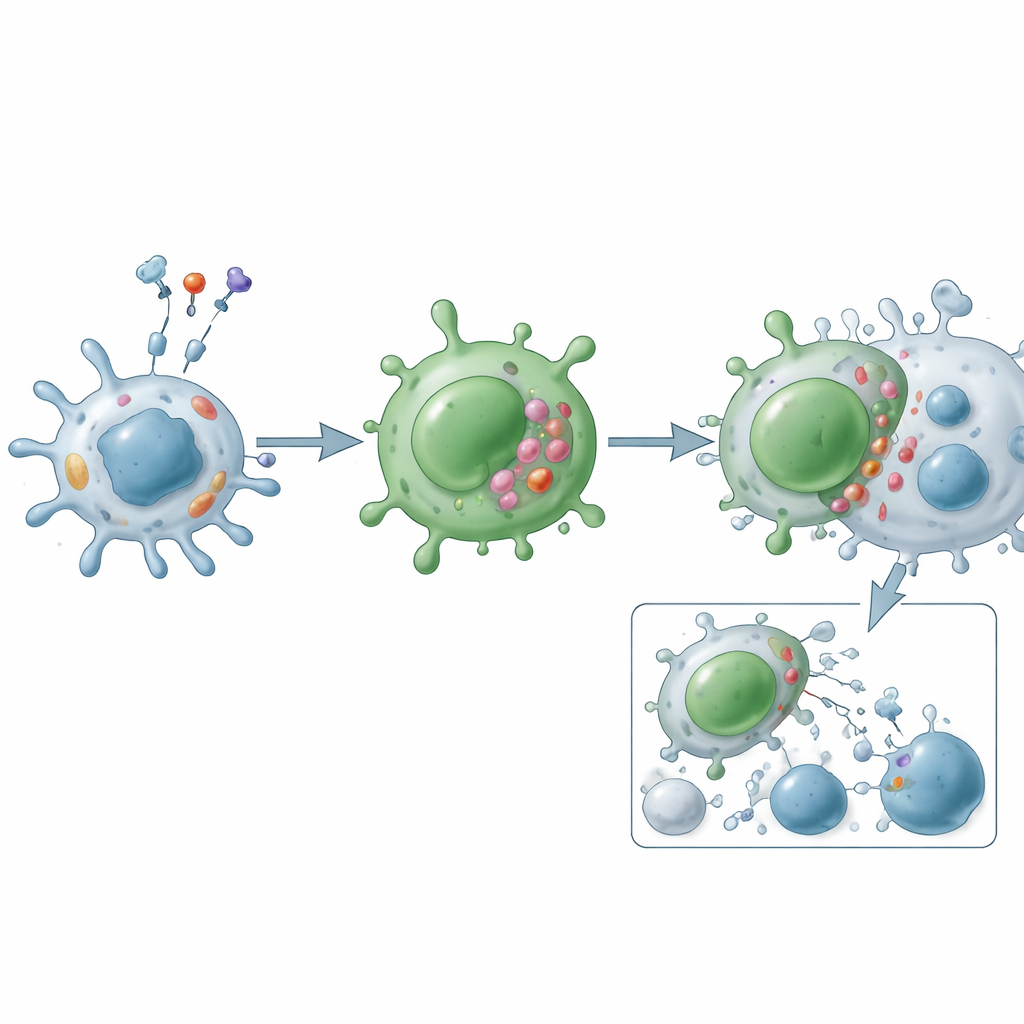
Aliadas en infección y cáncer, enemigas en autoinmunidad y enfermedad cardíaca
Este comportamiento de doble filo aparece en muchas condiciones. En hepatitis B crónica, VIH y COVID-19, los linfocitos CD4 citotóxicos ayudan a controlar virus cuando los CD8 están agotados, y su presencia puede asociarse con mejor control o recuperación. En tumores sólidos y neoplasias hematológicas, pueden reconocer directamente células tumorales que exhiben las señales inmunitarias o de estrés adecuadas y mejorar las respuestas a inmunoterapias como inhibidores de puntos de control y tratamientos CAR-T. Al mismo tiempo, esos mismos mecanismos pueden causar daño: en lupus, artritis reumatoide, enfermedad inflamatoria intestinal, enfermedad de las arterias coronarias, fibrilación auricular, arteritis de células gigantes y rechazo de trasplante, la expansión de linfocitos CD4 citotóxicos infiltra tejidos, daña vasos u órganos y amplifica inflamación persistente, a menudo correlacionada con peor pronóstico.
Convertir una herramienta peligrosa en terapia
Puesto que los linfocitos CD4 citotóxicos pueden ser protectores o destructivos, el artículo destaca estrategias terapéuticas emergentes que buscan afinar, más que eliminar, esta población. Una aproximación consiste en atenuar su actividad dañina usando inhibidores selectivos que apunten a receptores coestimuladores (como OX40 o 4-1BB), citocinas inflamatorias, canales iónicos o vías de supervivencia. Otra es aprovechar su poder citotóxico en terapias celulares adoptivas, incluyendo linfocitos editados genéticamente y CAR-T, donde las células CD4 citotóxicas a menudo muestran mejor persistencia que productos compuestos solo por CD8. Una tercera estrategia propone redirigir linfocitos CD4 asesinos de larga vida y específicos de virus hacia tumores mediante vacunas o péptidos derivados de patógenos presentados por células cancerosas. En conjunto, estas líneas de trabajo sitúan a los linfocitos CD4 citotóxicos no solo como una curiosidad biológica, sino como una palanca central para tratamientos futuros que permitan potenciar con mayor precisión la defensa contra infecciones y cáncer a la vez que reducen la inflamación que daña los tejidos.
Una nueva palanca para futuras inmunoterapias
Para el público general, el mensaje clave es que los linfocitos CD4 “colaboradores” son mucho más versátiles de lo que se pensaba: algunos pueden transformarse en asesinos completamente armados que nos protegen de infecciones persistentes y del cáncer, pero también contribuyen a la autoinmunidad, daño vascular y rechazo de trasplantes. La revisión sostiene que aprender a rastrear estas células, predecir cuándo ayudarán o dañarán y ajustar su comportamiento con fármacos o terapias diseñadas podría redefinir el tratamiento de una amplia gama de enfermedades crónicas—desde hepatitis y VIH hasta artritis, colitis, enfermedad cardíaca y leucemia. En lugar de simplemente subir o bajar la actividad inmunitaria, las terapias del futuro podrían trabajar orientando tipos celulares poderosos como los linfocitos CD4 citotóxicos hacia objetivos beneficiosos y alejándolos de nuestros propios tejidos.
Cita: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Palabras clave: linfocitos CD4 citotóxicos, plasticidad de las células inmunitarias, inflamación crónica, inmunoterapia contra el cáncer, enfermedad autoinmune