Clear Sky Science · es
IFFO1 inhibe el cáncer de mama coordinando la fisión mitocondrial y la síntesis de ácidos grasos mediante el eje LaminA/C-PGC1α
Por qué importa esta investigación
El cáncer de mama sigue siendo una de las principales causas de muerte por cáncer en mujeres, en gran parte porque algunos tumores continúan creciendo, diseminándose y eludiendo los tratamientos disponibles. Este estudio descubre un “freno” celular hasta ahora poco valorado, llamado IFFO1, que ralentiza el cáncer de mama al domesticar dos motores centrales del crecimiento tumoral: las fábricas de energía de la célula, las mitocondrias, y su capacidad para fabricar y almacenar grasas. Comprender este freno ofrece un ángulo nuevo para terapias que podrían funcionar en múltiples subtipos de cáncer de mama.
Un guardián oculto dentro de las células mamarias
Los investigadores empezaron examinando muestras de 30 mujeres con cáncer de mama, así como grandes bases de datos públicas sobre cáncer. Encontraron que los niveles de la proteína IFFO1 eran sistemáticamente más bajos en el tejido tumoral que en el tejido mamario normal adyacente. Cuanto más avanzado era el estadio del cáncer, menos IFFO1 había, y las pacientes cuyos tumores presentaban más IFFO1 tendían a vivir más tiempo. En células de cáncer de mama cultivadas, forzar la sobreexpresión de IFFO1 redujo drásticamente su capacidad para crecer, dividirse y migrar —comportamientos necesarios para que los tumores se expandan y metastaticen. IFFO1 también atenuó un programa celular conocido como transición epitelial-mesenquimal, que facilita que las células cancerosas se desprendan e invadan otros tejidos.
Calmando fábricas de energía hiperactivas
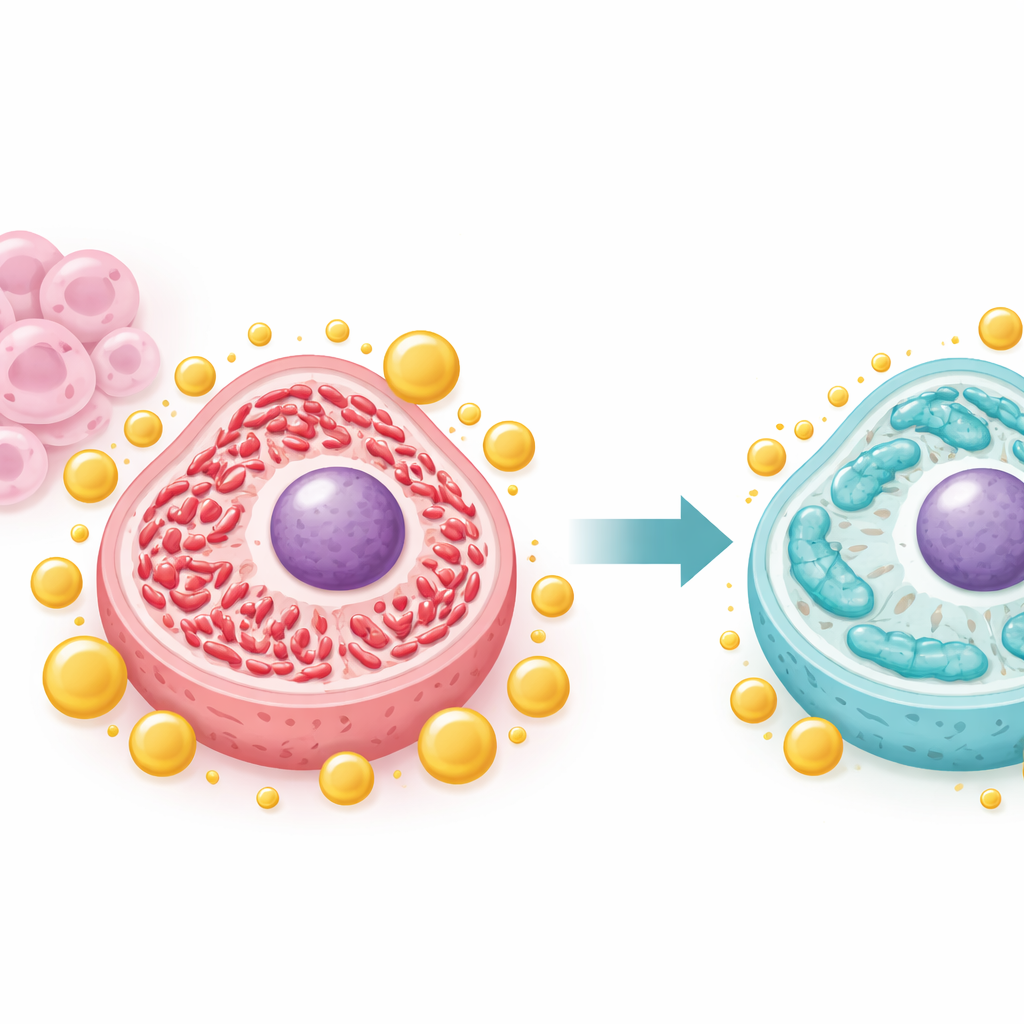
Las células cancerosas con frecuencia remodelan sus mitocondrias, las pequeñas plantas de energía en el interior celular, para alimentar un crecimiento rápido. El equipo mostró que IFFO1 desplaza este equilibrio lejos de un estado altamente fragmentado de “fisión” hacia un estado más alargado de “fusión”, asociado en general con mitocondrias más sanas y estables. Cuando IFFO1 era abundante, proteínas clave de la fisión como Drp1 y Fis1 disminuían, mientras que las proteínas de fusión aumentaban. La microscopía reveló que las mitocondrias se volvían más largas y menos fragmentadas, y las medidas de ADN mitocondrial y producción energética caían desde los niveles anormalmente altos observados en células agresivas. Estos cambios sugieren que IFFO1 evita que las mitocondrias entren en una configuración hiperactiva que sostiene el crecimiento tumoral descontrolado.
Cortando la línea de suministro de grasas
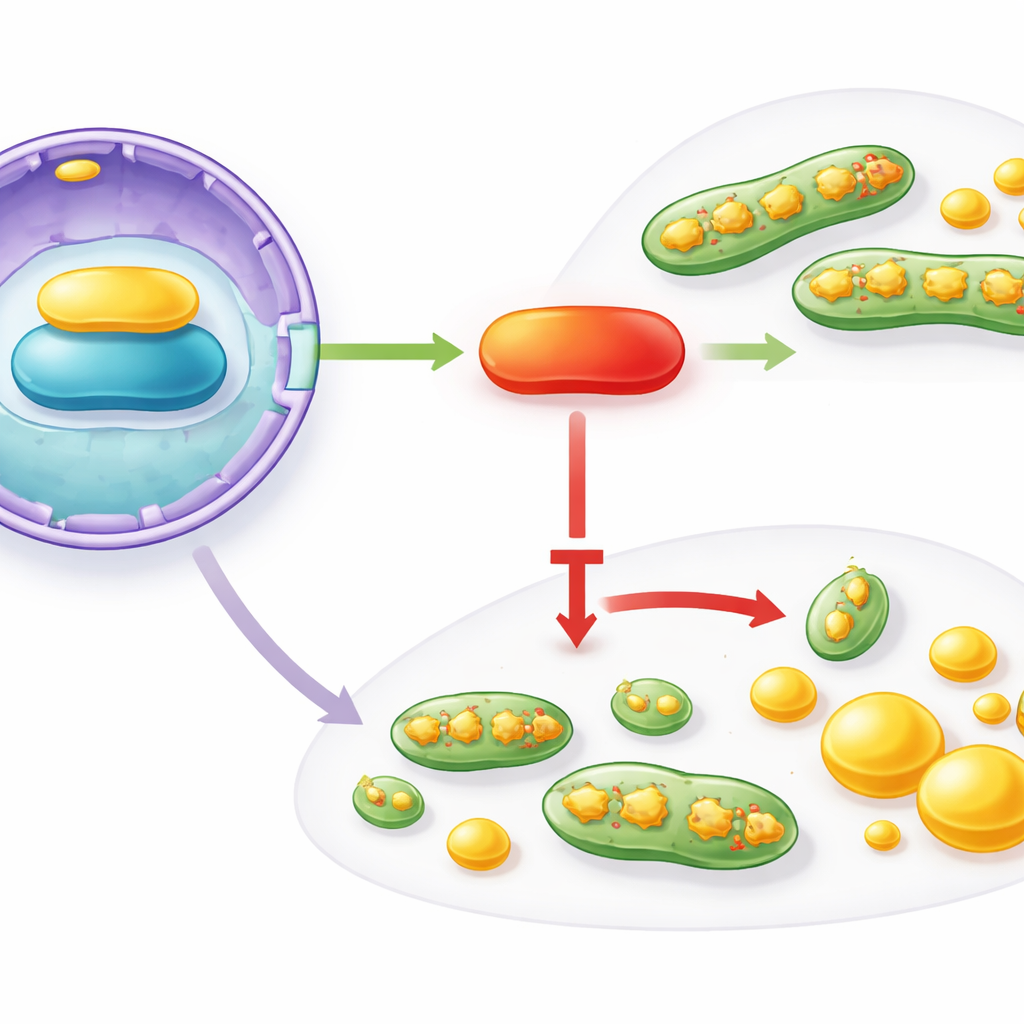
Los tumores de rápido crecimiento no solo necesitan energía; también requieren un aporte constante de grasas para construir nuevas membranas y moléculas de señalización. El estudio encontró que IFFO1 también reprime este acelerador metabólico. En células con sobreexpresión de IFFO1, proteínas centrales de la síntesis lipídica —incluyendo FASN, SREBP‑1, SCD1 y otras— se redujeron. Pruebas enzimáticas confirmaron una menor actividad sintetizadora de grasas, y ensayos químicos mostraron descensos en ácidos grasos libres, triglicéridos y colesterol. Tintes de imagen que resaltan las reservas lipídicas revelaron menos gotas lipídicas y menos grasa neutra en el interior de las células cancerosas. Por el contrario, aumentar la proteína de fisión Drp1 produjo el efecto opuesto, incrementando la producción de grasas, mientras que silenciar Drp1 la contuvo —lo que apoya un vínculo directo entre la forma mitocondrial y el suministro de lípidos en el cáncer.
Una cadena de señalización desde el núcleo hasta las mitocondrias
¿Cómo orquesta IFFO1 estos cambios tan amplios? Los autores trazaron una cadena de interacciones que comienza en el núcleo celular y termina en las mitocondrias y la maquinaria lipogénica. IFFO1 se une físicamente a una proteína estructural de la envoltura nuclear llamada Lamin A/C, y aumenta sus niveles. Lamin A/C, a su vez, favorece la actividad de PGC1α, un regulador maestro que supervisa la salud mitocondrial y el metabolismo. En tejidos y células de cáncer de mama, tanto Lamin A/C como PGC1α se encontraron reducidos, reflejando la pérdida de IFFO1. Cuando los científicos aumentaron artificialmente IFFO1, Lamin A/C y PGC1α se elevaron, la fisión mitocondrial disminuyó y la síntesis de grasas se redujo. La reducción de Lamin A/C eliminó estos beneficios, pero la restauración de PGC1α los recuperó, identificando un eje funcional IFFO1 → Lamin A/C → PGC1α que frena los cambios mitocondriales y lipogénicos que promueven el tumor.
Probando el freno en animales vivos
Para comprobar si estos efectos celulares se traducen en tumores reales, el equipo implantó en ratones células humanas de cáncer de mama con o sin sobreexpresión de IFFO1. Los tumores con IFFO1 potenciado crecieron más despacio, pesaron menos al final del experimento y mostraron menos signos de acumulación lipídica. En un modelo separado, en el que las células cancerosas se inyectaron en el torrente sanguíneo para originar metástasis pulmonares, las células que sobreproducían IFFO1 formaron muchas menos nódulos tumorales en los pulmones. Los análisis tisulares de estos ratones replicaron los hallazgos de cultivo celular: más Lamin A/C y PGC1α, menos fisión mitocondrial y menor síntesis de grasas.
Qué significa esto para futuros tratamientos
En conjunto, el trabajo presenta a IFFO1 como un supresor tumoral multinivel que conecta el armazón estructural de la célula, sus fábricas de energía y su maquinaria para fabricar grasas. Al estabilizar Lamin A/C y aumentar PGC1α, IFFO1 evita que las mitocondrias se fragmenten en exceso y corta la sobreproducción de lípidos de la que dependen las células cancerosas. Para el público general, el mensaje clave es que esta proteína actúa como un freno interno sobre la energía y los bloques constructivos que alimentan el crecimiento y la diseminación del cáncer de mama. Fármacos que eleven los niveles de IFFO1 o simulen sus efectos sobre la vía Lamin A/C–PGC1α podrían algún día ofrecer nuevas opciones, especialmente para formas agresivas o resistentes al tratamiento del cáncer de mama.
Cita: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Palabras clave: cáncer de mama, dinámica mitocondrial, síntesis de ácidos grasos, metabolismo tumoral, vía PGC1α