Clear Sky Science · es
El control oncogénico de la síntesis de nucleótidos
Por qué a las células cancerosas les importan los bloques de construcción
El cáncer suele describirse como células que no dejan de dividirse. Pero para copiarse, estas células necesitan un suministro constante de pequeños bloques de construcción llamados nucleótidos, que componen el ADN y el ARN y además ayudan a impulsar muchos procesos celulares. Esta revisión explica cómo los genes que provocan cáncer reconfiguran la química celular para mantener alta la producción de nucleótidos, cómo los tumores alternan entre diferentes maneras de obtener estas moléculas y cómo los médicos pueden explotar estas estrategias con fármacos antiguos y nuevos.
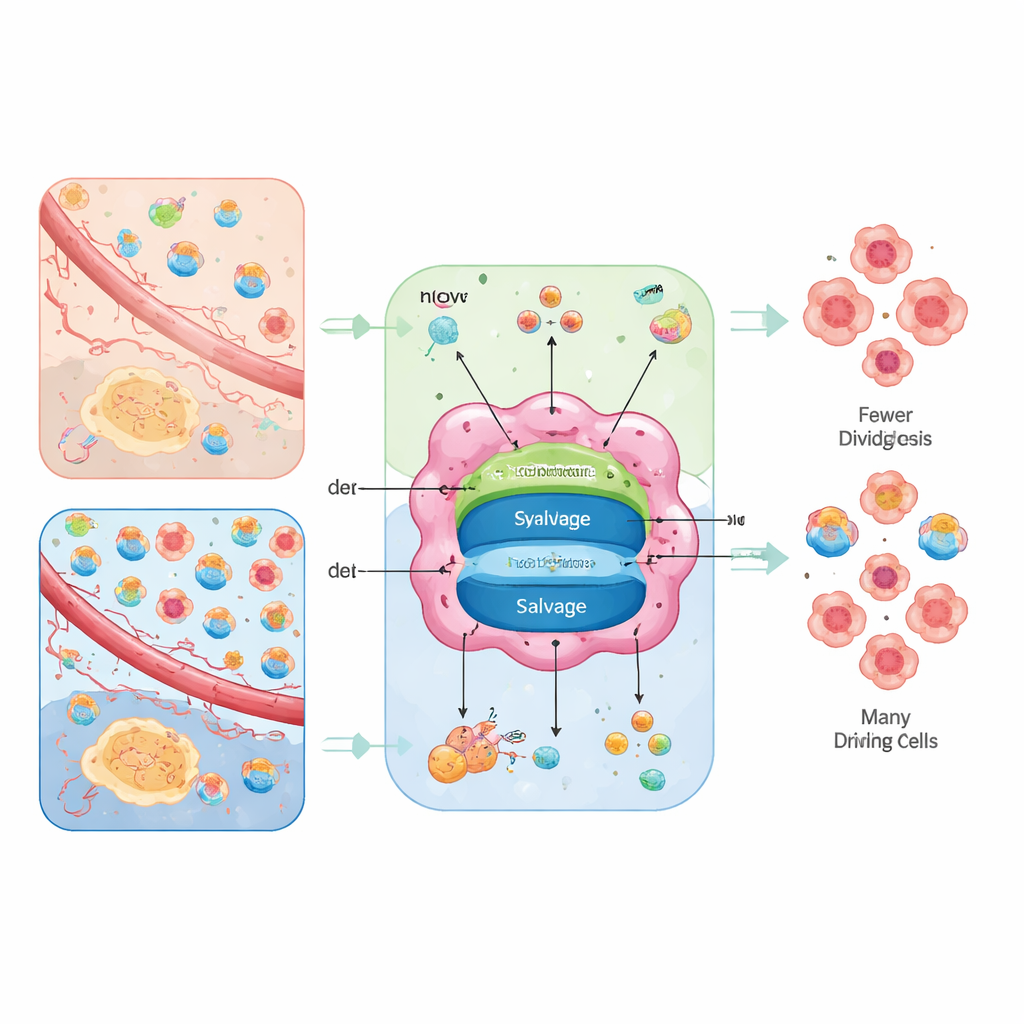
Dos caminos hacia los mismos bloques de construcción
Las células pueden fabricar nucleótidos desde cero o reciclarlos. La ruta «desde cero», llamada síntesis de novo, monta las bases a partir de nutrientes básicos como glucosa, aminoácidos, dióxido de carbono y bicarbonato, mediante reacciones multi‑paso que consumen mucha energía. La ruta de reciclaje, llamada rescate, toma bases y nucleósidos descompuestos del exterior o de los desechos celulares y los reconvierte en nucleótidos utilizables con un coste energético mucho menor. Los tumores usan ambas opciones, pero el equilibrio entre ellas depende de su suministro interno de energía y de lo que aporte el tejido circundante.
Cómo el entorno tumoral guía la elección
Los autores plantean el suministro de nucleótidos como un problema de «encaminamiento moldeado por el entorno». En regiones mal nutridas donde hay aminoácidos pero escasean los nucleósidos libres, las células cancerosas se apoyan en las vías de novo y se vuelven vulnerables a fármacos que bloquean esos pasos. En regiones mejor perfundidas, donde la sangre aporta abundantes nucleósidos o donde las mitocondrias son débiles, los tumores pueden depender más del rescate, volviéndose sensibles entonces a bloqueadores de transportadores que impiden la captación de nucleósidos. Cuando ambas opciones están disponibles, los tumores muestran flexibilidad metabólica y pueden evadir fármacos únicos; cuando ambas se cierran, las células se detienen en la replicación del ADN, acumulan daño y pueden morir o diferenciarse hacia estados más maduros y menos agresivos.
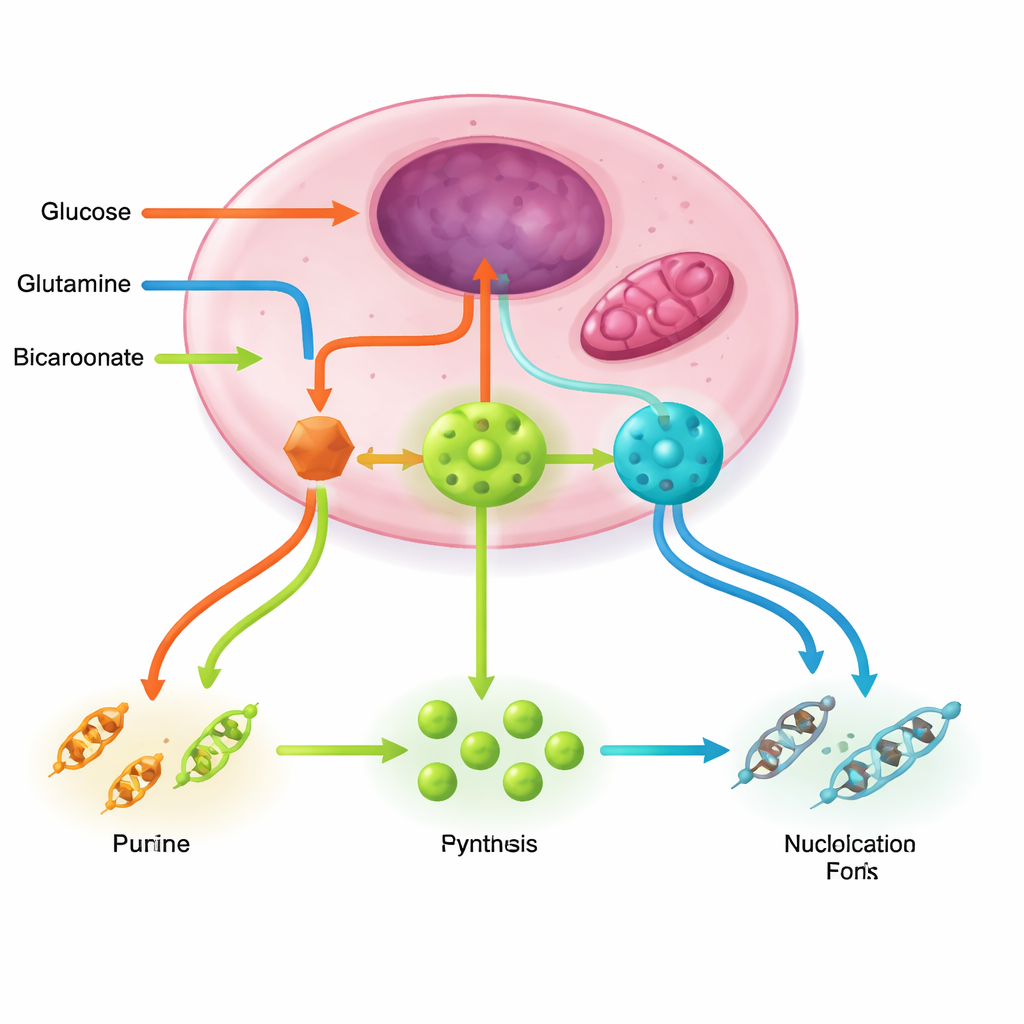
Líneas de apoyo ocultas que alimentan el suministro de nucleótidos
Mantener en marcha las fábricas de nucleótidos exige varios circuitos de apoyo. La vía de las pentosas fosfato proporciona la columna de azúcar y el poder reductor; la glutamina y el ciclo energético mitocondrial suministran nitrógeno y aspartato; la química de serina, glicina y folato dona unidades monocarbonadas que completan los anillos; el bicarbonato aporta carbonos esenciales. Impulsores del cáncer como PI3K–AKT–mTORC1, RAS–MAPK y MYC activan conjuntamente estas vías, elevan enzimas clave e incluso ensamblan complejos multi‑enzimáticos que canalizan eficientemente intermediarios inestables. En contraste, sensores de estrés como LKB1–AMPK y p53 actúan normalmente como frenos, reduciendo la producción de nucleótidos cuando la energía o la integridad del ADN se ven amenazadas—frenos que muchos tumores inactivan.
Quimioterapia antigua, nueva lógica metabólica
Puesto que las células de rápido crecimiento dependen tanto de los nucleótidos, algunos de los primeros quimioterápicos explotaron esta debilidad. Fármacos clásicos como metotrexato, 5‑fluorouracilo, citarabina, gemcitabina y diversos análogos de purinas bloquean el uso del folato, inhiben enzimas específicas o se hacen pasar por bloques defectuosos que envenenan el ADN y el ARN. La revisión reexamina estos medicamentos desde la perspectiva del modelo de encaminamiento, explicando por qué los efectos secundarios y la resistencia son frecuentes: los tejidos no cancerosos también necesitan nucleótidos, y los tumores a menudo pueden desviar el flujo a través del rescate o vías paralelas cuando se bloquea un nodo.
Estrategias de nueva generación y preguntas abiertas
Los enfoques más recientes buscan ser más selectivos atacando las piezas de la red con mayor sesgo tumoral. Se están desarrollando fármacos experimentales contra enzimas mitocondriales de un carbono como MTHFD2, la enzima de pirimidina DHODH y enzimas de purina como IMPDH y PAICS, a menudo en combinaciones que también bloquean los transportadores de rescate. Los autores proponen marcadores prácticos—como niveles de transportadores, densidad de vasos sanguíneos, estado mitocondrial y expresión de enzimas metabólicas concretas—para decidir qué tumores dependen más de la síntesis de novo o del rescate y para emparejar a los pacientes con terapias dirigidas a las vías. De cara al futuro, destacan cuestiones clave, entre ellas cómo cambian estas rutas en el espacio y el tiempo dentro de tumores reales, cómo las células inmunes y estromales circundantes moldean la disponibilidad de nucleótidos y cómo diseñar calendarios de fármacos tolerables que exploten el estrés de replicación sin sobrecargar los tejidos normales. En conjunto, este trabajo sostiene que entender y dirigir el metabolismo de nucleótidos podría convertir un requisito básico de la división celular en una palanca poderosa y personalizada contra el cáncer.
Cita: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Palabras clave: metabolismo de nucleótidos, metabolismo del cáncer, síntesis de novo, vías de rescate, terapias metabólicas