Clear Sky Science · es
Perfilado transcriptómico de células cancerosas y hospedadoras en cocultivo identifica la hipoxia como impulsora del efecto antiproliferativo de la célula muscular esquelética sobre las células cancerosas
Por qué algunos tejidos resisten la diseminación del cáncer
El cáncer suele volverse letal cuando las células tumorales escapan de su sitio original y se asientan en órganos distantes. Curiosamente, algunos tejidos, como los pulmones, son destinos frecuentes, mientras que otros, como el músculo esquelético, casi nunca son colonizados a pesar de constituir una gran parte del peso corporal. Este estudio plantea una pregunta simple pero importante para pacientes y médicos: ¿qué tiene el músculo que lo convierte en un suelo tan pobre para el crecimiento de células cancerosas, y podría comprender esta defensa natural cambiar la forma en que abordamos el tratamiento de la metástasis?
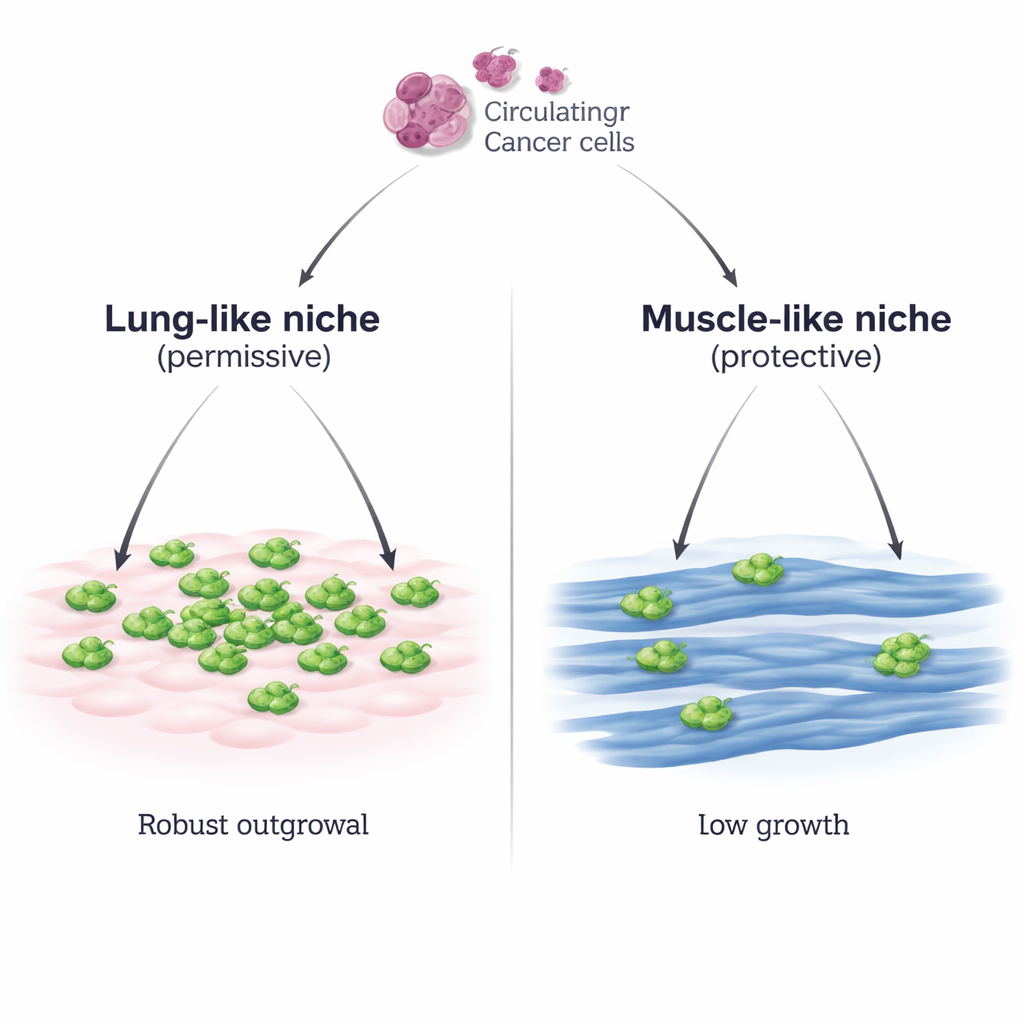
Dos vecindarios para las células tumorales viajeras
Los investigadores construyeron un sistema de laboratorio controlado que imita dos vecindarios distintos que podría encontrar una célula de cáncer de mama: un entorno similar al pulmón compuesto por células del tejido conectivo pulmonar (MLg) y un entorno similar al músculo formado por fibras musculares esqueléticas maduras (miotubos C2C12). Colocaron células de cáncer de mama de ratón sobre cada capa y observaron lo que ocurría. Sobre las células tipo pulmón, las células cancerosas se fijaron bien y luego se multiplicaron rápidamente, formando parches densos. Sobre las células musculares, se adherían igual de bien, pero su crecimiento permaneció escaso y lento, incluso cuando se aumentaba mucho el número inicial de células cancerosas o cuando se usaba una segunda línea de cáncer de mama. Una línea separada de músculo esquelético (Sol8) mostró la misma capacidad para frenar el crecimiento canceroso, subrayando que esto es una propiedad general de las células musculares más que una rareza de un solo tipo celular.
Cómo las células cancerosas y hospedadoras reconfiguran su actividad
Para entender lo que ocurría dentro de las células, el equipo aisló las células cancerosas y las células hospedadoras de estos cultivos mixtos y secuenció su ARN, una medida de qué genes están activados o desactivados. Las células cancerosas sobre fibras musculares presentaron cambios de actividad génica mucho más extensos que las que crecían sobre células pulmonares, lo que sugiere que el entorno muscular las obliga a adaptarse de forma intensa. En el entorno muscular, las células cancerosas activaron programas vinculados a características similares al músculo, al procesamiento energético y, sorprendentemente, a respuestas de baja oxigenación (hipoxia). Al mismo tiempo, los programas génicos habituales que impulsan la división celular rápida se atenuaron. En contraste, las células cancerosas sobre células pulmonares mantuvieron un perfil fuertemente orientado al crecimiento y necesitaron mucha menos reprogramación, coherente con la idea de que el nicho tipo pulmón es permisivo y fácil de explotar para las células tumorales.
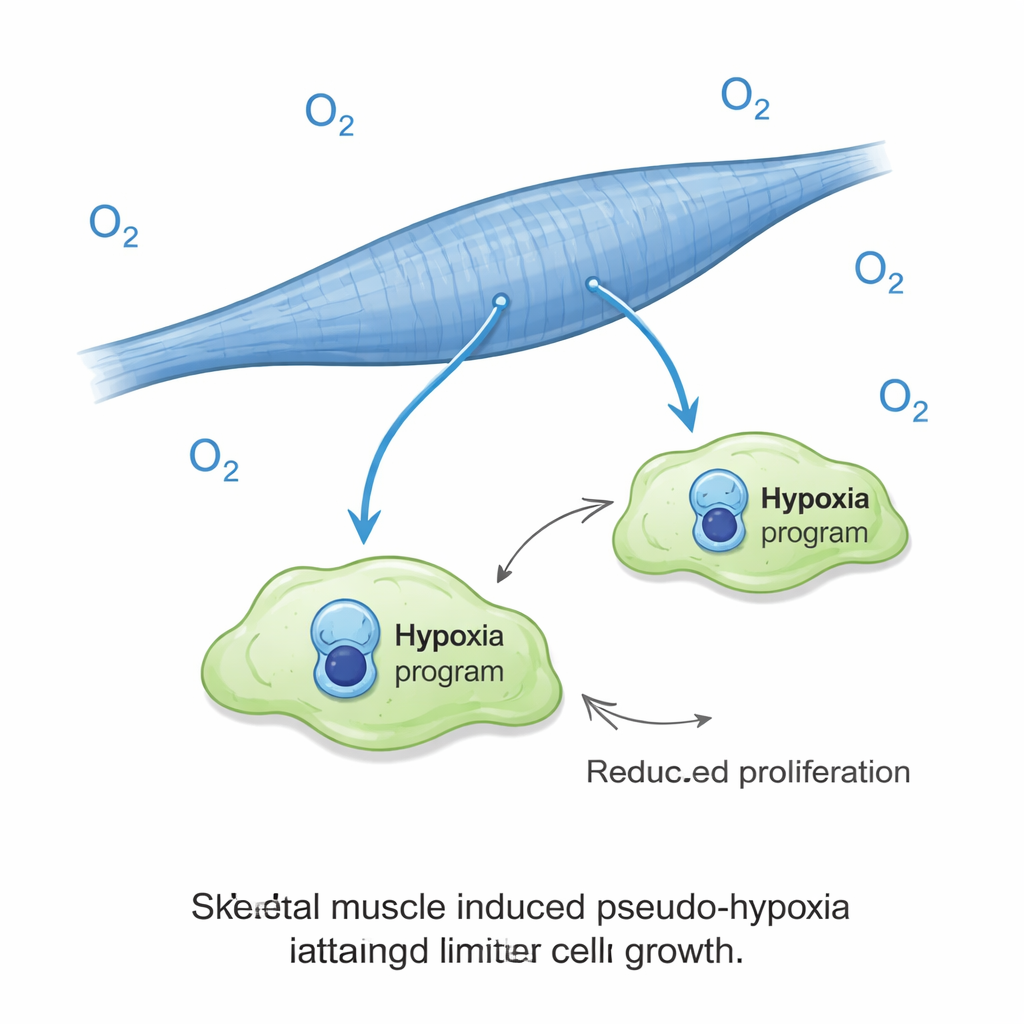
Un papel sorprendente para las señales de baja oxigenación
Uno de los hallazgos más llamativos fue que las células cancerosas sobre fibras musculares activaron una firma génica similar a la hipoxia a pesar de haberse cultivado en niveles normales de oxígeno. En la mayoría de los tumores, la hipoxia es un mal presagio, habitualmente asociada a comportamiento agresivo y malos resultados. Aquí, se asoció con lo contrario: pobre crecimiento. Los científicos expusieron luego los cultivos a oxígeno realmente bajo y comprobaron que esto casi eliminaba la expansión de las células cancerosas en el músculo, mientras que en realidad potenciaba el crecimiento canceroso en los cultivos tipo pulmón. En otras palabras, la misma señal que normalmente ayuda a los tumores a prosperar se convirtió en un freno cuando las células cancerosas estaban en un entorno muscular. Este efecto del oxígeno no pareció explicarse por cambios simples en el lactato, la acidez o la disponibilidad de glucosa en el medio de cultivo.
Más que factores secretados
El equipo también probó si sustancias solubles liberadas por las células musculares podían explicar su efecto protector. Añadir lactato extra, alterar la acidez, cambiar los niveles de glucosa o cultivar las células cancerosas en medio que había bañado previamente células musculares no reprodujo la fuerte supresión observada en los cocultivos en contacto directo. Esto sugiere que el contacto físico cercano, o señales de alcance muy corto en la superficie celular, son clave para que las células musculares empujen a las cancerosas hacia un estado de bajo crecimiento, posiblemente de latencia. Curiosamente, las propias células musculares se mantuvieron relativamente estables en su actividad génica frente al cáncer, mientras que las células pulmonares se reprogramaban con mayor facilidad, destacando al músculo como un tejido robusto y "resistente a la metástasis".
Qué significa esto para pacientes y terapias
En conjunto, el estudio revela que el músculo esquelético actúa como un hábitat hostil que obliga a las células cancerosas a adoptar un modo similar a la hipoxia y de baja proliferación, incluso cuando hay suficiente oxígeno disponible. Esto ayuda a explicar por qué el músculo es un sitio tan raro de metástasis. También ofrece un mensaje de precaución para el desarrollo de fármacos: las terapias diseñadas para bloquear la señalización de la hipoxia en todo el cuerpo podrían debilitar inadvertidamente esta defensa natural basada en el músculo, facilitando que las células cancerosas crezcan donde normalmente no lo harían. Comprender y preservar, o incluso imitar, las características protectoras del tejido muscular podría abrir nuevas vías para prevenir o controlar la enfermedad metastásica.
Cita: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Palabras clave: metástasis del cáncer, músculo esquelético, hipoxia, microambiente tumoral, latencia del cáncer