Clear Sky Science · es
La captación de ácidos grasos mediada por FABP4 promueve la senescencia de las células T CD8+ mediante la peroxidación lipídica en el microambiente rico en adipocitos del cáncer de ovario
Por qué importan la grasa y las células inmunitarias en el cáncer de ovario
El cáncer de ovario a menudo se disemina a la cavidad abdominal, donde encuentra grandes depósitos de tejido adiposo. Este entorno graso no es un telón de fondo pasivo: modela activamente el comportamiento de las células inmunitarias. En particular, puede debilitar a las propias células T CD8 “asesinas” que deberían atacar los tumores. Este estudio explora cómo las sustancias derivadas de la grasa empujan a estas células T hacia un estado envejecido y desgastado, y cómo bloquear una proteína clave de transporte de lípidos podría ayudar a restaurar su capacidad antitumoral.
Entornos ricos en grasa que envejecen a los defensores inmunitarios
Los médicos han observado durante mucho tiempo que muchas mujeres con cáncer de ovario avanzado acumulan líquido en el abdomen y presentan tumores alojados en tejidos ricos en grasa llamados epiplón. Mediante el análisis de datos de ARN unicelular de pacientes y el examen de muestras tumorales al microscopio, los investigadores hallaron que las células T CD8 próximas a estos depósitos de grasa mostraban con mayor probabilidad signos de envejecimiento celular, o senescencia. Estas células T “envejecidas” acumulan pigmentos de desecho, dejan de dividirse y producen señales inflamatorias en vez de matar células tumorales. Tanto en muestras humanas como en modelos murinos, las células T CD8 tomadas de áreas tumorales ricas en grasa y líquido eran visiblemente más senescentes que las procedentes de ganglios linfáticos o bazo, vinculando directamente el microambiente rico en adipocitos con el envejecimiento de las células T.
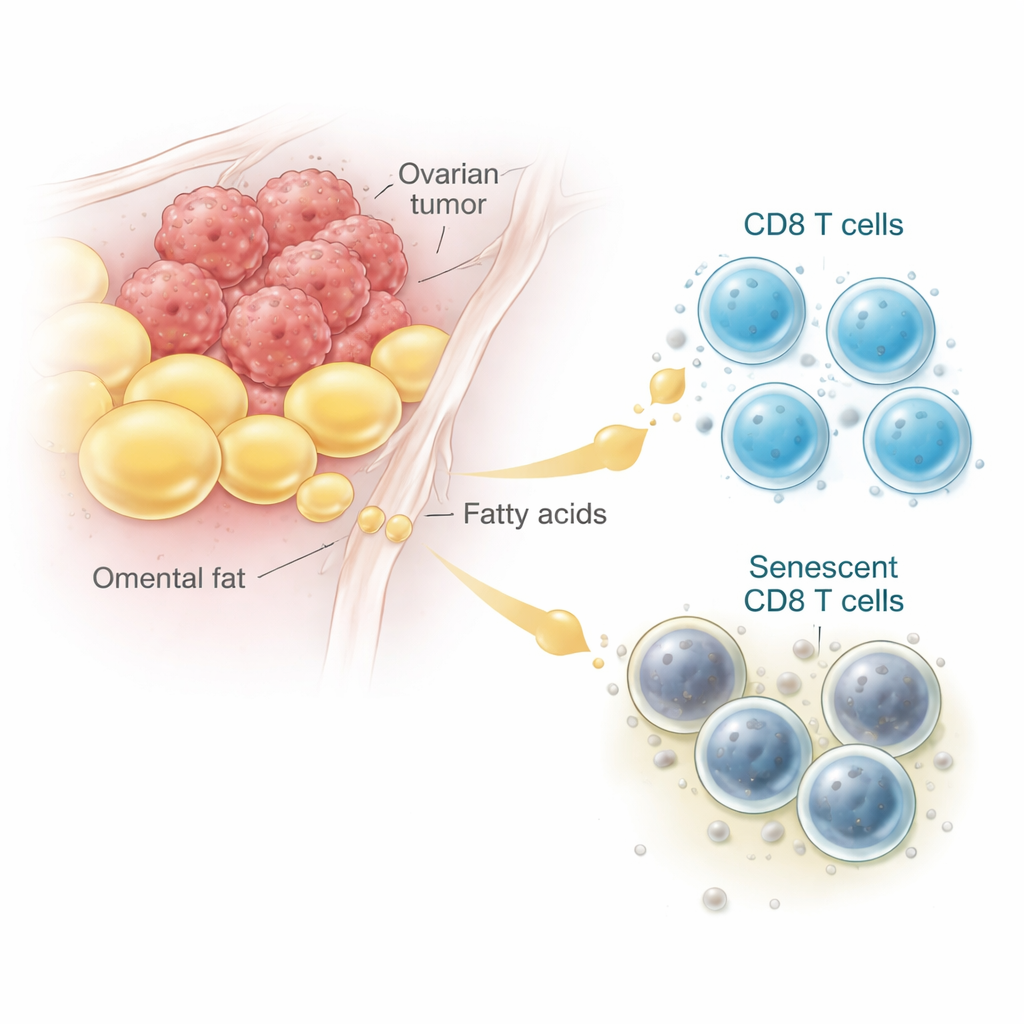
Cómo un ácido graso común convierte el combustible útil en daño
Para entender qué hace la grasa a las células T, el equipo recreó el entorno tumoral en el laboratorio. Crecieron células de cáncer de ovario junto con células T CD8 de ratón y luego añadieron extractos de tejido graso o un ácido graso específico llamado ácido oleico, que es abundante en el líquido de cáncer de ovario. A dosis moderadas a altas, el ácido oleico hizo que más células T CD8 entraran en senescencia, pero solo cuando las células tumorales estaban presentes. En lugar de quemar la grasa entrante como energía, las células T acumularon lípidos que se dañaron químicamente, un proceso conocido como peroxidación lipídica. Los análisis génicos y lipídicos mostraron marcadores aumentados de grasas oxidadas y estrés, mientras que la producción de energía a partir de grasa se mantuvo sin cambios. En resumen, en presencia del tumor, la grasa que debería ser combustible se desvió hacia reacciones dañinas que envejecen y desactivan a las células T.
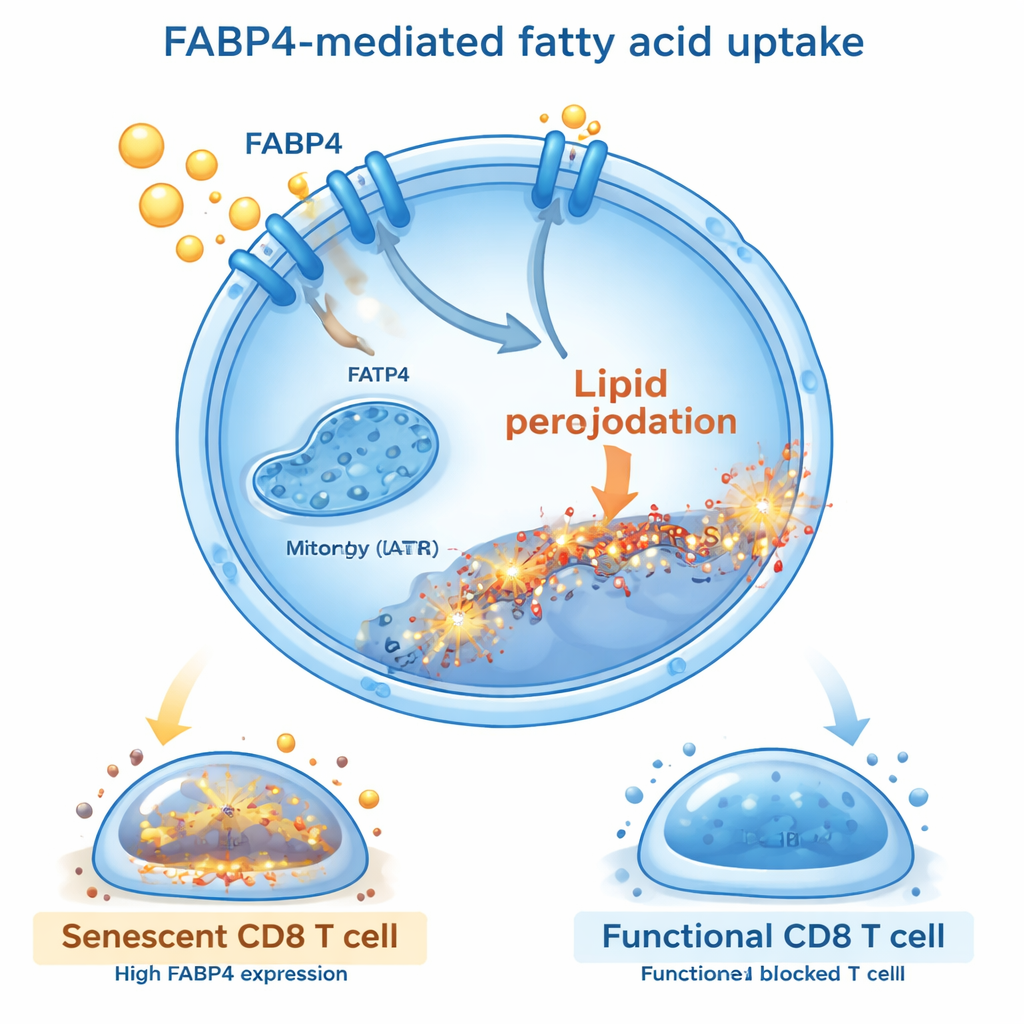
El transportador de grasas FABP4 como guardián clave
Indagando más, los investigadores preguntaron qué moléculas controlaban esta entrada perjudicial de lípidos. Encontraron que una proteína transportadora llamada FABP4 se activaba fuertemente en las células T CD8 expuestas a extractos grasos o ácido oleico. FABP4 actúa como un transportador, llevando ácidos grasos de cadena larga al interior de las células. Cuando bloquearon FABP4 usando un fármaco de pequeña molécula (BMS309403) o mediante silenciamiento genético, las células T captaron menos grasa, presentaron menos peroxidación lipídica y tuvieron menos probabilidad de volverse senescentes. Estas células T protegidas se dividieron mejor, produjeron más moléculas citotóxicas como interferón gamma y granzima B, y liberaron menos señales supresoras e inflamatorias. Restaurar los niveles de FABP4 revirtió estos beneficios, confirmando que este transportador es un interruptor central que vincula la captación de grasa con el envejecimiento de las células T.
De experimentos en ratones a una posible estrategia terapéutica
El equipo probó entonces el bloqueo de FABP4 en ratones vivos con cáncer de ovario diseminado en la cavidad abdominal. Tratar a los ratones con el inhibidor de FABP4 redujo la captación de grasa y el daño lipídico en las células T CD8 extraídas del líquido abdominal, disminuyó la proporción de células T senescentes y aumentó los niveles de moléculas efectoras clave. Cuando el inhibidor de FABP4 se combinó con quimioterapia estándar, los ratones mostraron menos nódulos tumorales visibles, respuestas T más fuertes en bazo, ganglios linfáticos y ascitis, y vivieron más tiempo que los tratados solo con quimioterapia. Estos hallazgos sugieren que dirigir el metabolismo de la grasa puede hacer que los tratamientos existentes sean más efectivos al reavivar a los soldados de primera línea del sistema inmunitario.
Qué significa esto para los pacientes
Para lectores no especializados, la conclusión es que en el cáncer de ovario no solo importa el tumor, sino también el vecindario graso en el que vive. Las moléculas derivadas de la grasa, en especial ciertos ácidos grasos, pueden envejecer prematuramente a las células T asesinas, robándoles su capacidad para combatir el cáncer. Este trabajo identifica al transportador de grasas FABP4 como un culpable clave en ese proceso. Bloquear FABP4, al menos en ratones, puede reducir la senescencia T, restaurar su función citotóxica y mejorar el impacto de la quimioterapia. Aunque se necesita más investigación antes de que esto se convierta en una terapia para pacientes, el estudio abre una nueva vía: tratar no solo el cáncer en sí, sino también las trampas metabólicas de su entorno que desarman al sistema inmunitario.
Cita: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Palabras clave: cáncer de ovario, senescencia de células T, metabolismo de ácidos grasos, microambiente tumoral, FABP4