Clear Sky Science · es
Mutaciones genéticas comunes en 103 líneas celulares de cáncer colorrectal autenticadas
Por qué importan estas líneas celulares de cáncer
El cáncer colorrectal es uno de los tumores más frecuentes en todo el mundo, y gran parte de lo que sabemos sobre su comportamiento y su tratamiento proviene de estudios en líneas celulares de cáncer cultivadas en el laboratorio. Pero estos modelos pueden derivar y cambiar con el tiempo. Este estudio comprobó y catalogó con cuidado 103 líneas celulares de cáncer colorrectal de uso extendido, mapeando las mutaciones génicas clave que impulsan el crecimiento tumoral. El resultado es una "guía de campo" detallada que ayuda a los investigadores a elegir el modelo adecuado para la pregunta adecuada, con el objetivo final de aumentar la probabilidad de que los hallazgos de laboratorio beneficien a los futuros pacientes.
Un catálogo de modelos tumorales
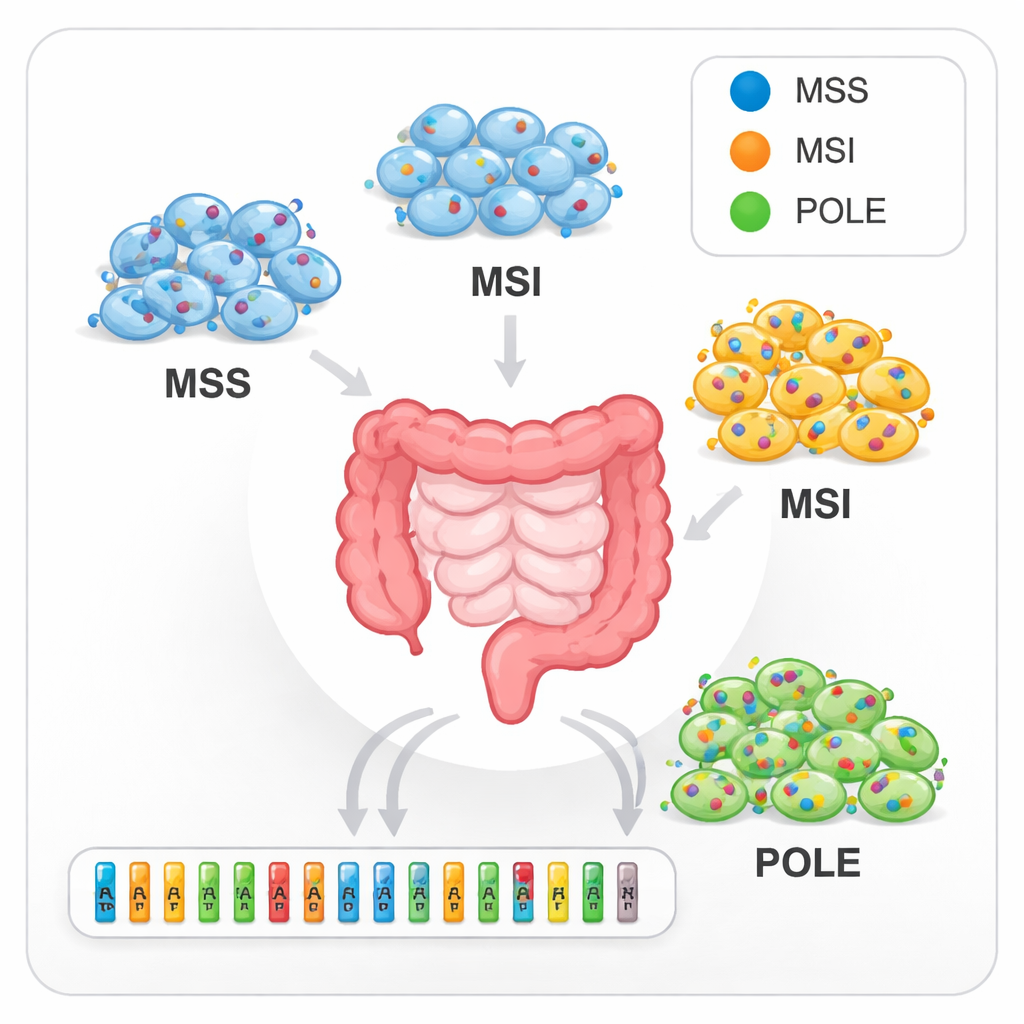
Los investigadores reunieron 103 líneas celulares de cáncer colorrectal que en conjunto reflejan los principales subtipos genéticos observados en pacientes. La mayoría procedían de tumores primarios de colon o recto, y el resto de metástasis. El equipo verificó primero que cada línea celular era realmente lo que decía ser, usando marcadores de ADN tipo huella dactilar llamados repeticiones en tándem cortas. Luego emplearon secuenciación dirigida en profundidad, leyendo tramos seleccionados de ADN en promedio 575 veces, para examinar 20 genes conocidos por su importancia en el cáncer colorrectal. Esta alta profundidad les permitió detectar incluso mutaciones relativamente raras dentro de una población celular y estimar qué proporción de células en una línea concreta portaba cada mutación.
Diferentes caminos hacia el caos genético
Los cánceres colorrectales pueden seguir distintas rutas genéticas durante su desarrollo. Aproximadamente cuatro de cada cinco tumores muestran inestabilidad cromosómica, con grandes fragmentos de ADN ganados o perdidos. Otros son “hipermutados”, acumulando muchos cambios pequeños en el ADN. Este estudio capturó ambos patrones. Dieciséis líneas celulares mostraron inestabilidad de microsatélites, una forma de hipermutación causada por fallos en la reparación por desajuste del ADN, que conduce a inserciones y deleciones pequeñas frecuentes. Otras cinco presentaron defectos en el gen de corrección de pruebas POLE, generando una elevada carga de cambios de una sola base. Las líneas no hipermutadas restantes tenían menos mutaciones pero más cambios a gran escala en el número de copias del ADN. Estas firmas distintas se parecían estrechamente a las observadas en tumores de pacientes reales.
Genes conductores clave y combinaciones peligrosas
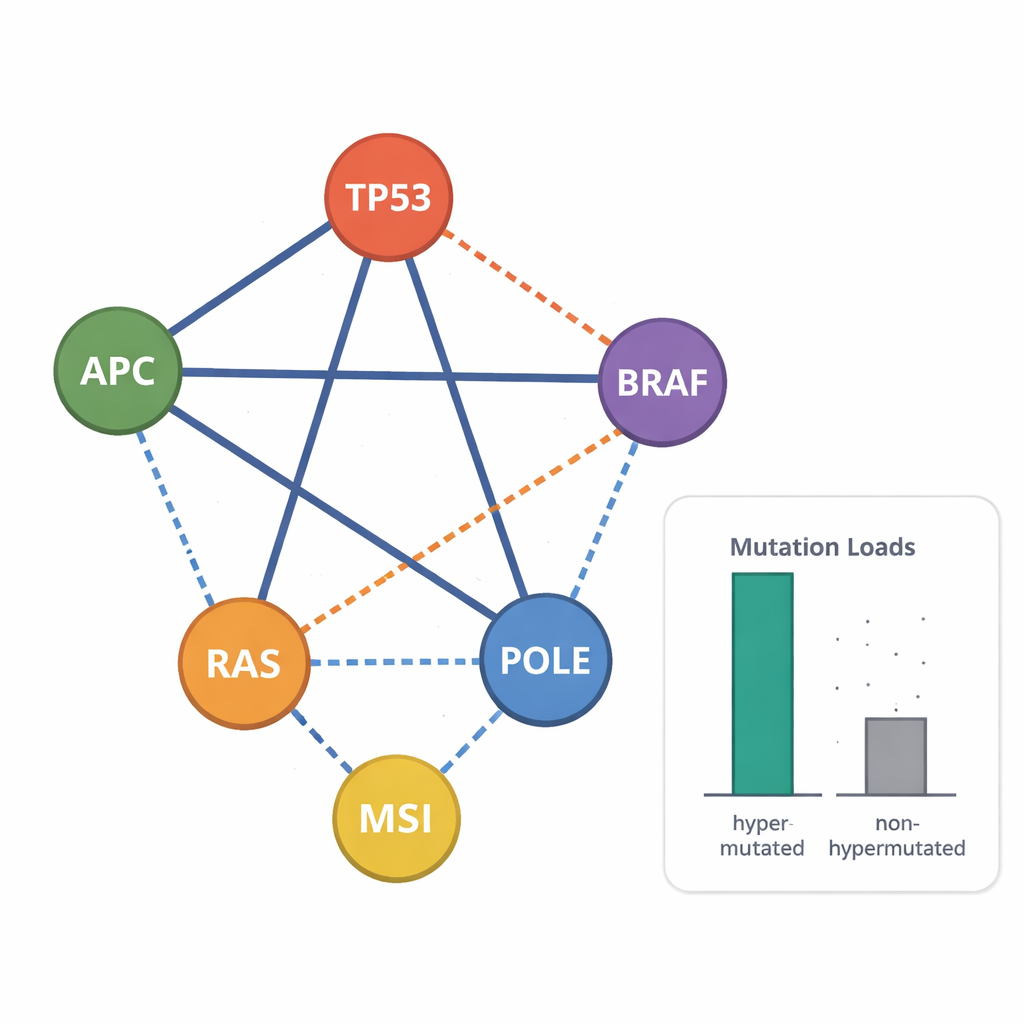
Entre los 20 genes estudiados, los patrones de mutación coincidieron con grandes estudios clínicos sobre cáncer colorrectal. Genes supresores de tumores como APC, TP53 y SMAD4 fueron afectados con frecuencia por mutaciones truncantes que inactivan la proteína, mientras que genes clásicos promotores del cáncer como KRAS y BRAF presentaron con mayor frecuencia sustituciones de un aminoácido que activan vías de señalización. Las líneas no hipermutadas tendían a acumular una mayor proporción de mutaciones claramente dañinas, o patogénicas, presentes en la mayoría o en todas las células del cultivo. En contraste, las líneas hipermutadas exhibían muchos cambios “pasajeros” adicionales y más mutaciones subclonales que aparecen solo en una fracción de las células, reflejando la evolución continua dentro de la placa.
Patrones ocultos en la interacción entre genes
Al observar qué mutaciones tienden a aparecer juntas o a excluirse mutuamente, los científicos pudieron identificar combinaciones genéticas asociadas con enfermedad particularmente agresiva. Por ejemplo, la mutación de punto frecuente BRAF p.V600 raramente coexistía con mutaciones en KRAS o NRAS, pero en un puñado de líneas sí apareció junto a mutaciones truncantes en APC, lo que refleja un subtipo de mal pronóstico observado en pacientes. Muchas líneas celulares mostraron combinaciones triples en APC, TP53 y genes RAS, otro marcador de tumores de alto riesgo. El estudio también reveló un patrón distintivo de “doble golpe” en APC: dos mutaciones truncantes ubicadas de tal manera que al menos una región de unión a β-catenina permanece, coherente con un nivel "justo" de activación de la vía WNT que favorece el crecimiento tumoral. El análisis del número de copias mostró amplificaciones frecuentes de genes relacionados con el crecimiento como MYC y EGFR, y pérdida de copias enteras de genes supresores de tumores, especialmente en las líneas no hipermutadas.
Qué significa esto para la investigación futura
Para los científicos que diseñan experimentos, el mensaje es que no todas las líneas celulares de cáncer colorrectal son iguales. Los modelos hipermutados son genéticamente complejos y pueden contener muchos cambios de bajo nivel que diluyen el impacto de una única mutación. Por el contrario, las líneas no hipermutadas tienden a portar alteraciones conductoras menos numerosas pero más fuertes y más uniformes. Al proporcionar un mapa cuidadosamente validado de qué genes están alterados, cómo lo están y qué tan comunes son esas mutaciones en cada cultivo, este trabajo permite a los investigadores elegir los modelos más apropiados para probar fármacos, explorar la biología y desarrollar nuevos enfoques dirigidos o inmunoterapéuticos para el cáncer colorrectal.
Cita: Kranjec, C., Eilertsen, I.A., Nunes, L. et al. Common gene mutations in 103 authenticated colorectal cancer cell lines. Oncogenesis 15, 8 (2026). https://doi.org/10.1038/s41389-026-00599-0
Palabras clave: cáncer colorrectal, líneas celulares de cáncer, mutaciones génicas, subtipos tumorales, oncología de precisión