Clear Sky Science · es
Reorganización del citoesqueleto inducida por una nueva fusión de queratinas K6-K14 promueve la condición de célula madre cancerosa y la plasticidad celular mediante selección cGAS-STING
Cómo las células cancerosas que cambian de forma engañan a su entorno
Las células cancerosas no solo proliferan sin control; además aprenden a doblar y torcer su propio “esqueleto” interno para sobrevivir, esconderse y diseminarse. Este estudio revela cómo un fallo estructural específico dentro de células de cáncer de cabeza y cuello puede fracturar sus núcleos, activar una alarma de peligro interna, empujarlas a un estado de latencia y, en última instancia, ayudarlas a reaparecer como células más agresivas, invasivas y con rasgos de célula madre. Entender esta vía mecánica de la evolución tumoral podría abrir nuevas formas de bloquear las recaídas y las metástasis.
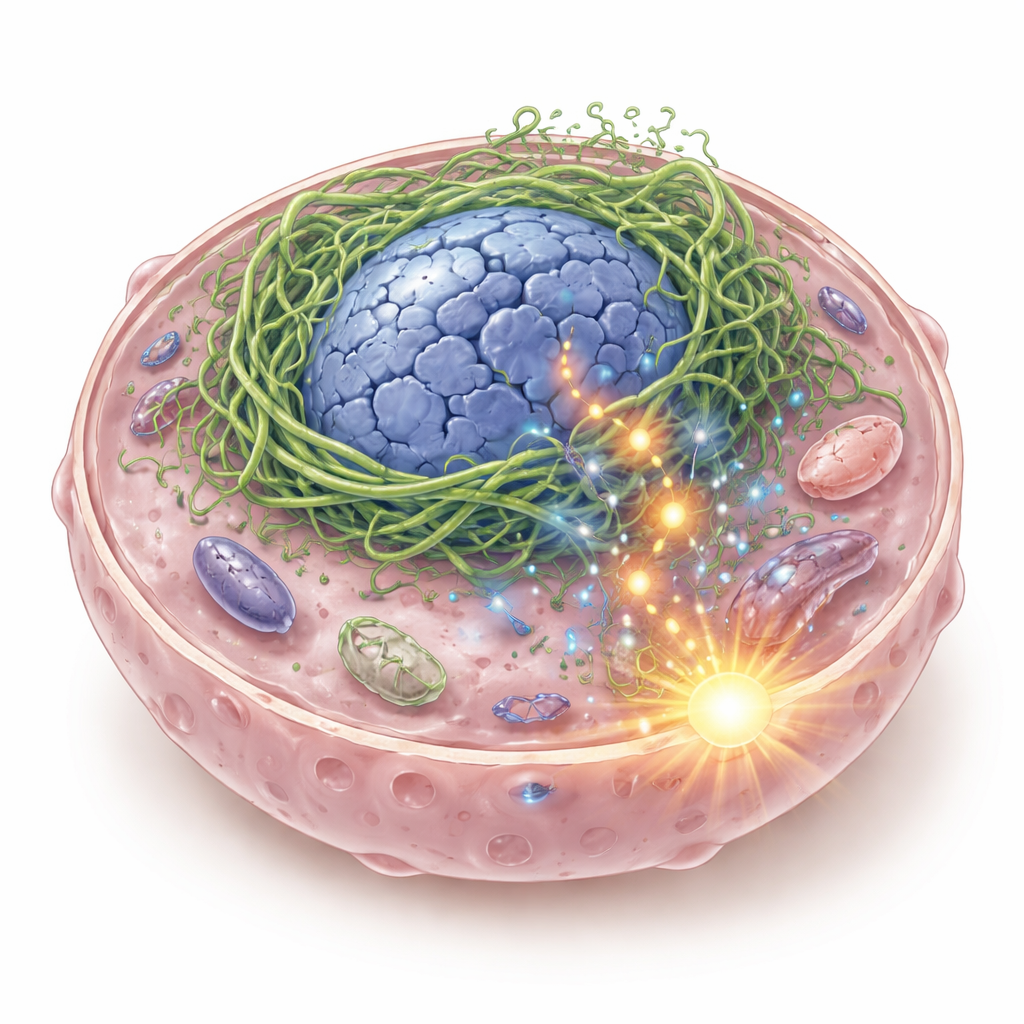
Un andamiaje interno roto con consecuencias peligrosas
Dentro de cada célula hay un andamiaje flexible formado por filamentos proteicos que mantiene la forma de la célula y su núcleo y le ayuda a percibir fuerzas físicas. Los autores se centraron en las queratinas, una familia de proteínas de andamiaje comunes en tejidos epiteliales, incluidos los que recubren la boca y la garganta. En algunos carcinomas escamosos de cabeza y cuello, descubrieron una queratina híbrida llamada K6-K14/V5, formada cuando se fusionan dos genes de queratina. Cuando esta proteína de fusión se expresa en las células cancerosas, no forma una red de soporte uniforme. En su lugar, se agrupa fuertemente alrededor del núcleo, deformándolo en estructuras huecas y de forma anómala y provocando roturas del ADN. Fragmentos de ADN se filtran al citoplasma, donde son detectados por un sistema sensor inmunitario llamado cGAS–STING, que normalmente activa la alarma ante ADN viral.
De la presión hacia la muerte celular a una supervivencia oculta
El efecto inmediato de este daño nuclear es perjudicial para las células cancerosas: su crecimiento se ralentiza y muchas mueren. Sin embargo, una fracción logra sobrevivir. Estos supervivientes están fuertemente condicionados por su entorno físico. En placas plásticas planas estándar desaparecen gradualmente, pero cuando se cultivan en un gel blando de colágeno—más cercano a la textura del tejido real—persisten y reaparecen como una nueva población denominada células 3D-V5. Los análisis de actividad génica muestran que estas células responden a la alarma de daño de ADN activando la autofagia, un programa de limpieza que recicla partes dañadas, en especial mitocondrias defectuosas. Esta respuesta les permite entrar en un estado de latencia y baja actividad que las ayuda a soportar el estrés en lugar de ser eliminadas.
Las células latentes se reprograman y se preparan para moverse
Mientras permanecen latentes, estos supervivientes reescriben silenciosamente sus programas internos. Cambian la mezcla de proteínas queratínicas y adoptan un estado de transición epitelio–mesénquima “parcial” (pEMT), una identidad intermedia que conserva algunos rasgos epiteliales pero gana flexibilidad y motilidad. Mejoran notablemente su capacidad para formar esferas y sembrar nuevos cúmulos celulares, una característica de la condición de célula madre cancerosa. Con el tiempo, sus propiedades mecánicas se recuperan: vuelven a endurecer sus núcleos, reconstruyen fibras de actina robustas y desarrollan prolongaciones largas que sondea y se anclan en la matriz circundante. También aumentan enzimas llamadas metaloproteinasas de matriz (MMPs), que degradan la red extracelular y abren caminos para la invasión.
Comunicación con células vecinas para construir un nicho favorable
Estas células cancerosas reprogramadas no actúan en solitario. El equipo observó que las células 3D-V5 liberan gran cantidad de diminutos paquetes llamados vesículas extracelulares al entorno. Cuando estas vesículas alcanzan fibroblastos orales cercanos—células del tejido conjuntivo—los fibroblastos modifican su propia actividad génica, adoptando un fenotipo más parecido al de fibroblastos asociados a tumores que favorecen el crecimiento tumoral. Muchas de las señales intercambiadas giran en torno al eje FGF–FGFR, una familia de factores de crecimiento y sus receptores conocida por impulsar la proliferación, la plasticidad y la resistencia. Tanto en cultivos como en tumores en ratón, bloquear la actividad de FGFR redujo esta ventaja de crecimiento. En animales, los tumores formados por células 3D-V5 estaban pobremente diferenciados, eran más invasivos, ricos en marcadores de célula madre y más propensos a diseminarse más allá del lugar de inyección.
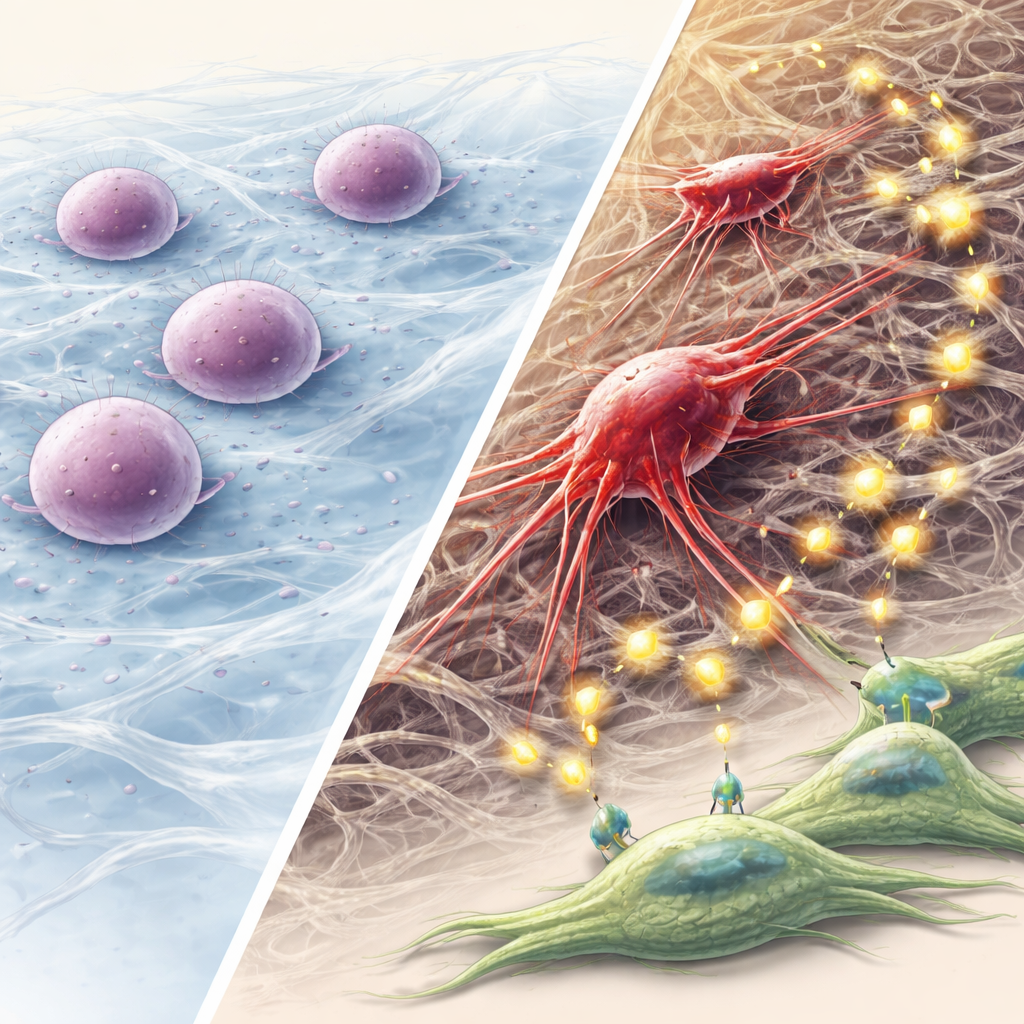
Por qué importa esta vía mecánica hacia un cáncer agresivo
Este trabajo propone un modelo por etapas: una fusión de queratina altera el andamiaje interno de la célula, aplasta el núcleo y desencadena una alarma por daño en el ADN; la autofagia permite que unas pocas células entren en latencia en vez de morir; con el tiempo, estos supervivientes reorganizan su citoesqueleto, adquieren rasgos de célula madre e invasividad, y remodelan su entorno mediante vesículas y señalización FGF. Para quienes no son especialistas, el mensaje clave es que las fuerzas físicas y las proteínas estructurales dentro de las células pueden ser tan importantes como los genes y los compuestos químicos en la conducción de la evolución del cáncer. Apuntar a esta vía de estrés mecánico–autofagia–FGF, especialmente en cánceres de cabeza y cuello con fusiones de queratina, podría ofrecer nuevas estrategias para evitar que las células tumorales latentes se reactivuen y se diseminen.
Cita: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Palabras clave: capacidad de célula madre cancerosa, citoesqueleto celular, latencia tumoral, cáncer de cabeza y cuello, mecano-transducción