Clear Sky Science · es
El papel de la desmetilasa de histonas PHF2 como supresora tumoral en el carcinoma hepatocelular mediante la regulación de SRXN1
Por qué importa este estudio sobre el cáncer de hígado
El cáncer de hígado es uno de los más mortales a nivel mundial, y los fármacos actuales solo prolongan la vida de forma modesta en muchos pacientes. Este estudio plantea una pregunta distinta: en lugar de dirigirse a los genes clásicos impulsores del cáncer, ¿podemos aprovechar la forma en que el ADN se empaqueta y se marca químicamente dentro de las células hepáticas para encontrar nuevas opciones de tratamiento más precisas? Los investigadores se centran en una proteína poco conocida llamada PHF2 y revelan cómo podría ayudar a impedir que las células hepáticas se vuelvan cancerosas.
Buscando debilidades en el sistema de control del cáncer
El cáncer no está impulsado solo por genes dañados; también se alimenta de controles “epigenéticos” defectuosos: las marcas químicas y los complejos proteicos que deciden qué genes se activan o se silencian. En el carcinoma hepatocelular, la forma más común de cáncer de hígado, muchos de esos reguladores están alterados. El equipo evaluó de forma sistemática 497 reguladores epigenéticos en seis líneas celulares de cáncer de hígado, usando herramientas de ARN para reducir temporalmente cada regulador uno por uno y luego midiendo la supervivencia de las células tumorales. Esta amplia criba estaba diseñada para revelar de qué reguladores dependen los cánceres para crecer y cuáles actúan normalmente como frenos en la formación de tumores.
Encontrar nuevos ayudantes y protectores del cáncer
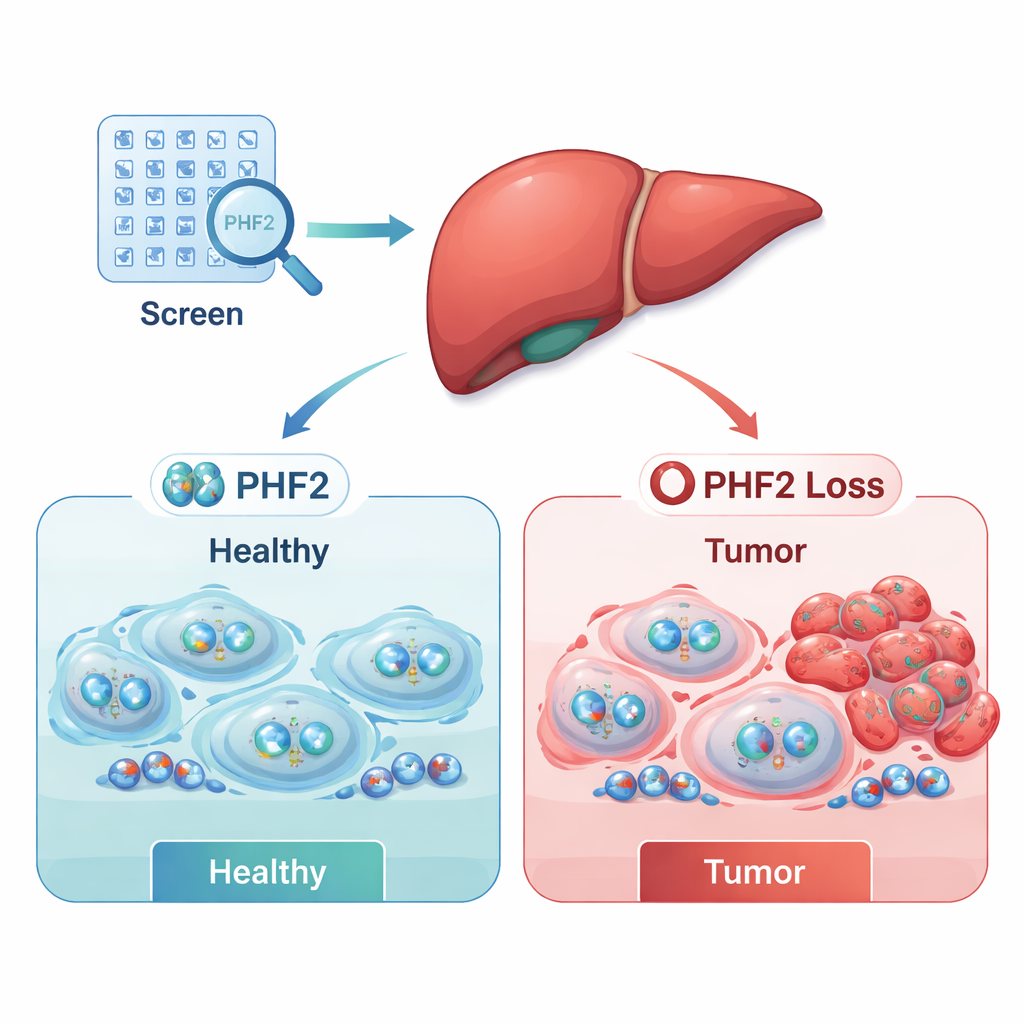
La criba descubrió dos grupos amplios: posibles “aceleradores” del cáncer (oncogenes) cuya pérdida perjudicaba la supervivencia celular, y posibles “frenos” (sustentadores tumorales) cuya pérdida favorecía el crecimiento de las células cancerosas. Al combinar sus datos de laboratorio con grandes conjuntos de datos clínicos públicos, los investigadores redujeron la lista a unos pocos candidatos relevantes clínicamente. Dos reguladores, SUPT7L y SMARCC1, tendían a estar más activos en los tumores y se asociaban con una supervivencia peor. En contraste, un regulador—PHF2—suele estar menos activo en los tumores hepáticos, y los pacientes cuyos tumores mantenían niveles más altos de PHF2 generalmente vivían más. Estos patrones sugerían que PHF2 podría actuar como supresor tumoral en el cáncer de hígado humano.
Cómo cambia el cáncer de hígado al perder PHF2
Para evaluar PHF2 con más profundidad, el equipo diseñó células de cáncer hepático que producían de forma estable menos de esta proteína y siguió su comportamiento a lo largo del tiempo. Las células con PHF2 reducido crecían más rápido y mostraban niveles más altos de Ki-67, un marcador de división celular activa, lo que indica que PHF2 normalmente ayuda a frenar la proliferación. Estos efectos fueron más pronunciados en líneas celulares de cáncer de hígado ya agresivas, lo que sugiere que la simple pérdida de PHF2 puede no iniciar el cáncer por sí sola, pero sí puede acelerar el crecimiento de células malignas una vez que los tumores se han formado.
Un vínculo sorprendente con las defensas frente al estrés celular
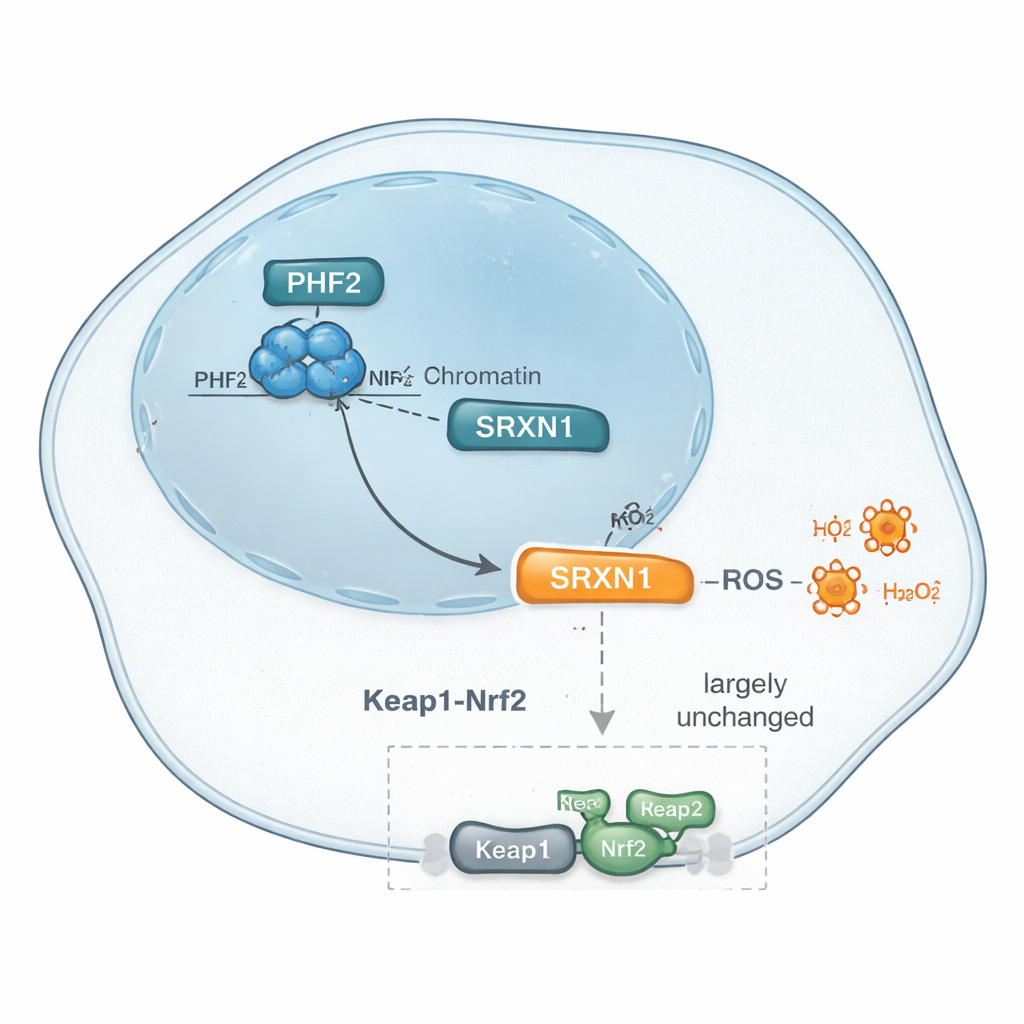
A continuación, los investigadores utilizaron métodos modernos de perfilado proteico para catalogar miles de proteínas cuyos niveles cambiaban cuando PHF2 se reducía. Entre muchos cambios sutiles, destacó un patrón: los niveles de una proteína protectora frente al estrés llamada SRXN1 bajaban de manera consistente cuando se perdía PHF2. SRXN1 ayuda a las células a gestionar las especies reactivas de oxígeno—subproductos químicamente reactivos que pueden dañar el ADN y las proteínas, pero que también pueden forzar a las células cancerosas a adaptarse. Los datos sugirieron que PHF2 contribuye a mantener los niveles de SRXN1, y que alterar este equilibrio podría influir en cómo las células de cáncer de hígado responden al estrés interno y, en última instancia, en la velocidad a la que crecen.
Actuando fuera de una vía de estrés conocida
SRXN1 suele controlarse por un conmutador maestro de la respuesta al estrés llamado Nrf2, que activa muchos genes antioxidantes cuando las células afrontan estrés oxidativo. Dado que SRXN1 disminuía al suprimir PHF2, el equipo preguntó si PHF2 podría estar actuando simplemente a través de esta conocida vía de Nrf2. Examinaron genes y proteínas clave relacionadas con Nrf2, trataron las células con fármacos que activan Nrf2 bloqueando su inhibidor Keap1, y usaron herramientas genéticas para reducir Keap1 directamente. En todas estas pruebas, la respuesta de las células deficientes en PHF2 se parecía mucho a la de las células normales, y los análisis de vías y factores de transcripción no destacaron a Nrf2 como actor principal. En cambio, surgieron como candidatos otros factores, incluidos ZNF384 y Nrf1—ambos anteriormente vinculados al cáncer de hígado. En conjunto, la evidencia sugiere que el control de PHF2 sobre SRXN1 y las respuestas antioxidantes puede eludir la señalización clásica de Nrf2, apuntando a una vía distinta de regulación del estrés en estos tumores.
Qué podría significar esto para tratamientos futuros
Para un público no especialista, la conclusión principal es que este estudio identifica a PHF2 como un factor protector prometedor en el cáncer de hígado: cuando PHF2 está presente y activo, las células tumorales crecen más despacio; cuando se reduce, ganan ventaja de crecimiento y cambian la forma en que gestionan el estrés celular. Dado que PHF2 en sí puede ser difícil de bloquear o potenciar con fármacos convencionales de pequeña molécula, los autores señalan estrategias emergentes como las terapias basadas en ARN o fármacos que mejoren la actividad de PHF2 a través de sus socios en vías de señalización ascendentes. También destacan que los efectos de PHF2 dependen del contexto—su impacto puede variar con otras mutaciones como el estado de p53—por lo que cualquier terapia futura probablemente requeriría una cuidadosa selección de pacientes. En conjunto, el trabajo refina nuestra comprensión de cómo los reguladores epigenéticos moldean el comportamiento del cáncer de hígado y abre nuevas vías para diseñar tratamientos que restauren o imiten la influencia supresora tumoral de PHF2.
Cita: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Palabras clave: carcinoma hepatocelular, regulación epigenética, PHF2, SRXN1, terapia contra el cáncer de hígado