Clear Sky Science · es
La degradación mediada por TRIM21 de HILPDA supera la resistencia a la inmunoterapia anti‑PD‑1 en el cáncer de mama al limitar la palmitoilación de PD‑L1
Por qué algunas inmunoterapias contra el cáncer dejan de funcionar
Los fármacos que liberan al sistema inmune, como las terapias anti‑PD‑1, han transformado el tratamiento de varios cánceres, incluidas formas agresivas de cáncer de mama. Sin embargo, muchos tumores o bien no responden nunca o acaban encontrando maneras de escapar. Este estudio examina una de esas rutas de escape en el cáncer de mama triple negativo y muestra cómo reconectar el metabolismo lipídico tumoral —y un fármaco reposicionado llamado fenretinida— podría reabrir la puerta al sistema inmunitario cuando la inmunoterapia estándar falla. 
Un cómplice oculto que protege a los tumores
Los investigadores se centraron en una proteína poco conocida llamada HILPDA, previamente vinculada a cómo las células gestionan las grasas bajo estrés. Al comparar tumores mamarios en ratones que seguían siendo sensibles a la terapia anti‑PD‑1 con tumores que se habían vuelto resistentes, encontraron que los niveles de HILPDA eran mucho más altos en los cánceres resistentes. Análisis de grandes bases de datos de pacientes y de muestras tumorales de mujeres con cáncer de mama confirmaron que HILPDA es más abundante en los tumores que en el tejido mamario normal, especialmente en la enfermedad triple negativa, y que las pacientes cuyos tumores expresan más HILPDA tienden a tener peores resultados. Los tumores de personas que no se beneficiaron de fármacos que bloquean PD‑1 también presentaban más HILPDA, vinculando esta proteína directamente al fracaso del tratamiento.
Cómo los tumores convierten el paisaje inmune en su contra
Para ver qué hace HILPDA dentro de los tumores, el equipo diseñó células de cáncer de mama que o bien sobreproducían la proteína o carecían de ella y luego las cultivó con células inmunes humanas o en ratones. Cuando HILPDA era alto, los tumores atraían más células T reguladoras, células supresoras derivadas de la médula mieloide y macrófagos de tipo M2 —tipos de células inmunes que atenúan el ataque y ayudan a los cánceres a esconderse. Al mismo tiempo, el número y la energía de las células CD8 asesinas y de las células NK disminuían, y su capacidad para liberar moléculas tóxicas y señales inflamatorias se veía reducida. Silenciar HILPDA cambió este guion: los tumores albergaban menos células supresoras, más células asesinas activas, crecían más despacio y produjeron menos metástasis. De forma crucial, cuando animales con tumores de baja expresión de HILPDA recibieron terapia anti‑PD‑1, sus tumores se encogieron más y los ratones vivieron más, demostrando que HILPDA controla la eficacia de la inmunoterapia.
Producción de grasa, armadura molecular y escape inmune
Indagando más, los científicos descubrieron cómo HILPDA remodela el metabolismo tumoral para reforzar las defensas inmunes. Dentro de las células cancerosas, HILPDA se une a una proteína chaperona llamada HSP90 para estabilizar un factor de transcripción, KLF5, que impulsa la producción de lípidos. Este trío aumenta la síntesis de ácidos grasos, especialmente palmitato, y llena las células tumorales de gotículas lipídicas. Una de estas grasas se une entonces a PD‑L1, la proteína de control que se sitúa en la superficie tumoral y envía una señal de “no atacar” a las células inmunes. El equipo mostró que agregar palmitato a un punto específico de PD‑L1 actúa como un pegamento molecular: ayuda a que PD‑L1 se mantenga estable en la membrana celular y evita que sea degradada. Mutar este único sitio de unión despojó a PD‑L1 de su estabilidad y debilitó su capacidad para proteger a las células cancerosas, incluso cuando HILPDA era abundante. En otras palabras, la producción de lípidos impulsada por HILPDA alimenta una modificación química en PD‑L1 que transforma el escudo inmune del tumor de endeble a reforzado.
El freno incorporado que puede activarse
Cualquier acelerador necesita un freno, y aquí el freno es otra proteína llamada TRIM21. Los autores descubrieron que TRIM21 reconoce HILPDA y la etiqueta con “marcas” moleculares que la envían al sistema de eliminación de la célula. En los tumores mamarios de pacientes, los niveles de TRIM21 tendían a ser bajos cuando HILPDA era alto, y un TRIM21 bajo se asoció con peores resultados, lo que sugiere que este sistema de frenado natural suele estar debilitado en el cáncer. El equipo buscó entonces fármacos que pudieran potenciar TRIM21 e identificó la fenretinida, un retinoide ya probado en humanos. En modelos celulares y animales de cáncer de mama triple negativo, la fenretinida aumentó la actividad de TRIM21, aceleró la degradación de HILPDA, redujo la síntesis de lípidos y la modificación protectora de PD‑L1, y frenó el crecimiento y la diseminación tumoral. De manera más llamativa, combinar fenretinida con terapia anti‑PD‑1 volvió a los tumores más vulnerables al ataque inmune, aumentando las células T asesinas y las NK mientras reducía las células supresoras en el microambiente tumoral. 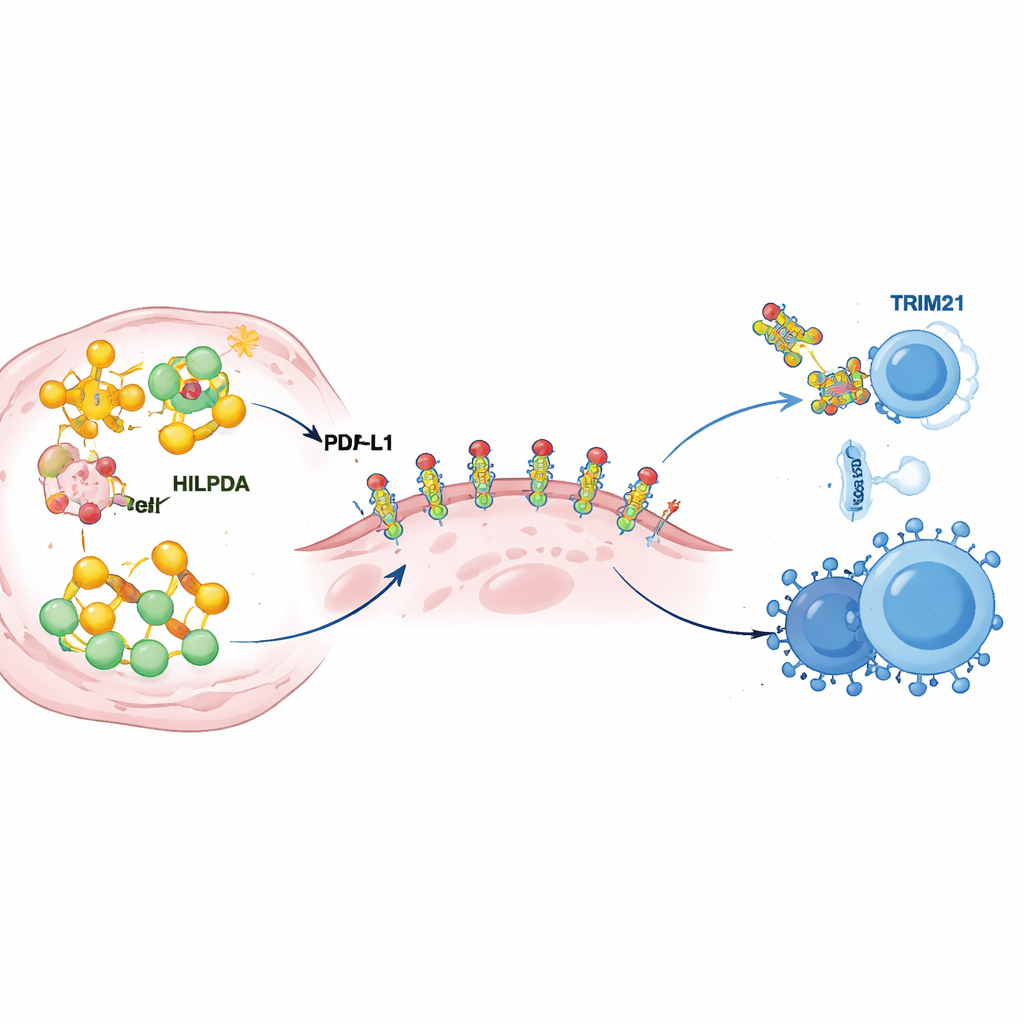
Qué significa esto para la atención oncológica futura
Este trabajo revela una cadena de acontecimientos en la que las células de cáncer de mama sometidas a estrés elevan HILPDA, aumentan la producción de lípidos y refuerzan químicamente PD‑L1 en su superficie, lo que les permite seguir suprimiendo a las células inmunes incluso frente a fármacos que bloquean PD‑1. TRIM21 actúa como una salvaguarda interna que puede desmontar HILPDA, pero a menudo es demasiado débil en los tumores. Al encontrar que la fenretinida puede reactivar esta salvaguarda, el estudio apunta a una vía práctica para combinar un fármaco metabólico con inmunoterapia existente y superar la resistencia. Si se confirma en ensayos clínicos, dirigirse al eje TRIM21–HILPDA–PD‑L1 podría dar a las pacientes con cáncer de mama triple negativo difícil de tratar una segunda oportunidad de beneficiarse de terapias basadas en el sistema inmune.
Cita: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Palabras clave: cáncer de mama triple negativo, resistencia a la inmunoterapia, palmitoilación de PD‑L1, metabolismo lipídico tumoral, fenretinida