Clear Sky Science · es
Cereblon (CRBN) inhibe la metástasis del cáncer de próstata al regular negativamente la 6‑fosfogluconato deshidrogenasa (6PGD)
Por qué importa esta investigación
Cuando el cáncer de próstata se disemina desde la próstata a otros órganos, su tratamiento se complica mucho y a menudo resulta mortal. Este estudio revela cómo una proteína de “control de calidad” celular poco conocida, cereblon (CRBN), ayuda a impedir la diseminación del cáncer de próstata desmantelando una enzima metabólica que impulsa el comportamiento agresivo. Entender este sistema de freno incorporado sugiere nuevas formas de ralentizar o detener la metástasis, especialmente en formas de la enfermedad difíciles de tratar.
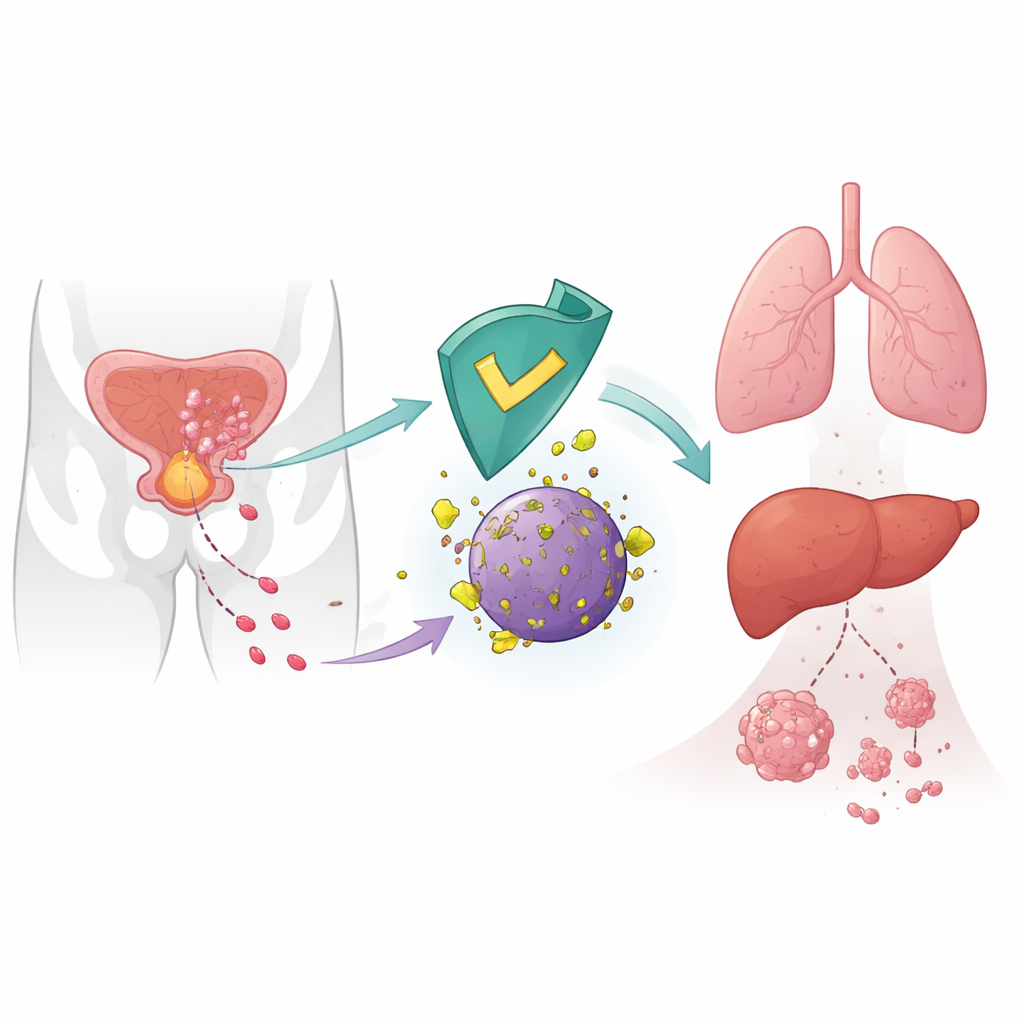
Un freno interno a la diseminación del cáncer
Las células cancerosas no se diseminan al azar; reconfiguran su maquinaria interna para moverse, invadir y colonizar órganos distantes. Los autores se centraron en CRBN, una proteína conocida principalmente como diana de fármacos como la talidomida usados en cánceres hematológicos. En células sanas, CRBN forma parte de una unidad molecular de eliminación que etiqueta ciertas proteínas para su destrucción. Trabajos anteriores sugerían que niveles bajos de CRBN en tumores se asociaban con peores resultados, pero su papel directo en la metástasis no estaba claro. Aquí, los investigadores muestran que CRBN actúa como un supresor natural de la diseminación del cáncer de próstata al dirigir una enzima metabólica llamada 6‑fosfogluconato deshidrogenasa (6PGD) hacia su degradación.
Un motor metabólico que el cáncer secuestra
6PGD forma parte de una ruta metabólica conocida como la vía oxidativa de las pentosas fosfato, que ayuda a las células a generar NADPH, una molécula que provee tanto bloques constructores como poder antioxidante. Muchos tumores aumentan esta vía para crecer más rápido y tolerar el estrés. El equipo encontró que las muestras de cáncer de próstata de pacientes tienden a presentar menos CRBN y más 6PGD que el tejido prostático normal, y que este desequilibrio es especialmente pronunciado en las enfermedades agresivas. En líneas celulares de cáncer de próstata, reducir CRBN o degradarlo con un compuesto diseñado aumentó los niveles de proteína y la actividad enzimática de 6PGD, elevando el NADPH. Restaurar CRBN producía el efecto contrario, disminuyendo 6PGD y NADPH sin alterar el mensaje génico de 6PGD, lo que apunta a un control a nivel de proteína.
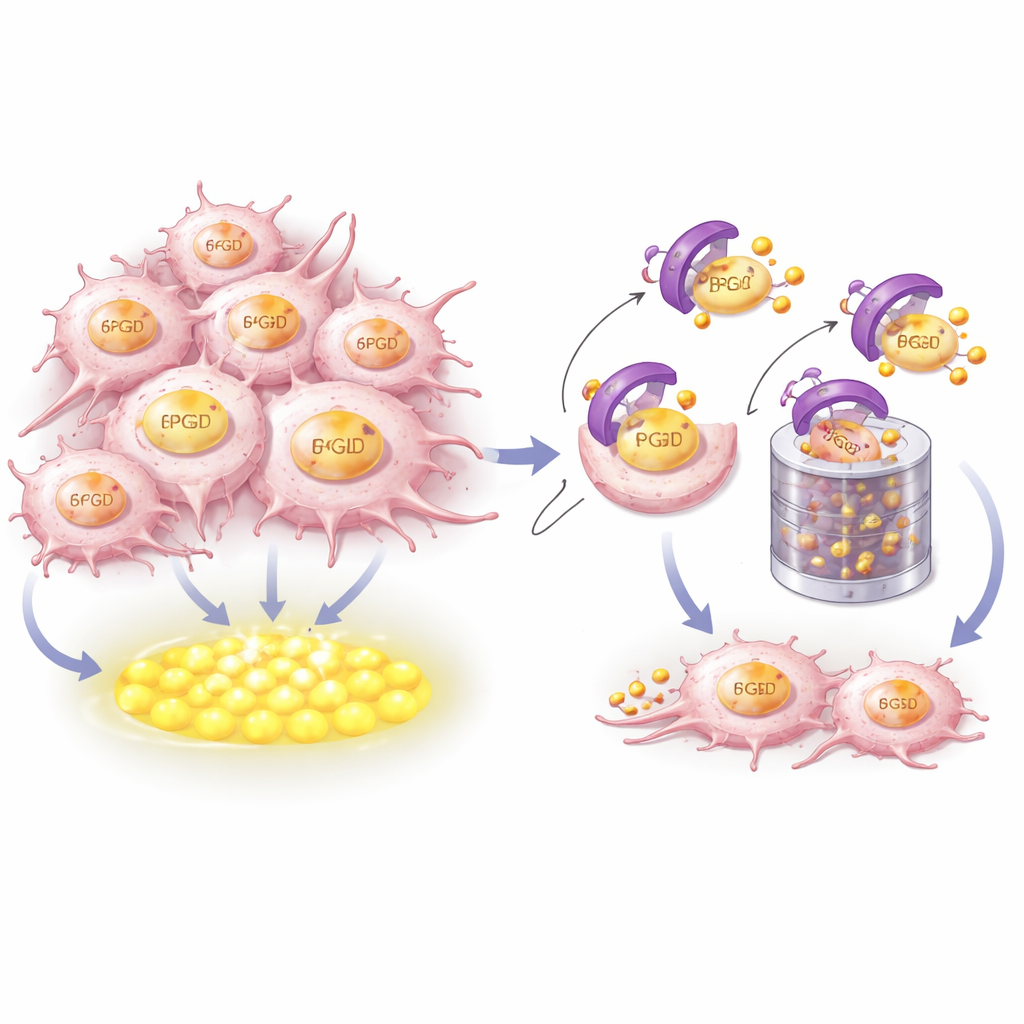
Cómo CRBN reconoce y destruye la fuente de combustible
Para entender cómo CRBN controla 6PGD, los investigadores combinaron modelado estructural con experimentos bioquímicos. Mostraron que CRBN se agarra físicamente a un segmento helicoidal corto y muy conservado cerca del extremo terminal de 6PGD. Aminoácidos clave en ambas proteínas forman una interfaz de acoplamiento ajustada. Cuando estos puntos de contacto se alteraron, CRBN ya no pudo unirse a 6PGD, agregar las pequeñas etiquetas de ubiquitina que la marcan para la eliminación ni enviarla al triturado celular conocido como proteasoma. Es notable que esta superficie de reconocimiento es distinta del bolsillo donde los fármacos inmunomoduladores se unen a CRBN, lo que significa que el control de CRBN sobre 6PGD forma parte de su función doméstica nativa y no es un efecto inducido por fármacos.
Del metabolismo alterado a células errantes
Las consecuencias de este apretón de manos molecular se reflejan en el comportamiento celular. En células de cáncer de próstata carentes de CRBN, el aumento de 6PGD y NADPH fue acompañado de mayor movilidad e invasión a través de barreras artificiales, rasgos característicos del potencial metastásico. Cuando CRBN se sobreexpresó, las células se volvieron menos móviles e invasivas, aunque su tasa de crecimiento no cambió. El perfilado de actividad génica mostró que CRBN incrementó los niveles de CDH1, asociado a células epiteliales fuertemente cohesionadas, y redujo los de MMP1, vinculado a la degradación de tejidos y migración. Importante, estos cambios requirieron la unión directa CRBN–6PGD y pudieron revertirse bloqueando la actividad enzimática de 6PGD, ligando así los cambios metabólicos con las alteraciones en el comportamiento metastásico.
Pruebas en modelos animales y otros cánceres
El equipo puso a prueba estas ideas en ratones inyectando células de cáncer de próstata en el torrente sanguíneo o en el bazo. Las células diseñadas para producir CRBN extra formaron muchos menos nódulos metastásicos en hígado y pulmones que las células control, confirmando un papel antimetastásico en animales vivos. Ratones modificados para carecer de CRBN mostraron niveles más altos de proteína 6PGD en varios órganos. Patrones similares aparecieron en líneas celulares de glioblastoma, pulmón y riñón: eliminar CRBN aumentó 6PGD y potenció el movimiento e invasión celular, mientras que la inhibición genética o farmacológica de 6PGD moderó este comportamiento agresivo. Estas observaciones sugieren que el freno CRBN–6PGD sobre la metástasis no es exclusivo del cáncer de próstata.
Qué podría significar para tratamientos futuros
En conjunto, el estudio propone que CRBN actúa como un guardián metabólico que restringe el suministro de energía necesario para que las células cancerosas se desprendan, migren y arraiguen nuevos tumores. Cuando CRBN se pierde o está bajo, 6PGD se acumula, la producción de NADPH se dispara y las células son más propensas a sufrir cambios que favorecen la metástasis. Para los pacientes, esto apunta a dos posibilidades: medir los niveles de CRBN y 6PGD podría ayudar a identificar tumores con alto riesgo metastásico, y las terapias que aumenten la función de CRBN —o que reduzcan selectivamente 6PGD en tumores con poco CRBN— podrían ofrecer nuevas vías para frenar o prevenir la diseminación del cáncer de próstata y otros cánceres.
Cita: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Palabras clave: metástasis del cáncer de próstata, metabolismo del cáncer, cereblon, enzima 6PGD, vía del NADPH