Clear Sky Science · es
L1TD1 promueve la progresión del adenocarcinoma mucinoso colorrectal al aumentar la estabilidad del ARNm de ABCC3
Por qué importa este cáncer cargado de moco
El cáncer colorrectal es una de las principales causas de muerte por cáncer en el mundo. Dentro de él, un subtipo especial llamado adenocarcinoma mucinoso destaca porque sus tumores están llenos de un moco espeso que constituye más de la mitad de la masa tumoral. Esa barrera viscosa puede ayudar a las células cancerosas a ocultarse de la quimioterapia y de las defensas del organismo. Este estudio plantea una pregunta básica pero crucial: ¿qué controla toda esa mucosidad, y podemos detenerla para frenar el cáncer y mejorar la eficacia de los tratamientos?
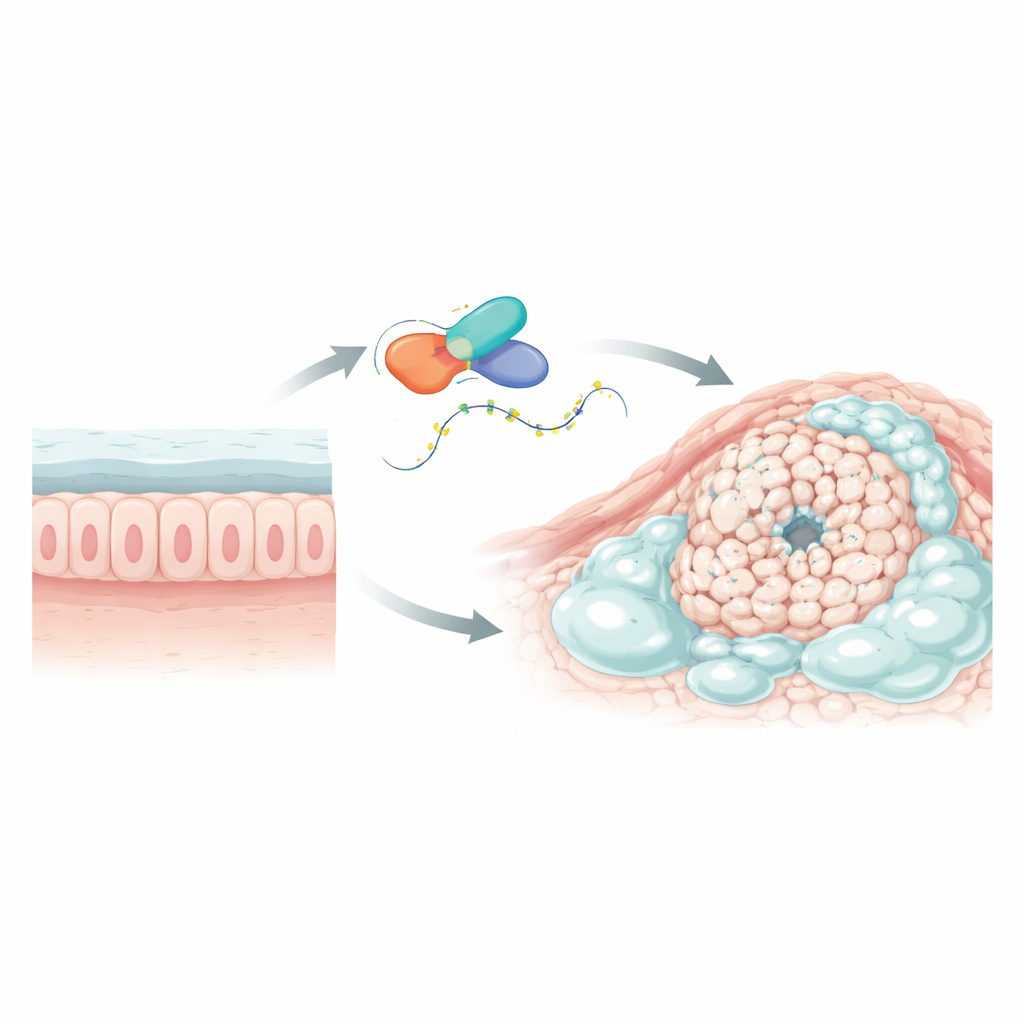
Identificando un gen clave problemático
Los investigadores empezaron buscando en grandes bases de datos de cáncer y en datos de secuenciación unicelular para localizar genes que se comportan de manera diferente en los tumores colorrectales ricos en moco en comparación con los cánceres colorrectales ordinarios y el tejido sano circundante. Un gen, llamado L1TD1, destacó claramente. Estaba marcadamente aumentado en tumores mucinosos pero no en los tumores regulares y era más alto en el tejido tumoral que en el colon normal adyacente. L1TD1 codifica una proteína que se une al ARN, la molécula que transporta los mensajes genéticos desde el ADN hasta la maquinaria celular que fabrica proteínas. Dado que las proteínas unidas al ARN pueden ajustar finamente cuánto duran los mensajes y con qué intensidad se traducen, L1TD1 fue un fuerte candidato para actuar como regulador maestro en estos cánceres cargados de moco.
Cómo L1TD1 impulsa el crecimiento y la diseminación del cáncer
Para probar qué hace realmente L1TD1, el equipo recurrió a líneas celulares de cáncer de colon y a modelos en ratón. Cuando aumentaron los niveles de L1TD1 en las células cancerosas, estas se multiplicaron más rápido, se movieron con mayor facilidad e invadieron barreras similares a tejido con más agresividad. Reducir L1TD1 tuvo el efecto opuesto, ralentizando el crecimiento y disminuyendo la invasión. En ratones inyectados con células con altos niveles de L1TD1, los tumores crecieron más y se diseminaron con mayor frecuencia al hígado y la cavidad abdominal. Los tumores con más L1TD1 también tendían a ser más grandes, menos diferenciados y a encontrarse en estadios más avanzados en los pacientes, vinculando este gen con un comportamiento clínico peor de la enfermedad.
Activando la mucosidad y la resistencia a fármacos
La mucosidad en sí resultó ser central para el impacto de L1TD1. Las células con más L1TD1 produjeron mayores cantidades de proteínas clave formadoras de moco, especialmente MUC2 y MUC5AC, y mostraron rasgos de células caliciformes, las células normales que secretan moco en el intestino. Cultivos tridimensionales y tinciones de tejido tanto de pacientes como de ratones confirmaron que niveles más altos de L1TD1 iban de la mano con un moco más espeso y abundante. Es importante que este moco no fuera solo un acompañante. Cuando los investigadores redujeron selectivamente MUC2, el aumento de crecimiento, invasión y resistencia a la quimioterapia impulsado por L1TD1 desapareció en gran medida. Las células ricas en L1TD1 fueron más difíciles de matar con el fármaco común oxaliplatino, y los tumores con estas células se redujeron menos en los ratones tratados, subrayando que el moco actúa como un escudo que L1TD1 contribuye a construir.
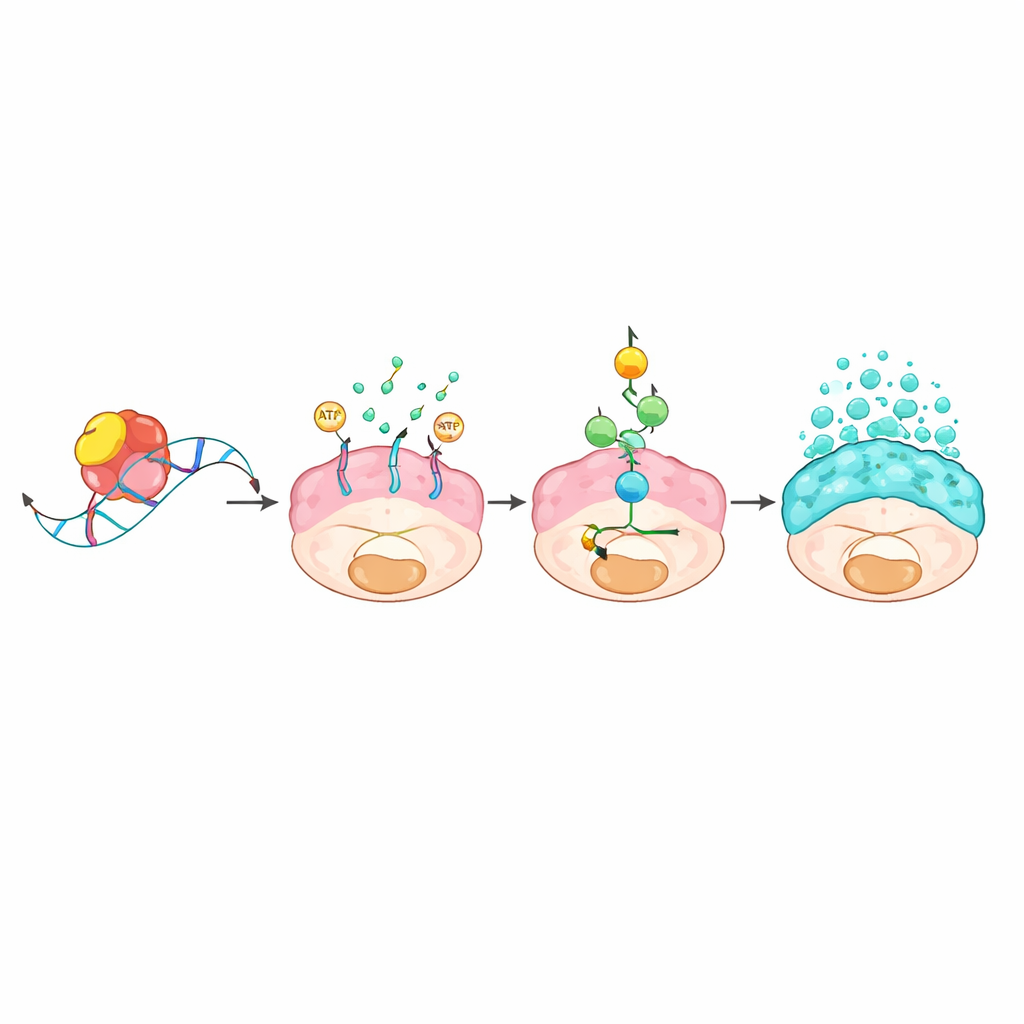
Una cadena molecular que enlaza el control del ARN con inundaciones de moco
El equipo preguntó a continuación cómo una proteína unida al ARN podía provocar cambios tan drásticos. Al capturar las moléculas de ARN unidas físicamente a L1TD1 y comparar la actividad génica con y sin L1TD1, identificaron al gen transportador ABCC3 como un objetivo principal. L1TD1 se acopla a un motivo corto “GUGU” en la cola del mensaje de ARN de ABCC3, estabilizándolo para que la célula produzca más de la proteína ABCC3, conocida como MRP3. Este transportador se localiza en la membrana celular y consume energía para expulsar sustancias fuera de la célula. El consiguiente drenaje energético activó un sistema de alarma metabólica centrado en el sensor AMPK, que a su vez activó una ruta clásica de crecimiento y respuesta al estrés conocida como MAPK. Una vez activada, esta cascada aumentó la producción y liberación de proteínas mucosas y reforzó la capacidad de las células tumorales para crecer, migrar y resistir fármacos. Bloquear ABCC3 genéticamente o con un compuesto experimental, o inhibir la vía MAPK, redujo la producción de moco y debilitó los tumores.
Qué significa esto para los pacientes
En conjunto, el trabajo revela un sistema de control por pasos para el cáncer colorrectal rico en moco: L1TD1 estabiliza el ARN de ABCC3, ABCC3 drena la energía celular, la vía AMPK–MAPK se activa y el tumor responde sobreproduciendo moco y volviéndose más agresivo y resistente a fármacos. Para los pacientes, esto sugiere varias vías prometedoras. Los niveles de L1TD1 y ABCC3 podrían ayudar a identificar tumores con mayor probabilidad de comportarse de forma más agresiva o resistir la quimioterapia estándar. Más importante aún, fármacos que interrumpan la interacción L1TD1–ABCC3, bloqueen la actividad de bombeo de MRP3 o ataquen las vías de señalización descendentes podrían adelgazar la barrera mucosa, frenar el crecimiento tumoral y aumentar la eficacia de los tratamientos existentes para esta forma desafiante de cáncer colorrectal.
Cita: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Palabras clave: cáncer colorrectal mucinoso, L1TD1, ABCC3 MRP3, producción de mucina, resistencia a quimioterapia