Clear Sky Science · es
La helicasa de ARN multifuncional DDX39A impulsa la progresión del glioblastoma modulando el splicing alternativo de WISP1 que induce una polarización inmunosupresora de macrófagos
Por qué importa este estudio sobre cáncer cerebral
El glioblastoma es uno de los cánceres cerebrales más letales, conocido por reaparecer tras el tratamiento y por su resistencia a los fármacos. Este estudio revela cómo un único “interruptor” molecular en las células tumorales no solo favorece el crecimiento del cáncer, sino que además convence a las células inmunitarias cercanas de dejar de combatir y empezar a proteger al tumor. Al trazar esta cadena de eventos, los investigadores identifican también un fármaco antipsicótico existente que podría reutilizarse para romper esta red perjudicial.
Un ayudante clave dentro de las células tumorales cerebrales
El equipo se centró en una proteína llamada DDX39A, una máquina molecular que ayuda a las células a procesar el ARN, la copia operativa de la información genética. Al analizar grandes bases de datos de pacientes y muestras tumorales, encontraron que DDX39A está mucho más activa en el glioblastoma que en el tejido cerebral normal, y sus niveles aumentan con el grado tumoral. Los análisis de célula única mostraron que DDX39A es especialmente abundante en células tumorales de rápida división y en ciertos tipos de células inmunitarias llamadas macrófagos dentro de la masa tumoral. Los pacientes cuyos tumores tenían niveles más altos de DDX39A tendieron a presentar peores resultados, lo que sugiere que esta proteína está estrechamente ligada a una enfermedad agresiva.
Cómo este ayudante alimenta el crecimiento y la diseminación
Para probar qué hace realmente DDX39A, los investigadores utilizaron herramientas genéticas para reducirlo en células tipo tronco de glioblastoma cultivadas en el laboratorio y en modelos murinos de tumores cerebrales. Cuando se disminuyó DDX39A, las células tumorales crecieron más despacio, invadieron menos el tejido circundante y tuvieron más probabilidad de sufrir muerte celular programada. Las células tumorales con características de células madre también perdieron gran parte de su capacidad para formar nuevas esferas tumorales, señal de que su capacidad de autorrenovación se vio mermada. En ratones, los tumores con DDX39A reducido eran más pequeños y los animales vivían más tiempo, confirmando que esta proteína impulsa activamente la progresión tumoral y no solo la marca de forma pasiva.
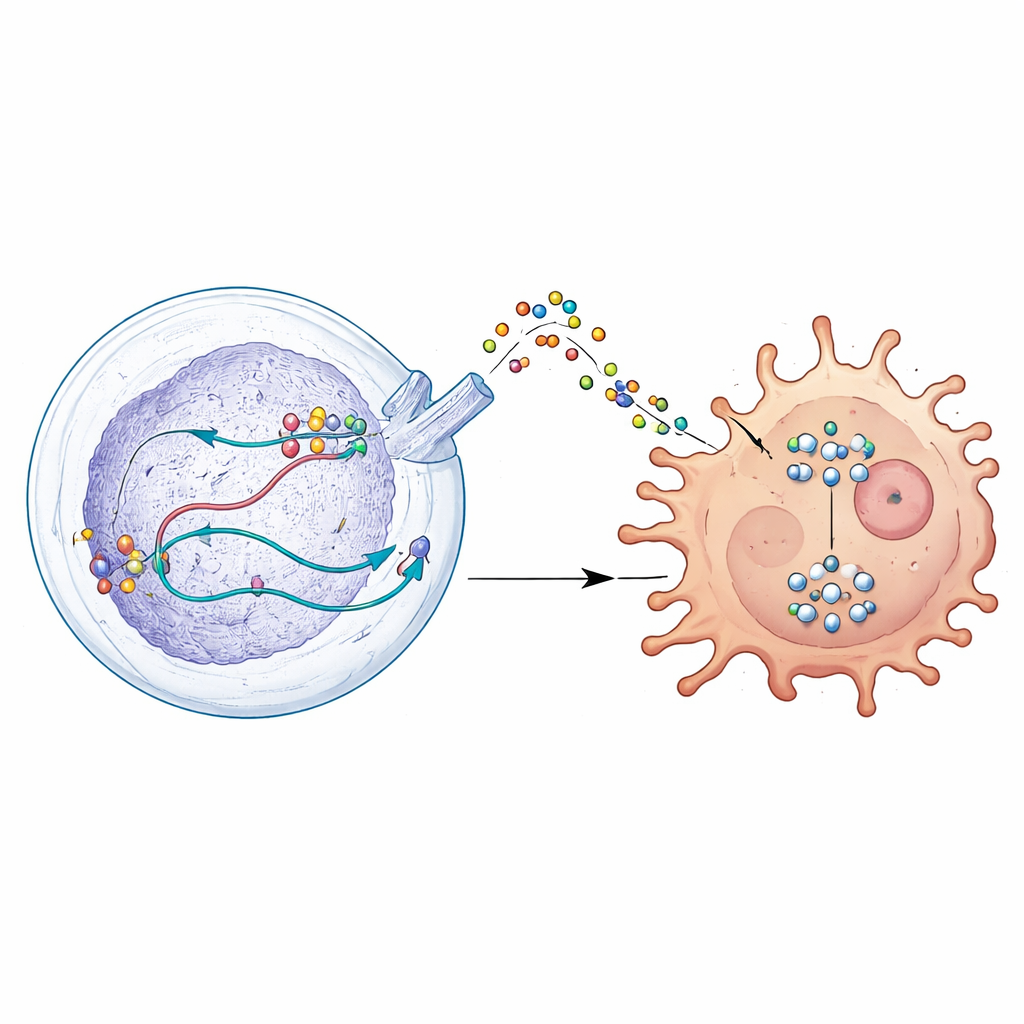
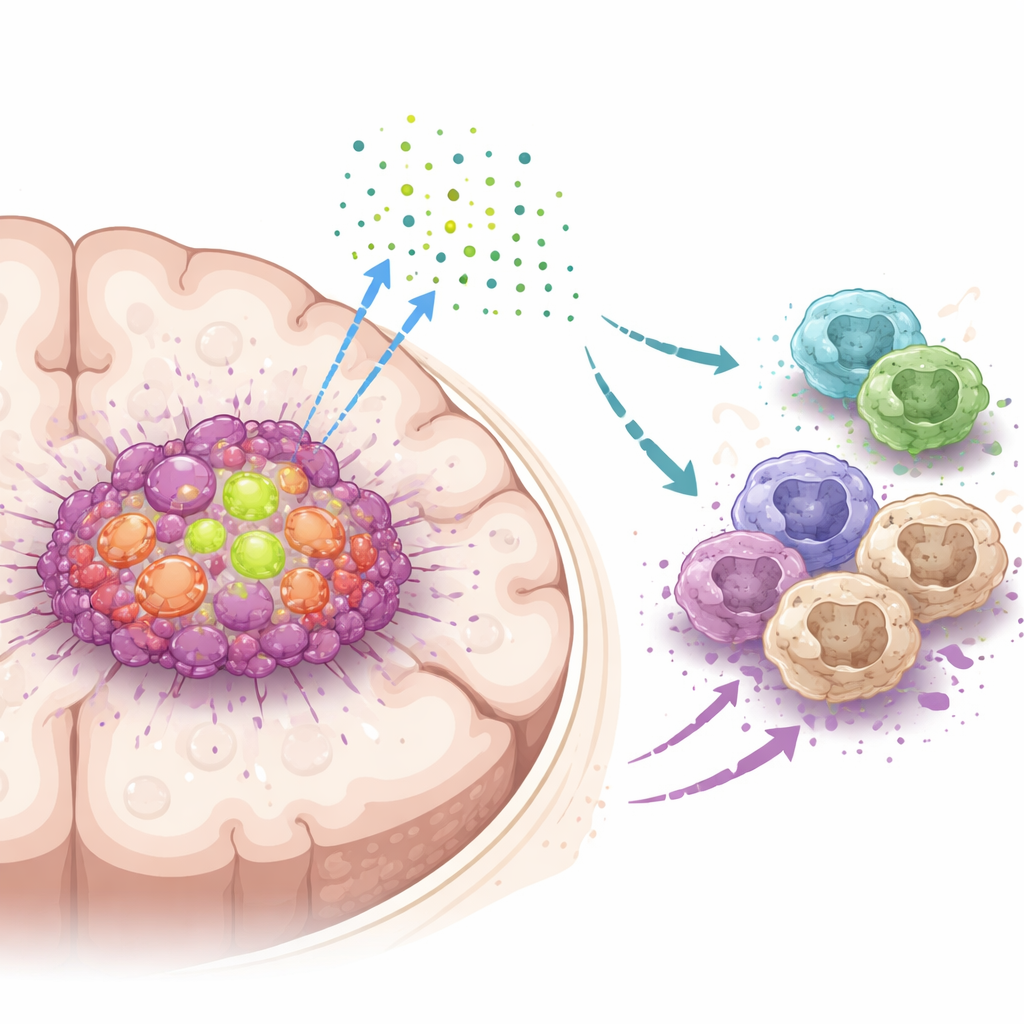
Una señal secreta que desarma a los defensores inmunitarios
Al profundizar, los científicos descubrieron que DDX39A cambia cómo se procesa un gen llamado WISP1. En lugar de limitarse a activar o desactivar WISP1, DDX39A ayuda a moldear su ARN de modo que estabiliza el mensaje y aumenta la producción de la proteína WISP1. Las células tumorales liberan entonces WISP1 a su alrededor, donde actúa como una señal engañosa. Los macrófagos cercanos, que pueden atacar a los tumores o apoyarlos, responden a esta señal cambiando hacia un estado inmunosupresor que ayuda al tumor. Este cambio se impulsa mediante la activación de una vía de control del crecimiento intracelular conocida como AKT. Cuando se redujo DDX39A o WISP1, esta vía se atenuó, las células tumorales se volvieron menos agresivas y los macrófagos regresaron hacia un perfil más orientado a combatir el tumor.
Convertir un fármaco psiquiátrico en un arma contra el cáncer
Con este mapa de la vía en mano, los investigadores buscaron en bases de datos de fármacos moléculas que pudieran interferir con la actividad de DDX39A. Se fijaron en la flufenazina, un antipsicótico de larga utilización conocido por alcanzar el cerebro. El modelado por ordenador y las pruebas de unión mostraron que la flufenazina puede unirse directamente a DDX39A. En las células tumorales, el fármaco debilitó la afinidad de DDX39A por el ARN de WISP1, redujo los niveles de WISP1 y disminuyó la señalización AKT. Las células tratadas crecieron menos, invadieron menos, formaron menos esferas tumorales y fueron más propensas a morir. En modelos murinos, la flufenazina ralentizó el crecimiento del tumor cerebral, redujo el número de macrófagos que apoyan al tumor y alargó la supervivencia, todo ello con dosis similares a las ya usadas en humanos para otras indicaciones.
Qué significa esto para el tratamiento futuro
En términos sencillos, este estudio muestra que las células de glioblastoma explotan DDX39A para afinar un mensaje (WISP1) que tanto aumenta su propia resistencia como reprograma a las células inmunitarias cercanas en guardaespaldas en lugar de soldados. Bloquear a este ayudante, ya sea genéticamente o con un fármaco como la flufenazina, debilita al cáncer en dos frentes: las propias células tumorales y el escudo protector de macrófagos inmunosupresores. Aunque se necesita mucha más investigación antes de que esta estrategia pueda aplicarse en pacientes, el trabajo abre una vía prometedora para reposicionar un medicamento conocido y atacar un punto débil recién descubierto en uno de los cánceres cerebrales más tenaces.
Cita: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Palabras clave: glioblastoma, splicing de ARN, microambiente tumoral, polarización de macrófagos, reposicionamiento de fármacos