Clear Sky Science · es
PMM2 interactúa con TRIM28 para reclutar a E2F4 y promover la glicólisis mediada por KIFC3 y la progresión del cáncer colorrectal
Por qué importa esta historia del cáncer
El cáncer colorrectal es uno de los cánceres más letales del mundo, en parte porque muchos tumores aprenden a secuestrar los sistemas energéticos del cuerpo para alimentar un crecimiento descontrolado. Este estudio revela cómo una enzima poco conocida, PMM2, ayuda a los tumores colorrectales a quemar azúcar de forma más agresiva y a diseminarse, y por qué eso la convierte en un nuevo objetivo prometedor para futuros fármacos y pruebas diagnósticas.
Un motor tumoral hambriento de azúcar
Las células cancerosas a menudo reprograman la forma en que usan la glucosa, favoreciendo una forma de quema de azúcar de alta velocidad y baja eficiencia conocida como glicólisis. Los investigadores comenzaron comparando miles de genes en muestras de tumores colorrectales con tejido sano cercano. PMM2, una enzima normalmente implicada en unir cadenas de azúcar a proteínas, destacó como uno de los genes más aumentados en el cáncer. Las células tumorales con exceso de PMM2 crecieron más rápido, formaron más colonias y se dispersaron con mayor facilidad en platos de laboratorio, mientras que las células en las que se apagó PMM2 redujeron su crecimiento, migraron menos y fueron más propensas a morir.
Cómo las células tumorales sobreactivan el uso de azúcar
Cuando el equipo redujo los niveles de PMM2 en células de cáncer colorrectal, las células captaron menos glucosa, produjeron menos ATP (su principal moneda energética) y liberaron menos lactato, el producto de desecho de la glicólisis. Mediciones metabólicas sensibles confirmaron que la acidificación global del medio circundante disminuyó, mientras que el consumo de oxígeno aumentó, lo que significa que las células se desplazaron de una glicólisis sobreacelerada hacia una respiración más normal. Proteínas clave que ayudan a la glicólisis, PKM2 y LDHA, también se redujeron. Sorprendentemente, incluso una versión catalíticamente “muerta” de PMM2 pudo seguir impulsando este comportamiento hambriento de azúcar, lo que muestra que el papel de la enzima en el cáncer no depende de su química habitual, sino de con quién se une dentro de la célula.
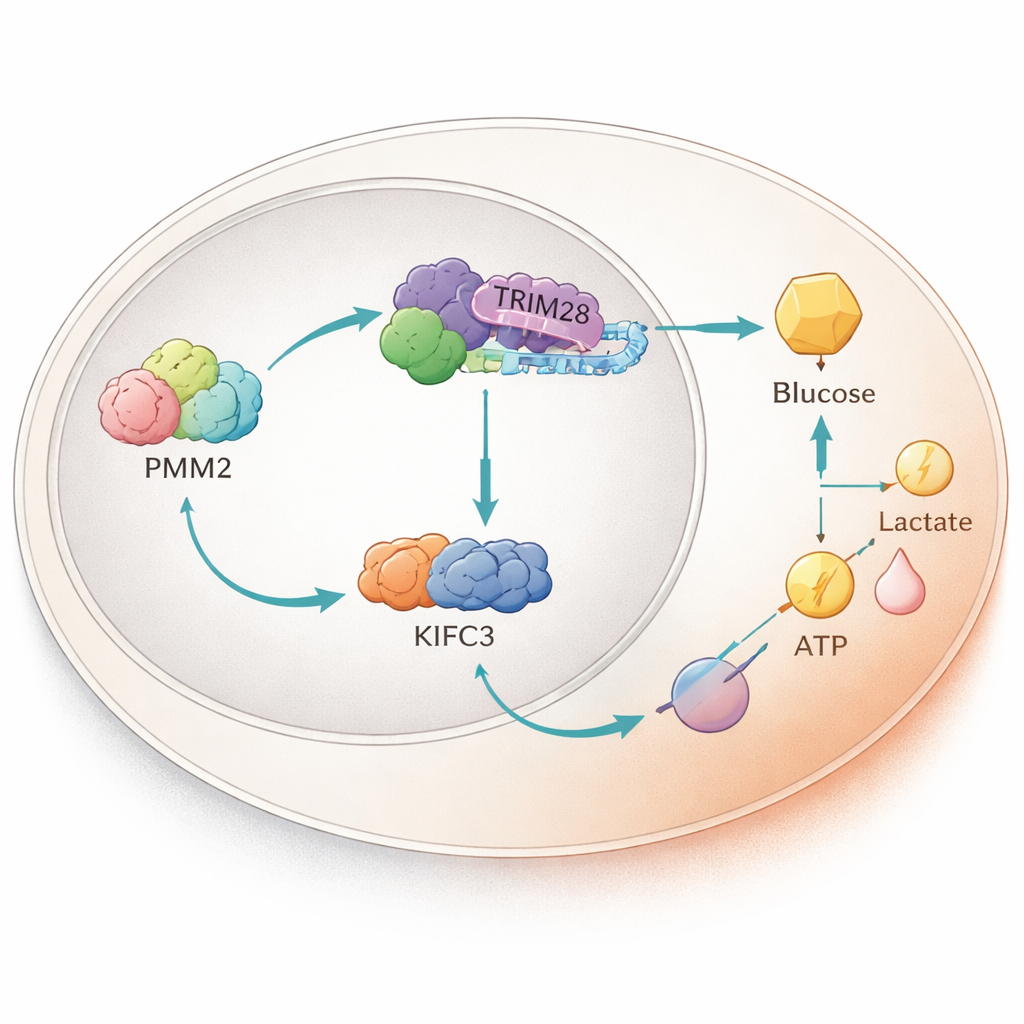
Un relevo de proteínas dentro del núcleo
Al profundizar, los científicos encontraron que PMM2 se une físicamente a otra proteína llamada TRIM28, que puede moverse al núcleo celular e influir en la actividad génica. PMM2 ayuda a que TRIM28 se acumule en el núcleo, donde TRIM28 se asocia con un factor de transcripción, E2F4. Juntos, este trío incrementa la producción de una proteína motora llamada KIFC3 al unirse a un tramo específico de la región reguladora de su ADN. Experimentos que eliminaron la región de PMM2 necesaria para la unión con TRIM28 borraron la capacidad de PMM2 de aumentar la glicólisis y el crecimiento celular, subrayando que esta asociación de proteínas—y no la función enzimática clásica de PMM2—es lo que potencia la ventaja tumoral.
Activando un interruptor metabólico clave
KIFC3, más conocido por su papel en el transporte de cargas a lo largo del andamiaje interno de la célula, resultó ser un interruptor metabólico crucial. Cuando los investigadores redujeron los niveles de KIFC3, las células de cáncer colorrectal consumieron menos glucosa, produjeron menos ATP y lactato, y mostraron una actividad glicolítica más débil, mientras que su consumo de oxígeno aumentó. Importante, silenciar KIFC3 canceló en parte el impulso glicolítico y la ventaja de crecimiento normalmente provocados por PMM2. En ratones implantados con células humanas de cáncer colorrectal, los tumores con exceso de PMM2 crecieron más, pero este efecto se atenuó cuando KIFC3 se redujo. Las muestras tumorales de estos animales mostraron niveles más altos de PMM2, KIFC3 y marcadores de glicólisis, enlazando toda la cadena de sucesos en tejido vivo.
De modelos de laboratorio a muestras de pacientes
Para acercar el trabajo a la clínica, el equipo creó pequeños tumores tridimensionales, conocidos como organoides, a partir de cánceres colorrectales de pacientes. Los organoides con niveles más altos de PMM2 y KIFC3 crecieron más rápido y produjeron más ATP y lactato que aquellos con niveles bajos. Forzar a los organoides a producir más PMM2 aumentó KIFC3 y la glicólisis, mientras que reducir PMM2 tuvo los efectos opuestos. Los análisis de matrices tumorales de pacientes mostraron además que niveles altos de PMM2 se asociaban con enfermedad más avanzada, diseminación a ganglios linfáticos y supervivencia global más corta, señalando a PMM2 como un fuerte candidato a biomarcador.
Qué significa esto para la atención futura
En términos sencillos, este estudio muestra que muchos tumores colorrectales parecen conectar a PMM2 en un relevo de proteínas nucleares—a través de TRIM28 y E2F4—para aumentar KIFC3 y, a su vez, su maquinaria de quema de azúcar. Ese aumento metabólico ayuda a los cánceres a crecer y diseminarse. Dado que esta vía depende de interacciones proteicas más que del trabajo enzimático habitual de PMM2, abre nuevas vías terapéuticas: pequeñas moléculas, péptidos o fármacos degradadores que interrumpan la unión de PMM2 a TRIM28, bloqueen el acceso de E2F4 al ADN o atenúen la actividad de KIFC3 podrían, en principio, privar a los tumores de su combustible preferido. Aunque tales tratamientos aún no están disponibles, la cadena PMM2–TRIM28–E2F4–KIFC3 destaca ahora como una hoja de ruta prometedora para estrategias más precisas y centradas en el metabolismo contra el cáncer colorrectal.
Cita: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Palabras clave: cáncer colorrectal, metabolismo tumoral, glicólisis, señalización oncogénica, biomarcador