Clear Sky Science · es
ULK1 promueve la progresión metastásica en modelos experimentales de cáncer de ovario epitelial
Por qué importa esta investigación
El cáncer de ovario epitelial suele descubrirse solo después de haberse diseminado silenciosamente por el abdomen, lo que lo convierte en uno de los cánceres más letales que afectan a las mujeres. Un paso clave en esta diseminación es la formación de pequeños grupos de células tumorales, llamados esferoides, que flotan en el líquido abdominal, resisten la quimioterapia y siembran nuevos tumores. Este estudio plantea una pregunta concreta con grandes implicaciones: ¿ayuda un “interruptor de supervivencia” celular llamado ULK1 a que estos grupos perduren y se propaguen, y podría desactivarlo abrir nuevas vías para tratar el cáncer de ovario avanzado?
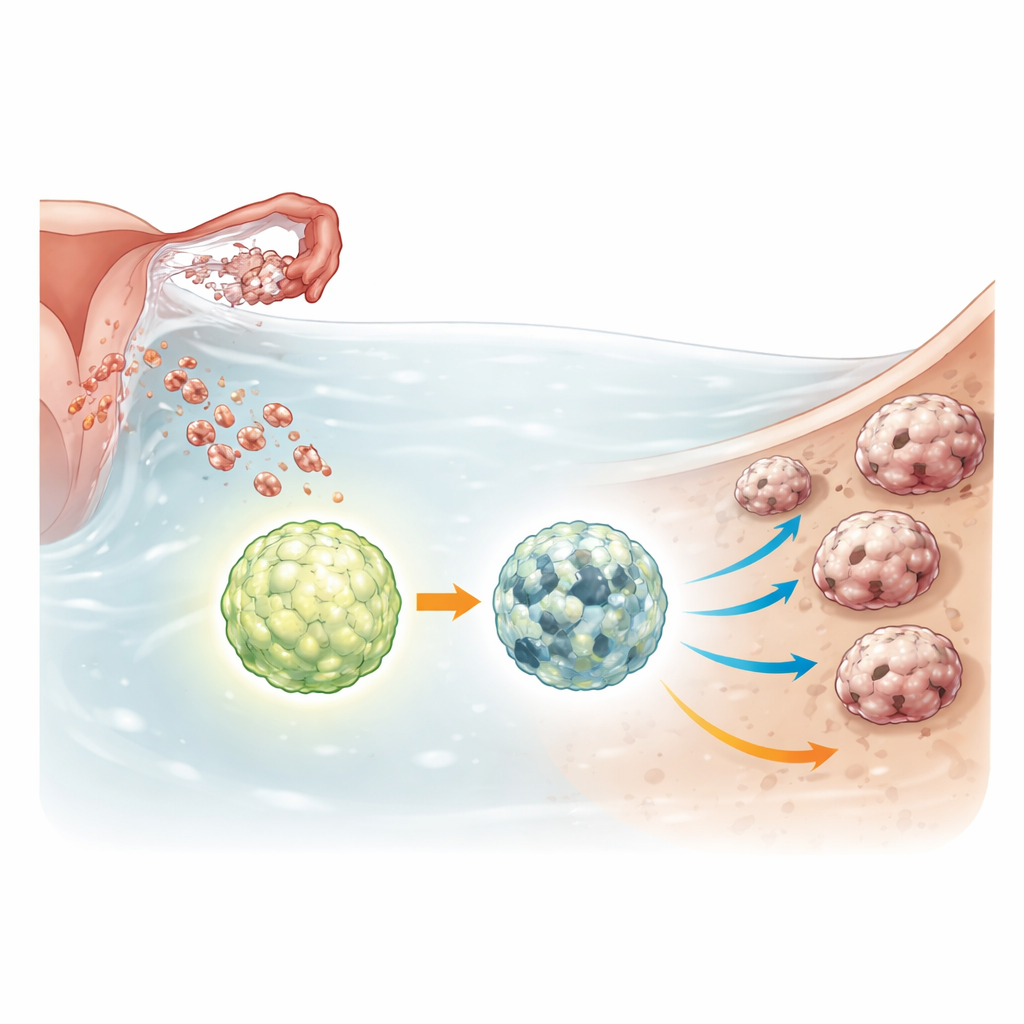
Un interruptor de supervivencia dentro de los grupos tumorales
Los esferoides de cáncer de ovario sobreviven en condiciones adversas: bajos nutrientes, falta de adhesión y exposición a quimioterapia. Para afrontarlo, aumentan un proceso de reciclaje conocido como autofagia, que descompone y reutiliza componentes internos para mantener las células vivas bajo estrés. ULK1 es un interruptor maestro que activa este sistema de reciclaje. Los investigadores utilizaron herramientas de edición genética para eliminar por completo ULK1 en varias líneas celulares de cáncer de ovario y en una línea de células no cancerosas de trompa de Falopio que representa estadios tempranos, precancerosos. Luego compararon cómo se comportaban las células normales y las carentes de ULK1 cuando se cultivaban como esferoides en suspensión o como mini-tumores tridimensionales llamados organoides.
Qué sucede cuando se apaga el interruptor
Cuando se eliminó ULK1 en las células de cáncer de ovario, su capacidad para realizar autofagia dentro de los esferoides se vio fuertemente afectada, como lo mostraron los cambios en proteínas clave del reciclaje. Estos esferoides sin ULK1 contenían menos células vivas y mostraron más señales de muerte celular programada, lo que indica que los grupos cancerosos ya no resistían las condiciones de estrés con la misma eficacia. De forma interesante, eliminar ULK1 en las células precursoras no cancerosas no cerró su sistema de reciclaje en la misma medida, lo que sugiere que las células cancerosas dependen más de ULK1 que sus contrapartes sanas. Esta dependencia específica del cáncer convierte a ULK1 en un objetivo terapéutico atractivo.
Ralentizar la diseminación y debilitar los puestos tumorales
Más allá de la supervivencia en suspensión, los esferoides deben adherirse e invadir el revestimiento liso de la cavidad abdominal para formar nuevos tumores. Usando modelos de laboratorio que imitan este paso temprano de la metástasis, el equipo mostró que los esferoides deficientes en ULK1 eran claramente peores para desplazar e invadir una capa de células mesoteliales, que normalmente recubren los órganos abdominales. Cuando se cultivaron como organoides incrustados en una matriz tipo gel, las células cancerosas sin ULK1 también formaron estructuras tumorales más pequeñas y menos robustas. En modelos de ratón donde se inyectaron células humanas de cáncer de ovario en la cavidad abdominal, la pérdida de ULK1 condujo a menos depósitos tumorales y menor acumulación de líquido, ambos signos de enfermedad avanzada, aunque la supervivencia general de los animales no mejoró.
Debilitar señales clave y potenciar el efecto de fármacos dirigidos
Para entender cómo ULK1 apoya al cáncer más allá del reciclaje, los investigadores cartografiaron cambios proteicos en esferoides sin ULK1. Encontraron que rutas mayores de crecimiento y supervivencia dentro de la célula—especialmente las vías MEK–MAPK y PI3K–AKT–mTOR—se veían alteradas. Estas vías normalmente ayudan a las células cancerosas a resistir la muerte y seguir dividiéndose. Cuando el equipo trató esferoides deficientes en ULK1 con fármacos que bloquean MEK o mTOR, los grupos cancerosos se volvieron mucho más vulnerables, con una viabilidad y capacidad de re-adherencia marcadamente reducidas. En contraste, eliminar ULK1 no mejoró la eficacia de fármacos quimioterapéuticos estándar como carboplatino, paclitaxel o del inhibidor de PARP olaparib, y en algunas condiciones pareció atenuar su beneficio.
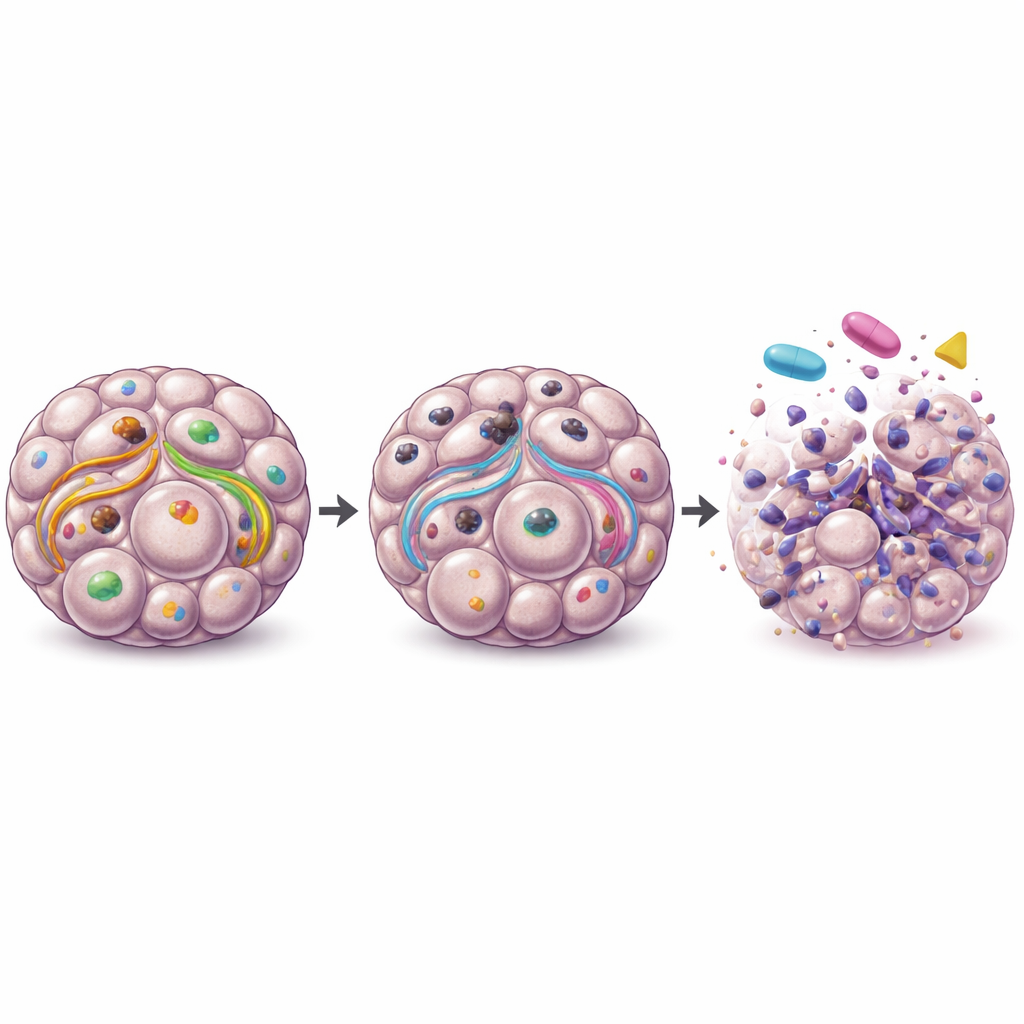
Pistas desde tumores de pacientes y modelos miniatura de paciente
Al observar grandes bases de datos públicas de tumores ováricos, los autores encontraron que una mayor actividad del gen ULK1 se asociaba con peor supervivencia a largo plazo y estaba especialmente elevada en muestras metastásicas en comparación con tumores primarios y tejido normal. Para acercarse a la clínica, probaron una pastilla clínica bloqueadora de ULK1, DCC-3116, en organoides derivados de pacientes obtenidos de muestras tumorales metastásicas. En un subconjunto de estos modelos de paciente, bloquear ULK1 por sí solo, o usar fármacos contra MEK o mTOR por separado, redujo la supervivencia de los organoides, aunque la combinación de los agentes no añadió de forma consistente un beneficio adicional. Otros organoides de pacientes fueron resistentes a todos los tratamientos, lo que subraya la diversidad del cáncer de ovario y la necesidad de biomarcadores para identificar quién podría beneficiarse.
Qué significa esto para la atención futura
En conjunto, los hallazgos presentan a ULK1 como un ayudante central en la diseminación del cáncer de ovario: impulsa el reciclaje interno que mantiene vivos a los esferoides, sostiene su capacidad de invadir nuevos sitios y ayuda a mantener potentes señales de crecimiento. Apagar ULK1 debilita estos procesos, reduce los tumores experimentales y hace que los grupos de células cancerosas sean más sensibles a ciertos fármacos dirigidos, aunque no a la quimioterapia estándar. Para los pacientes, este trabajo sugiere que ULK1 podría incorporarse a una estrategia de medicina de precisión—especialmente para quienes tienen enfermedad metastásica con alta expresión de ULK1—donde inhibidores dirigidos de ULK1 se combinan con bloqueadores de MEK o mTOR para limitar el crecimiento y la diseminación tumoral, siempre que pruebas cuidadosas puedan identificar los tumores con mayor probabilidad de responder.
Cita: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Palabras clave: cáncer de ovario, metástasis, autofagia, ULK1, terapia dirigida