Clear Sky Science · es
Asociación entre retinoides, receptores de ácido retinoico y epigenética en el cáncer de mama
Por qué la vitamina A importa en el cáncer de mama
La mayoría de la gente conoce la vitamina A como un nutriente importante para la visión, pero su forma activa en el organismo, el ácido retinoico, también ayuda a las células a decidir si deben crecer, especializarse o autodestruirse cuando están dañadas. Este artículo de revisión examina cómo el ácido retinoico y sus “puertos de acoplamiento” celulares se alteran en el cáncer de mama, por qué resultados prometedores en el laboratorio aún no se han traducido en fármacos efectivos para los pacientes, y cómo nuevos hallazgos sobre el “software” de la célula cancerosa —su código epigenético— pueden reactivar esta estrategia terapéutica.
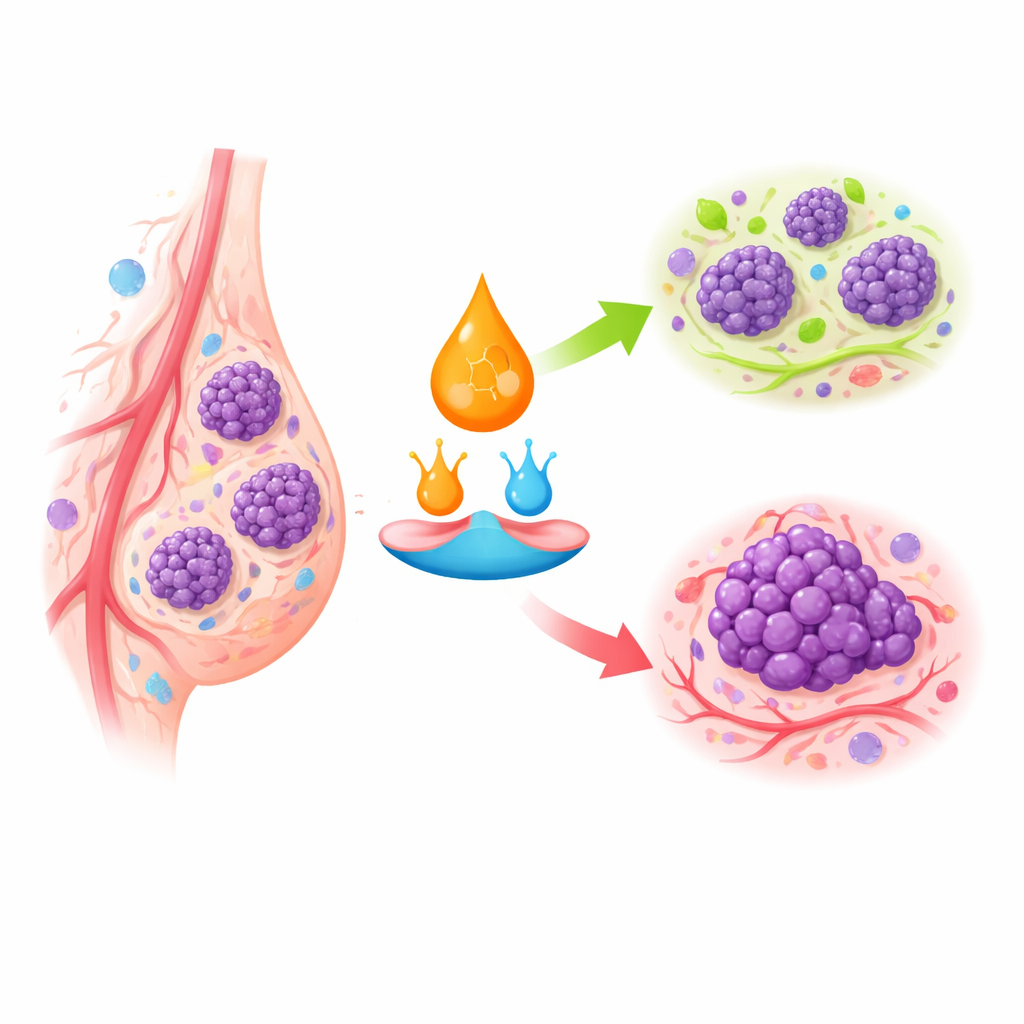
Semáforos celulares para el crecimiento y la autodestrucción
El ácido retinoico actúa uniéndose a receptores específicos dentro de las células, que a su vez activan o desactivan conjuntos enteros de genes. En el tejido mamario sano, este sistema fomenta que las células dejen de dividirse, maduren hacia formas estables o mueran si se vuelven anormales. En el cáncer de mama, especialmente en los subtipos más agresivos, receptores clave están ausentes o silenciados, y el transporte interno del ácido retinoico se redirige. En lugar de entregarse a receptores que frenan el crecimiento, puede desviarse hacia vías que favorecen la supervivencia y la proliferación. Esto ayuda a explicar por qué algunos tumores mamarios apenas responden a fármacos retinoides aunque esos mismos fármacos son muy efectivos en ciertos cánceres hematológicos.
Interruptores ocultos en el software de la célula cancerosa
Los autores se centran en la epigenética —marcas químicas en el ADN y sus proteínas de empaquetamiento que actúan como ajustes del software del genoma. En muchos cánceres de mama, estas marcas bloquean receptores importantes del ácido retinoico, en especial uno llamado RARβ2, en una posición de “apagado” sin alterar la secuencia de ADN subyacente. Grupos metilo adicionales en el ADN y el apretamiento de la «bobina» proteica cierran este receptor, mientras que otras enzimas remodelan el paisaje de la cromatina para favorecer el crecimiento y la migración. Los ARN no codificantes, que no producen proteínas pero influyen en la actividad génica, desvían aún más la señalización lejos de la muerte celular y la diferenciación. En conjunto, estos cambios dan a las células cancerosas la flexibilidad necesaria para resistir el tratamiento y adaptarse al estrés.
Reconfigurar las vías de señalización
Es importante que estos candados epigenéticos son reversibles. En modelos de laboratorio, fármacos que eliminan la metilación del ADN o aflojan la cromatina pueden restaurar RARβ2 y otros componentes de la vía del ácido retinoico. Cuando se combinan con el propio ácido retinoico y la quimioterapia estándar, estos agentes de “preparación” reducen los tumores de forma más eficaz y disminuyen la reserva de células con rasgos de progenitor que se cree alimentan las recaídas. También importa cómo se transporta el ácido retinoico dentro de la célula: una proteína portadora lo dirige hacia receptores supresores del crecimiento, mientras que otra lo entrega a vías promotoras del crecimiento. Ajustar el equilibrio entre estos transportadores puede convertir al ácido retinoico de un efecto parecido a un fertilizante en uno parecido a un freno.
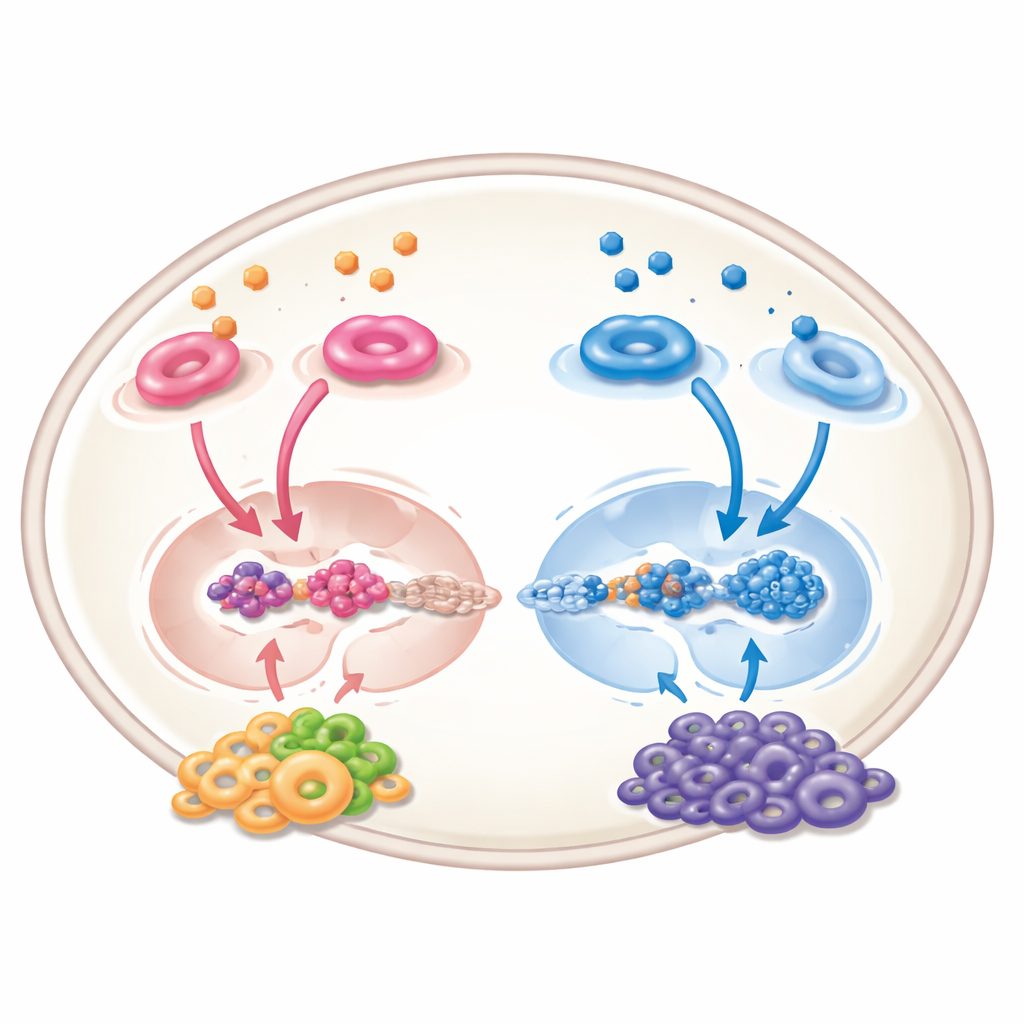
Más allá del tumor: el efecto del vecindario
El ácido retinoico no actúa solo sobre las células cancerosas; también remodela el “vecindario” que rodea al tumor —vasos sanguíneos, células inmunitarias y células de soporte. En sistemas experimentales puede reducir la formación de nuevos vasos, impulsar a las células inmunitarias hacia un estado más activo y antitumoral, y limitar las células supresoras que normalmente amortiguan las defensas del organismo. Sin embargo, la historia no es completamente positiva: en ciertos tipos de estroma que rodean el tumor, la activación de la señalización del ácido retinoico puede en realidad favorecer el crecimiento tumoral reforzando canales de comunicación química que atraen y sostienen a las células malignas. Estos efectos opuestos implican que cualquier terapia futura debe ajustarse con precisión para golpear a los tipos celulares correctos de la forma adecuada.
Diseñar ensayos más inteligentes para el futuro
Los primeros ensayos clínicos con fármacos retinoides en cáncer de mama fracasaron en buena medida, pero se llevaron a cabo antes del conocimiento actual sobre subtipos, biomarcadores y farmacología compleja. Los autores sostienen que los nuevos ensayos deberían seleccionar pacientes cuyos tumores muestren las características moleculares de sensibilidad a los retinoides, como la conservación de la expresión de receptores o patrones específicos de metilación del ADN, y deberían combinar retinoides con fármacos que desbloqueen los bloqueos epigenéticos, ataquen vías de crecimiento o potencien la respuesta inmune. Formulaciones mejoradas que mantengan niveles estables del fármaco en el organismo, junto con un seguimiento estrecho tanto del tumor como del tejido circundante, serán cruciales. Si se superan estos obstáculos, los tratamientos basados en ácido retinoico podrían todavía encontrar un lugar como herramientas de precisión contra formas seleccionadas de cáncer de mama.
Cita: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Palabras clave: ácido retinoico, cáncer de mama, epigenética, terapia de diferenciación, microambiente tumoral