Clear Sky Science · es
Modelización del diálogo entre tejido adiposo y cáncer: una perspectiva tridimensional
Por qué la grasa y el cáncer están más cerca de lo que crees
La mayoría de nosotros pensamos en la grasa corporal como un acolchado extra o energía almacenada, pero la investigación revela ahora que es un órgano activo y comunicativo que puede moldear nuestra salud de maneras sorprendentes. Este artículo de revisión explora cómo se comunican el tejido adiposo y las células cancerosas, y cómo nuevos modelos de laboratorio tridimensionales (3D) ayudan a los científicos a reproducir ese diálogo con más realismo que nunca. Comprender esta conversación oculta podría mejorar la prevención del cáncer, las pruebas de fármacos y los tratamientos, especialmente en un mundo cada vez más con sobrepeso. 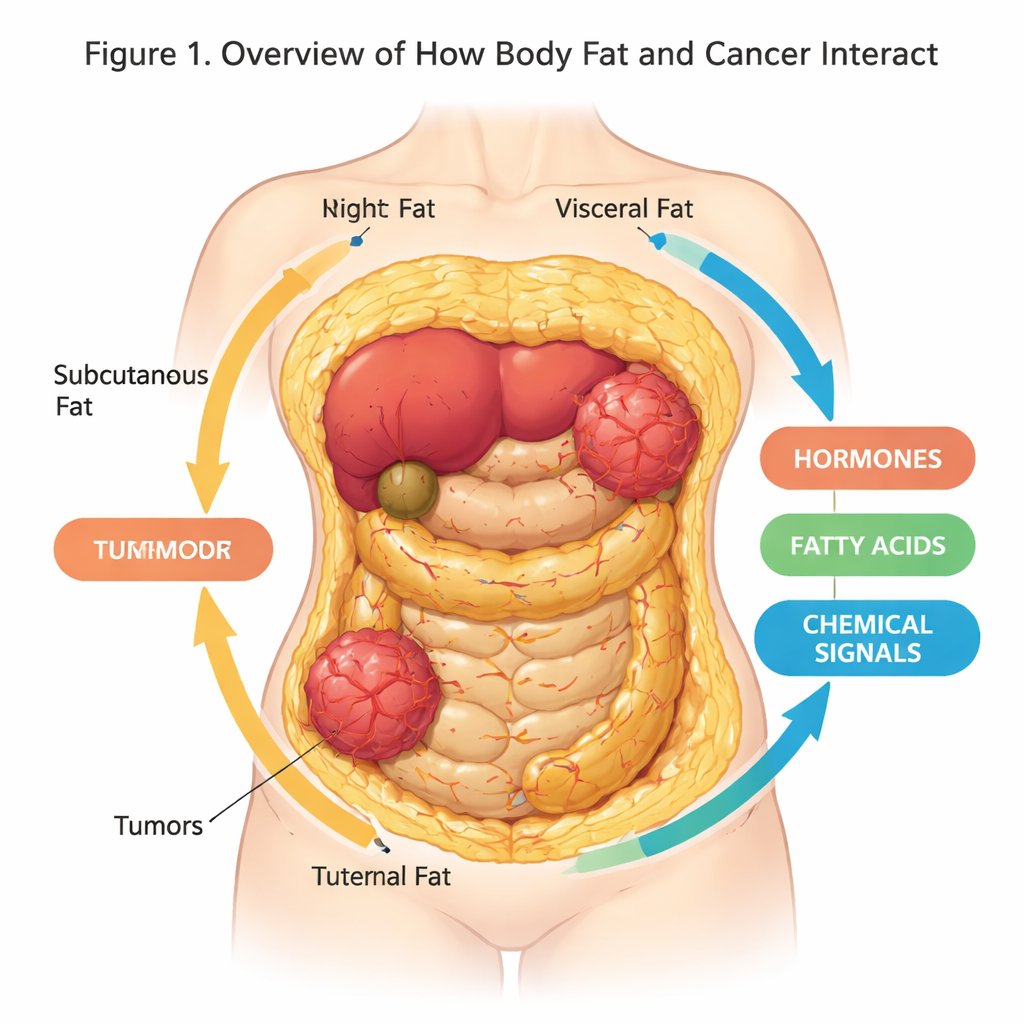
La grasa como un órgano vivo y comunicativo
El tejido adiposo—nuestra grasa corporal—no es solo un depósito pasivo. Es un órgano complejo formado por adipocitos, células inmunitarias, vasos sanguíneos y células de soporte, todos integrados en una red estructural conocida como matriz extracelular. Existen distintos tipos de grasa en diferentes lugares: grasa subcutánea bajo la piel, grasa visceral alrededor de los órganos internos, y adipocitos blancos, marrones y beige que difieren en cómo almacenan energía o la queman en forma de calor. Estas células liberan constantemente un cóctel de hormonas, ácidos grasos y proteínas señalizadoras que influyen en el metabolismo, la inflamación y, como sabemos ahora, el riesgo y el comportamiento del cáncer.
Obesidad, inflamación y riesgo de cáncer
Cuando ganamos demasiado peso, los adipocitos blancos aumentan de tamaño y número y el tejido se estresa e inflama. Esta grasa “no saludable” libera más moléculas inflamatorias y ácidos grasos a la circulación, al tiempo que maneja el azúcar y las grasas con menos eficiencia. Grandes estudios epidemiológicos han vinculado la obesidad con un mayor riesgo y peores resultados en muchos cánceres, incluidos el de mama, colon, páncreas y útero. La revisión explica cómo la grasa disfuncional puede alimentar a los tumores con combustible adicional, endurecer el tejido circundante y reclutar otros tipos celulares que, en conjunto, crean un entorno más favorable al cáncer.
Una conversación bidireccional entre la grasa y los tumores
Hoy se considera el cáncer como una enfermedad de todo un ecosistema, no solo de células fuera de control. Las células tumorales aprovechan la grasa cercana para obtener apoyo, reprogramando adipocitos, células inmunitarias y fibroblastos para que les ayuden a crecer y diseminarse. A cambio, los adipocitos responden degradando lípidos almacenados y liberando ácidos grasos y hormonas que las células cancerosas pueden utilizar fácilmente. Este diálogo puede ocurrir a distancia mediante señales circulantes, o localmente donde los tumores crecen junto a la grasa, como en la mama o el abdomen. Las células tumorales incluso pueden impulsar a los adipocitos a perder su identidad original y transformarse en células más parecidas a formadoras de cicatriz o con rasgos inmunes que remodelan el tejido y favorecen la invasión. 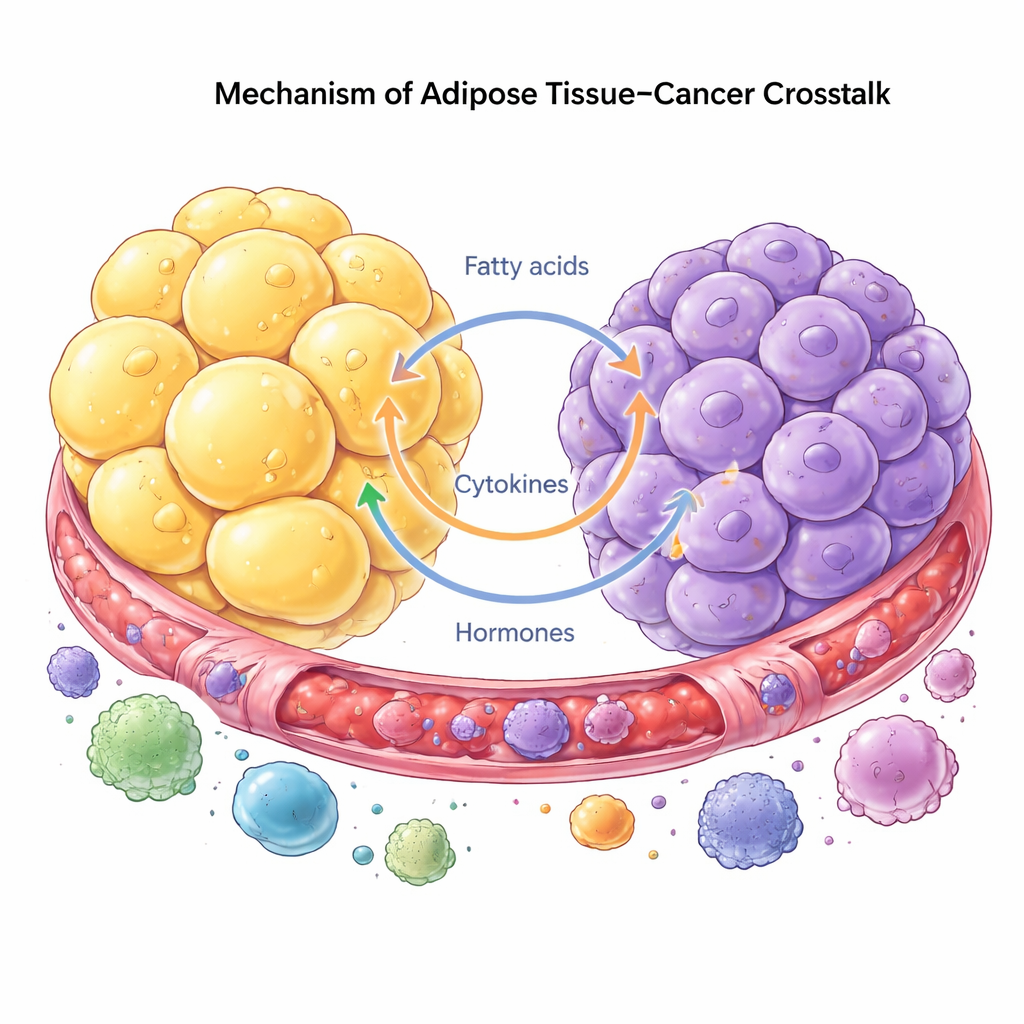
Construir mini tejidos en 3D
Los cultivos celulares tradicionales en plano (2D) y los modelos animales a menudo no capturan estas interacciones complejas. Los autores describen una nueva generación de sistemas 3D que se parecen más al tejido real. Los esferoides son agregados celulares simples que se autoensamblan en pequeñas esferas; los andamiajes son materiales diseñados que proporcionan un soporte 3D para el crecimiento celular; los organoides son versiones en miniatura y autoorganizadas de tejidos; y los assembloides combinan múltiples organoides o esferoides en “mini-órganos” compuestos. Los investigadores están usando ahora estos enfoques 3D para cocultivar adipocitos y células cancerosas, estudiar cómo condiciones similares a la obesidad alteran su comportamiento y probar cómo los fármacos podrían interrumpir el diálogo perjudicial entre ellos.
Promesas y lagunas actuales
Cada modelo ofrece compensaciones. Los esferoides son económicos y de alto rendimiento, pero relativamente simples. Los andamiajes permiten controlar cuidadosamente propiedades físicas como la rigidez, que puede influir en la diseminación tumoral, pero son más exigentes técnicamente. Los organoides y assembloides capturan el mayor nivel de realismo, con múltiples tipos celulares interactuando, sin embargo son costosos, difíciles de estandarizar y a menudo carecen de redes vasculares completas o de componentes inmunitarios. La revisión enfatiza que los sistemas actuales aún no reproducen a la perfección el tejido adiposo y tumoral humano, especialmente en la replicación completa de la matriz extracelular, adipocitos maduros y la participación de células inmunes.
Hacia dónde se dirige esta investigación
Los autores concluyen que mejorar los modelos 3D de las interacciones grasa–cáncer es esencial para unas pruebas de fármacos más precisas y para descubrir cómo la obesidad promueve el cáncer. A medida que estos “mini-tejidos” se vuelvan más realistas—combinando grasa, células tumorales, vasos sanguíneos y células inmunitarias verosímiles—podrían ayudar a los investigadores a predecir qué tratamientos funcionarán en pacientes concretos, diseñar mejores estrategias para bloquear el uso de la grasa corporal como combustible por parte del cáncer y, en última instancia, orientar terapias que no solo ataquen los tumores, sino los entornos no saludables que los ayudan a prosperar.
Cita: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Palabras clave: tejido adiposo, obesidad, microambiente tumoral, cultivo celular 3D, metabolismo tumoral