Clear Sky Science · es
POM121 O-GlcNAcilación facilita la metástasis ósea en el cáncer de pulmón no microcítico mediante una mayor importación nuclear de c-MYC y la reprogramación de la matriz extracelular
Por qué importa esta investigación
Cuando el cáncer de pulmón se disemina a los huesos, provoca dolor intenso, fracturas y una supervivencia mucho más corta, y aun así los médicos disponen de pocas herramientas para detener este paso letal. Este estudio examina los mecanismos internos de las células del cáncer de pulmón para revelar cómo algunas de ellas adquieren una ventaja especial que les permite viajar desde el pulmón hasta el hueso y prosperar allí. Al rastrear este proceso hasta pequeños cambios en una sola proteína portera situada en el borde del núcleo celular, los autores identifican una nueva cadena de acontecimientos que podría dirigirse para predecir, prevenir o tratar mejor las metástasis óseas en pacientes con cáncer de pulmón no microcítico.
Una etiqueta azucarada que cambia el comportamiento del cáncer
Los investigadores se centraron en modificaciones postraduccionales, pequeños cambios químicos que las proteínas adquieren después de ser sintetizadas. Una de esas modificaciones, llamada O-GlcNAcilación, consiste en la unión de un pequeño azúcar a puntos específicos de las proteínas. Usando líneas celulares de cáncer de pulmón y modelos en ratón, el equipo comparó células tumorales ordinarias con subpoblaciones seleccionadas repetidamente por su capacidad para colonizar el hueso. Encontraron que estas células buscadoras de hueso tenían niveles globales de O-GlcNAcilación mucho más altos, impulsados por una mayor actividad de la enzima OGT, que instala la etiqueta azucarada. Entre cientos de proteínas modificadas, una destacó: POM121, un componente central del poro nuclear, la estructura que controla el tráfico dentro y fuera del núcleo celular.
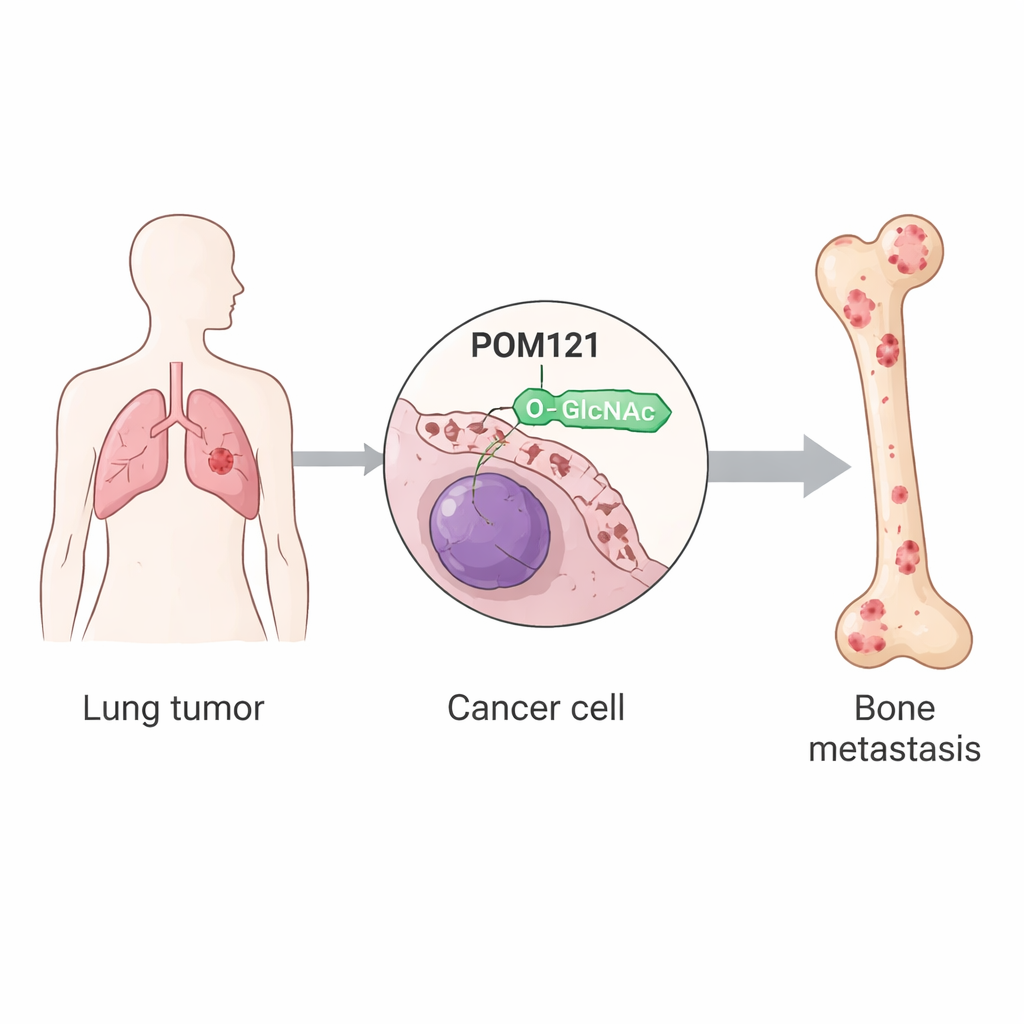
El vigilante nuclear POM121 se estabiliza
POM121 se sitúa en la membrana que rodea el núcleo, formando parte del canal por el que deben pasar muchas proteínas señalizadoras. En las células de cáncer de pulmón metastásicas al hueso, POM121 presentaba una carga elevada de O-GlcNAc en una única posición de aminoácido denominada serina 199. Cuando este sitio se modificó para que ya no pudiera ser alterado, la proteína se volvió inestable y fue rápidamente degradada por la maquinaria de eliminación de la célula. El estudio muestra que la etiqueta azucarada protege a POM121 de ser marcada para destrucción por una enzima llamada TRIM21, que normalmente añade etiquetas de ubiquitina de “eliminación”. Con la O-GlcNAc presente, TRIM21 no puede unirse bien, la ubiquitinación disminuye y POM121 se acumula en el poro nuclear sin cambiar su localización.
Abrir la puerta a un potente impulsor del cáncer
¿Qué diferencia hace tener POM121 más estable? La clave está en una conocida proteína promotora del cáncer, el factor de transcripción c-MYC. c-MYC debe entrar en el núcleo para activar genes, pero su paso depende de componentes del poro nuclear como POM121. Los autores mostraron que cuando POM121 era abundante y O-GlcNAcilado, se encontraba más c-MYC dentro del núcleo; cuando los niveles de POM121 se redujeron o se eliminó su etiqueta azucarada, la importación nuclear de c-MYC cayó drásticamente. En ratones, las células de cáncer de pulmón que portaban la mutación de POM121 no modificable formaron muchas menos y más pequeñas metástasis óseas, mientras que restaurar c-MYC en células deficientes en POM121 recuperó gran parte de su capacidad de colonizar el hueso. Esto sitúa a POM121 aguas arriba de c-MYC en una vía metastásica crítica.
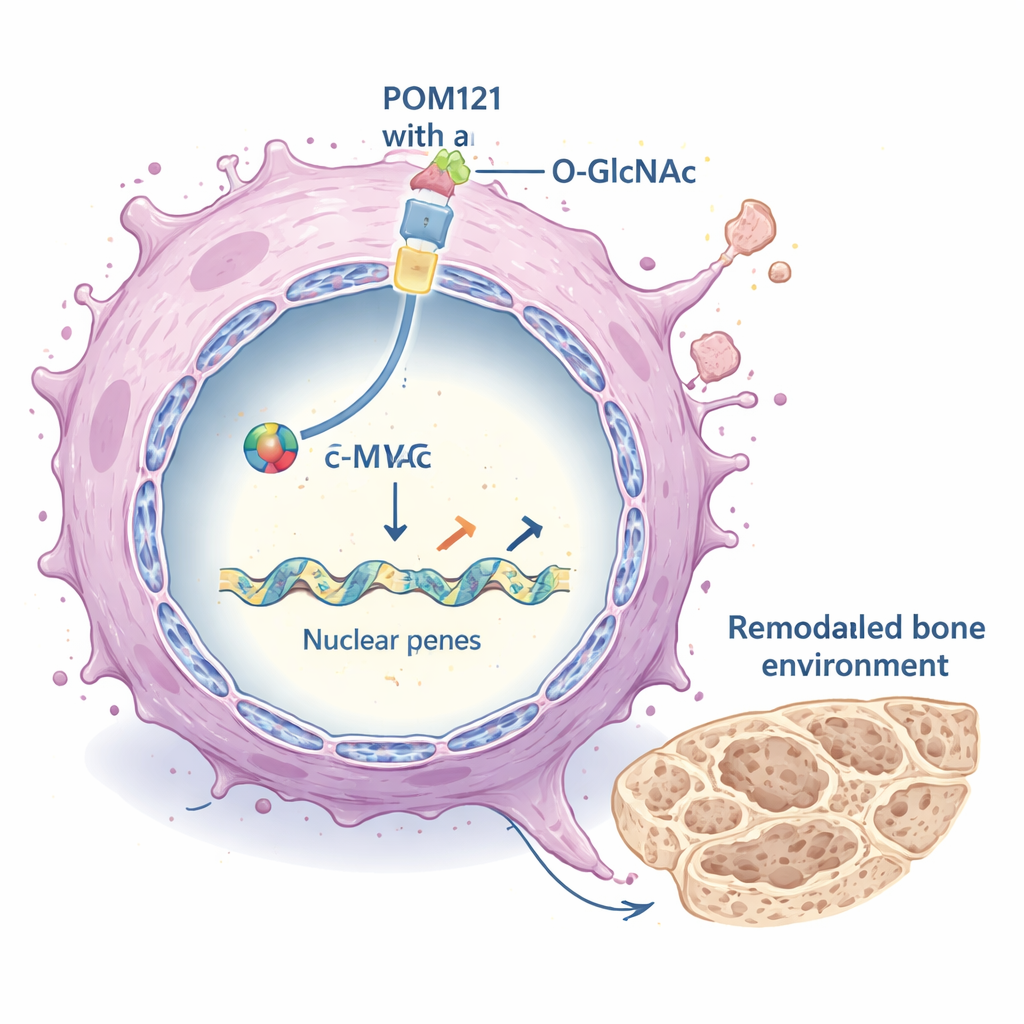
Reconfigurar el entorno del tumor
Una vez dentro del núcleo, c-MYC actúa como un interruptor maestro para muchos genes. Aquí se observó que activaba con fuerza un conjunto de genes que moldean la matriz extracelular (MEC), el andamiaje de proteínas que rodea a las células. Estos genes de la MEC, que incluyen varios colágenos y enzimas que remodelan la estructura tisular, se suprimieron cuando POM121 o c-MYC fueron bloqueados, y se activaron cuando la O-GlcNAcilación y POM121 eran altos. La MEC alterada, a su vez, potenció importantes vías de crecimiento dentro de las células cancerosas, notablemente la cascada de señalización PI3K–AKT–mTOR, que favorece la supervivencia, el crecimiento y la diseminación. Patrones similares aparecieron en varios modelos diferentes de cáncer de pulmón, lo que sugiere que este mecanismo no se limita a una sola línea celular.
Del descubrimiento de laboratorio al impacto en pacientes
Al analizar datos de pacientes, los investigadores encontraron que niveles elevados de OGT, POM121 y c-MYC, así como de los genes de la MEC que regulan, se asociaban con peores resultados y con tumores pulmonares que ya se habían diseminado al hueso. En conjunto, el trabajo describe un eje OGT–POM121–c-MYC–MEC: una mayor O-GlcNAcilación estabiliza al portero nuclear POM121, que transporta más c-MYC al núcleo, lo que a su vez reconfigura el andamiaje tisular y las señales de crecimiento para favorecer la metástasis ósea. Para los pacientes, esto sugiere nuevos tipos de biomarcadores que permitan identificar a quienes están en riesgo de diseminación ósea, y nuevas dianas terapéuticas —desde bloquear la función de OGT o POM121 hasta atenuar a c-MYC o la remodelación de la MEC— que podrían algún día ayudar a impedir que el cáncer de pulmón llegue al esqueleto.
Cita: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Palabras clave: metástasis ósea cáncer de pulmón, POM121, O-GlcNAcilación, c-MYC, matriz extracelular