Clear Sky Science · es
Sortilina exhibe una actividad similar a la de un supresor tumoral al limitar la función de transducción de EGFR
Por qué esto importa para el tratamiento del cáncer
El cáncer de pulmón es la principal causa de muertes por cáncer en todo el mundo, y muchos fármacos modernos se dirigen a una molécula llamada EGFR que impulsa el crecimiento tumoral. Estos medicamentos suelen funcionar bien al principio, pero los tumores con frecuencia desarrollan resistencia. Este estudio descubre un "freno" natural dentro de las células de cáncer de pulmón: un papel inesperado de una proteína llamada sortilina que puede atenuar las señales promotoras del cáncer procedentes de EGFR. Entender esta relación podría ayudar a explicar por qué algunos pacientes responden mejor a las terapias dirigidas contra EGFR y sugerir nuevas formas de mantener esos tratamientos efectivos por más tiempo. 
Un interruptor de crecimiento que se acelera
EGFR es un receptor ubicado en la superficie de muchas células, donde detecta señales de crecimiento del entorno. En una gran fracción de los adenocarcinomas de pulmón, EGFR está alterado de modo que permanece activado de forma permanente. Esto alimenta un crecimiento y una división constantes, y explica por qué las pastillas que bloquean EGFR, llamadas inhibidores de la tirosina quinasa, pueden reducir los tumores. Pero EGFR tiene otro lado, menos apreciado: puede viajar al núcleo celular y actuar directamente sobre el ADN, activando genes como cMYC y CCND1 que aumentan aún más el crecimiento, la supervivencia y la resistencia al tratamiento. Este papel nuclear de EGFR puede ayudar a los tumores a escapar incluso cuando su actividad en la superficie está químicamente bloqueada.
La sortilina entra en el núcleo
La sortilina se conocía principalmente como una proteína de clasificación que ayuda a internalizar EGFR desde la superficie celular y enviarlo hacia la degradación, debilitando así sus señales de crecimiento. En este trabajo, los autores muestran que la sortilina también sigue a EGFR hasta el núcleo cuando las células de cáncer de pulmón son estimuladas. Mediante microscopía de alta resolución y fraccionamiento bioquímico, observaron complejos de EGFR y sortilina formándose dentro de los núcleos poco después de la activación. De manera importante, cuando EGFR no podía entrar al núcleo, la sortilina tampoco lo hacía, lo que indica que EGFR actúa como el "pasaporte" de la sortilina hacia este compartimento. Una vez allí, se encontró que los complejos EGFR–sortilina estaban unidos a tramos de ADN cerca de los sitios de inicio de genes clave de control del crecimiento, incluidos cMYC y CCND1.
Un freno incorporado sobre los genes del cáncer
Para entender qué hacen estos complejos, los investigadores mapearon su unión a lo largo del genoma y midieron los cambios en la actividad génica. Encontraron que EGFR por sí solo tiende a promover la activación de genes relacionados con el crecimiento, mientras que la presencia de sortilina en esas mismas regiones del ADN atenúa este efecto. Cuando los niveles de sortilina se redujeron artificialmente, la unión de EGFR en los genes diana aumentó y genes impulsores del cáncer como cMYC y CCND1 se volvieron más activos. En contraste, aumentar los niveles de sortilina produjo el efecto opuesto: el agarre de EGFR sobre el ADN se aflojó, el reclutamiento de la maquinaria de transcripción disminuyó y la expresión de estos genes oncogénicos cayó. En modelos en ratón, los tumores pulmonares diseñados para sobreproducir sortilina crecieron más lentamente y mostraron niveles reducidos de cMYC y CCND1. 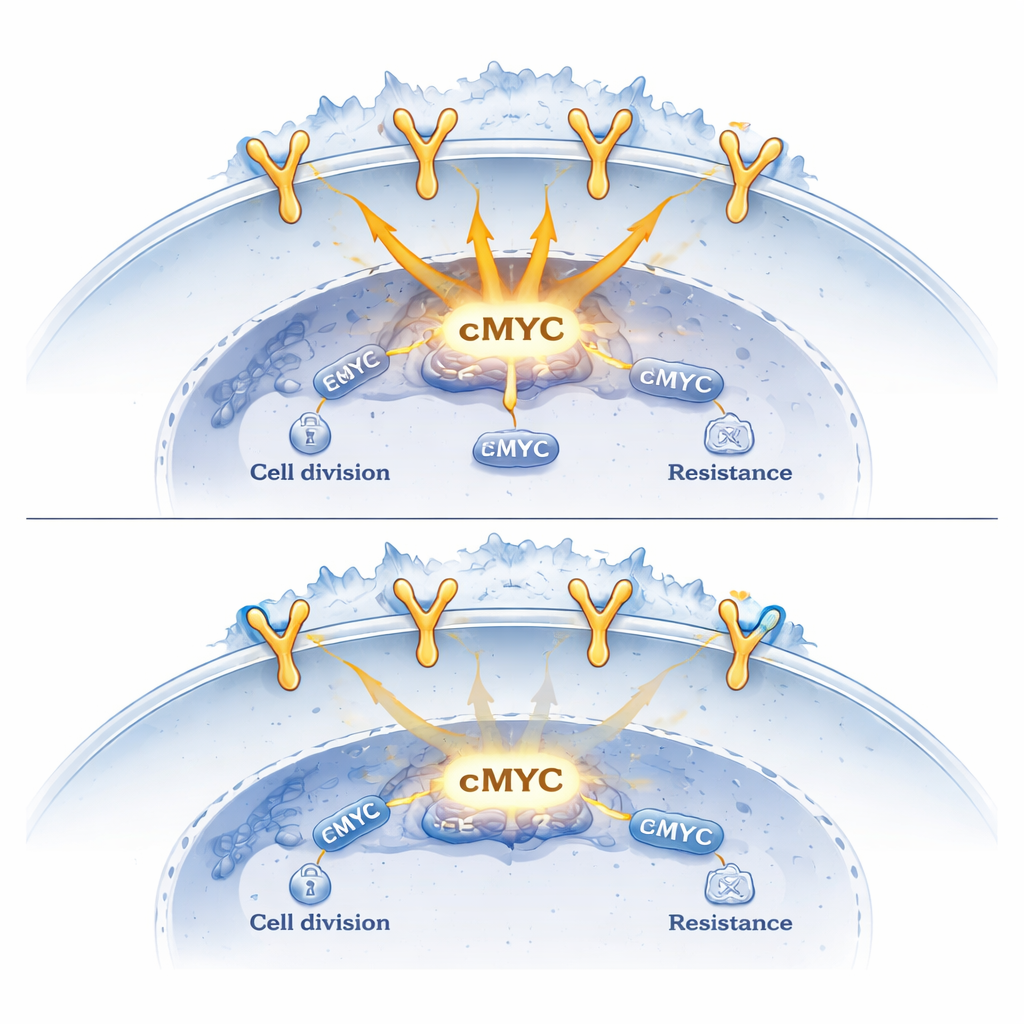
Interacción con fármacos contra EGFR
El estudio también exploró cómo este mecanismo interactúa con osimertinib, un fármaco dirigido contra EGFR ampliamente utilizado y diseñado para bloquear las mutaciones problemáticas de EGFR. Sorprendentemente, incluso cuando osimertinib inactivó la actividad enzimática de EGFR, el receptor siguió moviéndose al núcleo. Allí, continuó uniéndose al ADN, especialmente cerca del gen cMYC. Sin embargo, la sortilina también se acumuló en el núcleo bajo estas condiciones. Cuando la sortilina era abundante, los niveles de cMYC descendieron con más fuerza en respuesta a osimertinib y las células cancerosas mostraron menor viabilidad. El análisis de tumores de pacientes y de grandes conjuntos de datos públicos sobre cáncer mostró que los niveles de sortilina suelen ser más bajos en adenocarcinomas de pulmón que en tejido pulmonar normal, y que una mayor expresión de sortilina se asocia de forma consistente con una menor expresión de cMYC.
Qué significa esto para los pacientes
Considerados en conjunto, los hallazgos muestran a la sortilina como una especie de socia con rasgos de supresor tumoral que acompaña a EGFR al núcleo y luego lo modera. Al limitar la capacidad de EGFR para activar potentes genes de crecimiento como cMYC, la sortilina puede frenar la progresión tumoral y potenciar el efecto de los fármacos que bloquean EGFR. Debido a que muchos tumores pulmonares tienen niveles reducidos de sortilina, pueden carecer de este freno interno, lo que ayuda a explicar por qué algunos cánceres son particularmente agresivos o se vuelven rápidamente resistentes a los medicamentos. Medir los niveles de sortilina en los tumores podría ayudar a predecir la respuesta de un paciente a las terapias dirigidas contra EGFR, y las estrategias que aumenten la actividad de la sortilina podrían ofrecer una nueva vía para mantener los cánceres impulsados por EGFR bajo mejor control a largo plazo.
Cita: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Palabras clave: cáncer de pulmón, EGFR, sortilina, cMYC, resistencia a terapias dirigidas