Clear Sky Science · es
RO4938581, un modulador alostérico negativo de GABAA-α5 rescató fenotipos conductuales y de EEG en un modelo murino del síndrome Dup15q
Por qué importa esta investigación cerebral
El síndrome Dup15q es una condición genética poco frecuente que con frecuencia provoca autismo, convulsiones y graves dificultades de aprendizaje. Las familias cuentan principalmente con cuidados de apoyo y no existe un tratamiento que aborde la biología subyacente. Este estudio utilizó ratones portadores del mismo segmento extra de ADN que las personas con Dup15q para investigar qué falla en el cerebro y para probar si un fármaco experimental muy dirigido puede atenuar ese problema. El trabajo destaca un tipo específico de receptor cerebral como un objetivo prometedor y comprobable para futuras medicinas de precisión.
Demasiado freno en el cerebro
Nuestros cerebros dependen de un equilibrio delicado entre señales de “avance” que excitan las neuronas y señales de “alto” que las silencian. En el síndrome Dup15q se duplica un tramo del cromosoma 15. Esa región incluye tres genes que codifican partes de un receptor clave de “alto” en el cerebro, llamado receptor GABAA, y en especial una variante que contiene una subunidad llamada alfa-5. Los investigadores diseñaron ratones con ese mismo tipo de duplicación y encontraron que estos animales producían aproximadamente un 50 % más de receptores que contienen alfa-5 en regiones cerebrales importantes para la memoria, la emoción y el movimiento, incluido el hipocampo y la corteza. Múltiples métodos —desde la expresión génica hasta la imagen de receptores— convergieron en la misma conclusión: este sistema de freno en particular está sobredimensionado en el modelo Dup15q.
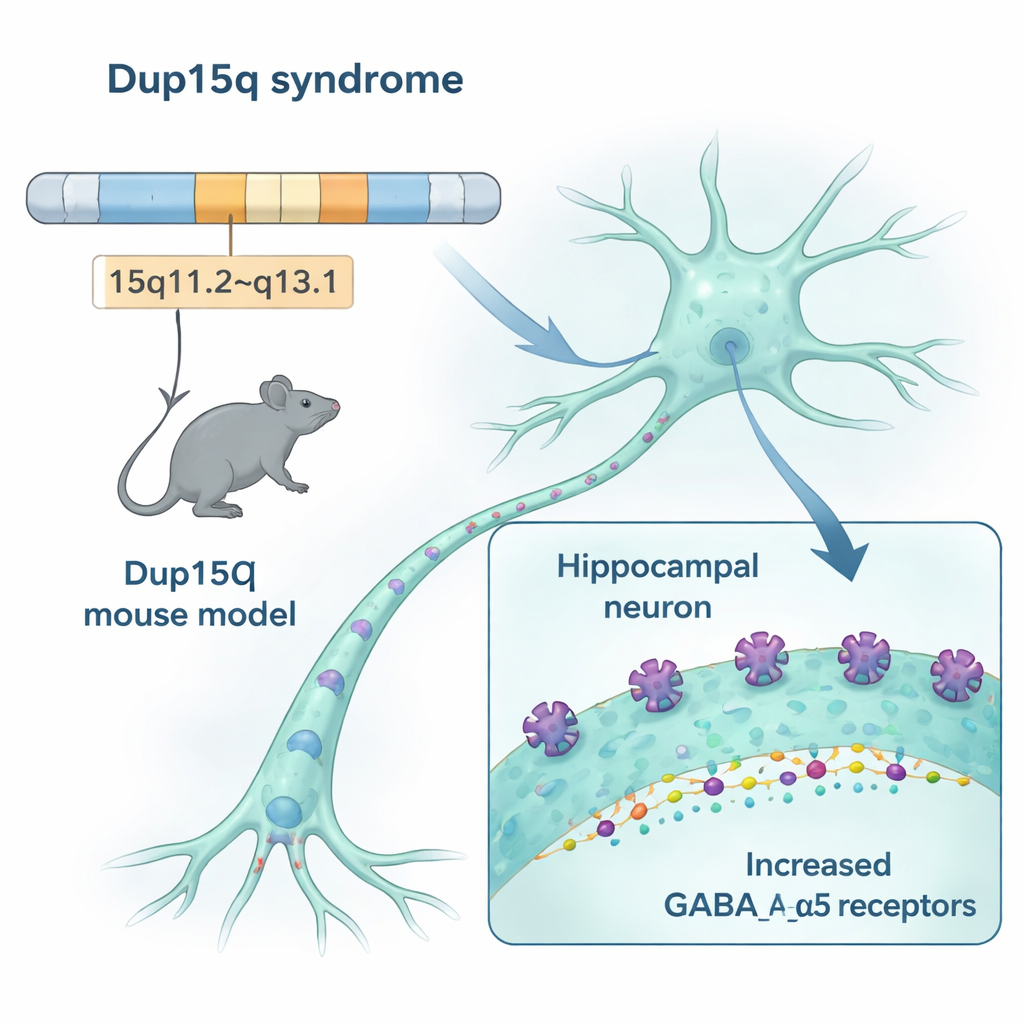
Cómo los receptores extra cambian las señales cerebrales
Tener más receptores de freno solo importa si de hecho cambia cómo disparan los circuitos. En cortes finos de hipocampo, el equipo midió las minúsculas corrientes eléctricas que las neuronas inhibitorias envían a otras células. En los ratones Dup15q, esas corrientes inhibitorias ocurrían con mayor frecuencia, lo que sugiere que las neuronas experimentaban un freno continuo más intenso, aunque el tamaño de cada señal individual no cambiaba. Una prueba separada del comportamiento de los circuitos, llamada inhibición pareada, también mostró que las redes en estos ratones estaban más amortiguadas que las de sus compañeros sanos. En conjunto, los datos indican que los receptores extra hacen que los circuitos inhibitorios sean más dominantes, desplazando el equilibrio lejos de un procesamiento de la información flexible.
Conducta y ondas cerebrales en ratones afectados
Los científicos preguntaron a continuación si este cableado alterado se traducía en comportamientos que recuerdan a los síntomas humanos. En una serie de pruebas, los ratones Dup15q mostraron indicios de diferencias sociales y de comunicación y, de forma más clara, problemas con la flexibilidad cognitiva. En una tarea del laberinto con agua, tanto los ratones normales como los Dup15q aprendieron dónde estaba una plataforma oculta. Pero cuando la plataforma se movió, los animales Dup15q fueron lentos en abandonar la ubicación anterior y adaptarse a la nueva, un paralelo de laboratorio de las rutinas rígidas que a menudo se observan en el autismo. El equipo también registró señales de electroencefalografía (EEG), los ritmos sumados de muchas neuronas. Como en las personas con Dup15q, los ratones mostraron una actividad anormalmente fuerte en la banda beta, un ritmo rápido que a menudo se potencia con fármacos que aumentan la acción de los receptores GABAA, lo que refuerza la idea de que su sistema inhibitorio estaba hiperactivo.
Un fármaco dirigido que afloja los frenos
Para ver si podían normalizar este exceso de freno, los investigadores recurrieron a RO4938581, un compuesto experimental que debilita selectivamente los receptores GABAA tipo alfa-5 sin afectar a otras formas. En cortes de hipocampo, el fármaco redujo la cantidad de transferencia de carga inhibitoria en neuronas Dup15q, contrarrestando el freno excesivo. Administrado por vía oral a diario durante varias semanas, el mismo compuesto mejoró el rendimiento de los animales en la fase de inversión del laberinto con agua, permitiéndoles ajustarse al cambio de plataforma de manera más parecida a los ratones sanos. También acercó sus interacciones sociales a la normalidad. En registros de EEG, una dosis aguda redujo parcialmente la potencia beta exagerada en los ratones Dup15q, empujando sus ritmos cerebrales hacia el patrón típico.
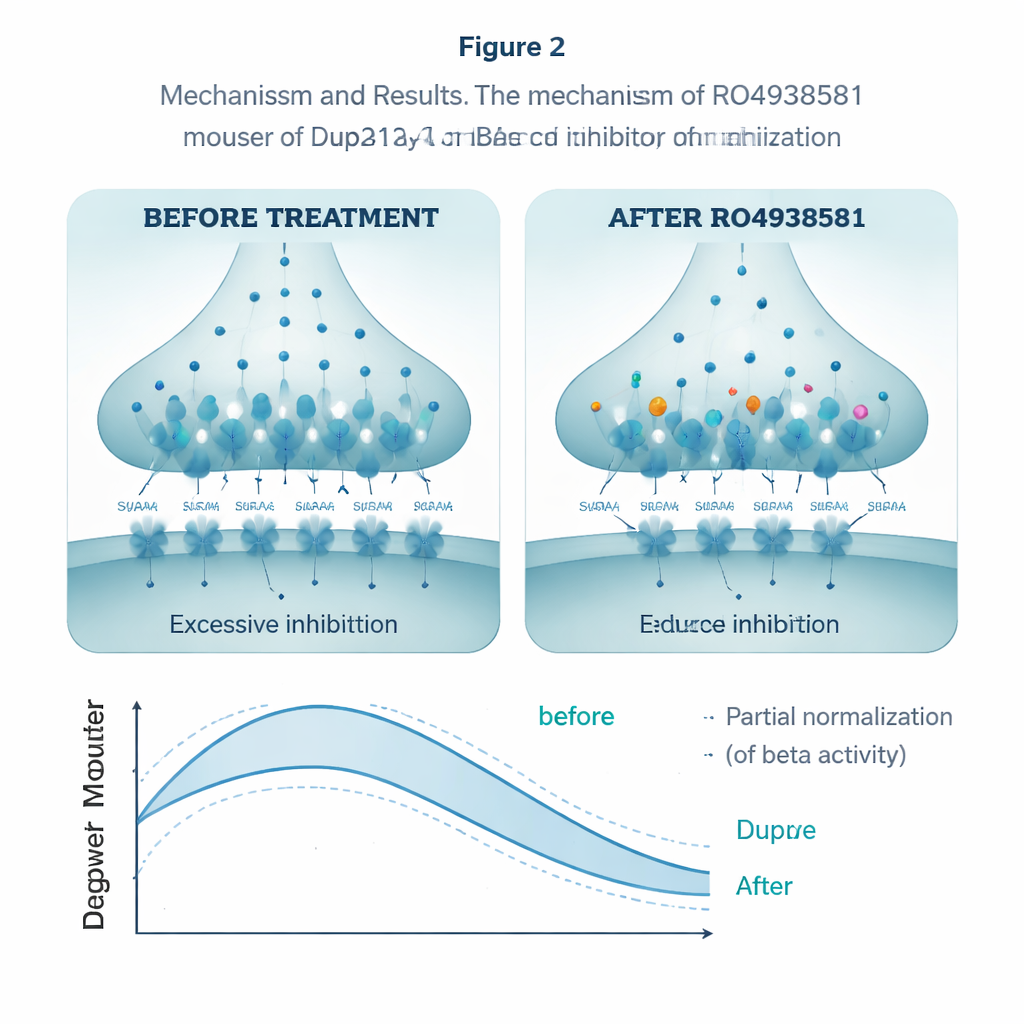
Qué podría significar esto para futuros tratamientos
Para las familias que conviven con el síndrome Dup15q, estos hallazgos no representan una cura inmediata, pero sí ofrecen una pista concreta. El trabajo señala un subtipo de receptor en particular —los receptores GABAA que contienen la unidad alfa-5— como sobreproducido y funcionalmente importante en un modelo animal relevante. Reducir modestamente este receptor con un modulador negativo como RO4938581 no lo arregló todo, pero mejoró el aprendizaje flexible, la conducta social y una firma clave en EEG. Esa combinación de cambios en el cerebro, el comportamiento y un biomarcador refuerza el argumento para probar fármacos dirigidos a alfa-5, más seguros y aptos para humanos, como tratamientos de precisión para Dup15q y, potencialmente, para condiciones del neurodesarrollo relacionadas.
Cita: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Palabras clave: síndrome Dup15q, receptor GABAA alfa-5, trastorno del neurodesarrollo, potencia beta en EEG, modelo de ratón