Clear Sky Science · es
Microfluidos inercial en cascada para el enriquecimiento de alto rendimiento y multi-escala de células tumorales y cúmulos intactos hacia un diagnóstico mejorado de malignidad
Por qué importa clasificar células cancerosas en fluidos
Cuando el cáncer se disemina, las células tumorales a menudo se escapan hacia los fluidos que bañan nuestros órganos. En personas con cáncer de pulmón, esto puede incluir el líquido que se acumula alrededor de los pulmones, llamado derrame pleural. Ocultas en este fluido hay células tumorales individuales raras y racimos compactos de células. Se piensa que estos cúmulos son especialmente peligrosos porque se asocian fuertemente con enfermedad agresiva y malos resultados. Sin embargo, los métodos de laboratorio actuales tienen dificultades para extraer con suavidad y eficiencia tanto las células individuales como los cúmulos de grandes volúmenes de fluido de pacientes. Este estudio presenta una nueva tecnología basada en un chip que puede clasificar rápida y cuidadosamente estas células de derrames pleurales, abriendo la puerta a un diagnóstico de cáncer más fiable y a mejores conocimientos sobre cómo se propagan los tumores.
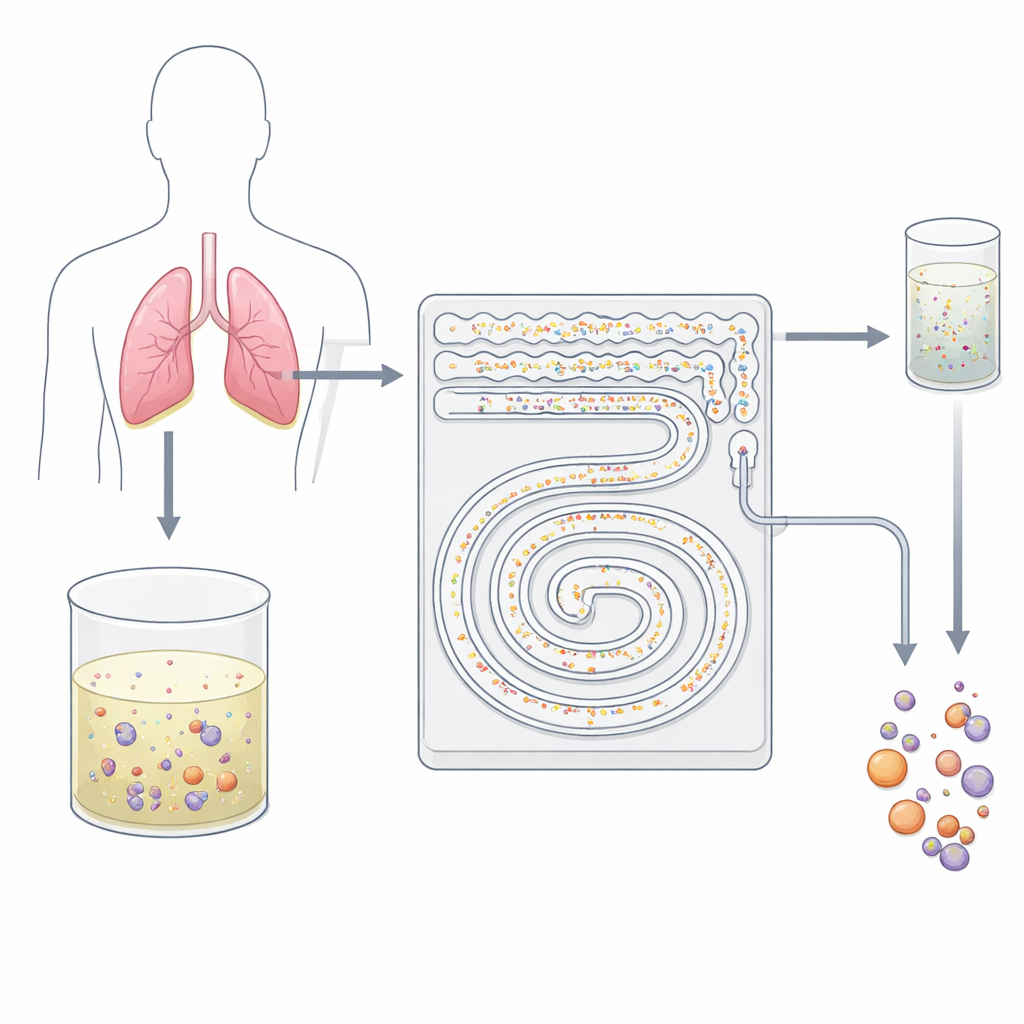
Un colador celular suave en un chip
Los investigadores diseñaron un dispositivo del tamaño de la palma tallado en plástico con canales diminutos que actúan como un filtro inteligente de dos etapas. En lugar de usar anticuerpos adhesivos o un tamizado agresivo, el chip se basa en cómo se comportan las células en un líquido que fluye a alta velocidad. A medida que el fluido atraviesa microcanales curvos, fuerzas invisibles empujan partículas de diferentes tamaños hacia diferentes líneas de flujo. El equipo aprovecha este efecto, conocido en términos generales como microfluidos inercial, para separar las pequeñas células sanguíneas de fondo de las células tumorales más grandes y sus cúmulos sin tocarlas ni marcarlas. Como todo ocurre en un flujo continuo y cerrado, el dispositivo puede procesar decenas de mililitros de fluido en cuestión de minutos: algo que la citología tradicional en portaobjetos no puede lograr fácilmente.
Primer paso: despejar la multitud
En la primera etapa del dispositivo, el derrame pleural —tras eliminar el exceso de líquido y re-suspender las células— se impulsa a través de una matriz de canales serpentinos paralelos. Aquí, el flujo curvo y arremolinado empuja las pequeñas células blancas hacia las paredes del canal, mientras que las células tumorales más grandes y los cúmulos permanecen cerca del centro del flujo. Las células pequeñas son guiadas hacia salidas de desecho, afinando drásticamente el fondo. Esta etapa de alto rendimiento puede funcionar a unos 8 mililitros por minuto, lo que significa que una muestra clínica típica de 50 mililitros puede procesarse en aproximadamente seis minutos y medio sin obstrucciones. Lo que surge de esta primera etapa es una mezcla mucho más limpia, enriquecida en células potencialmente malignas y lista para una separación más fina.
Segundo paso: separar individuales de cúmulos
La muestra parcialmente enriquecida entra entonces en un canal espiral inclinado que incluye un patrón repetido de secciones estrechas y anchas. En esta etapa, varias fuerzas de flujo se equilibran de manera diferente para objetos de distintos tamaños, guiándolos hacia carriles distintos cerca de la pared interna o externa de la espiral. Las células tumorales individuales, que son más pequeñas, se alinean en una posición lateral, mientras que los cúmulos más voluminosos migran a una posición diferente, más cercana a la pared interna. Al colocar salidas en los puntos adecuados, el chip divide físicamente estas corrientes: una salida recoge principalmente células tumorales individuales, otra reúne cúmulos intactos y otras eliminan las células pequeñas restantes. Es importante que los cúmulos se mantengan enteros, evitando el daño y la fragmentación que suele producirse con los métodos de filtración tradicionales.
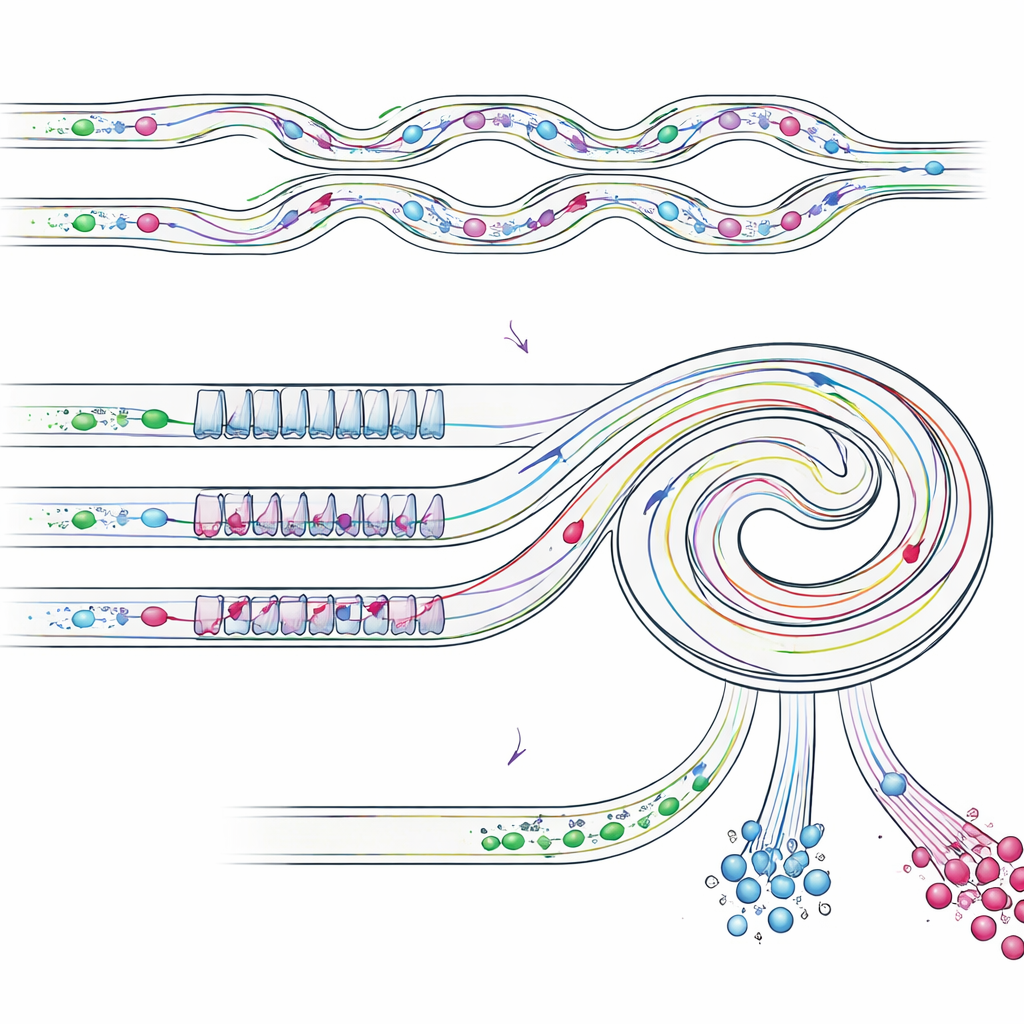
Poner el dispositivo a prueba
Para comprobar el rendimiento de su diseño, el equipo primero utilizó bolas de plástico de tamaños conocidos para imitar células sanguíneas, células tumorales individuales y cúmulos. Demostraron que el chip en cascada recuperó más del 87 % de las bolitas “de célula individual” y alrededor del 92 % de las bolitas “de cúmulo”, mientras eliminaba la mayoría de las bolitas más pequeñas “de células sanguíneas”. Luego pasaron a células reales de cáncer de pulmón (células A549) mezcladas con leucocitos. En estas pruebas, el dispositivo recuperó alrededor del 82 % de las células cancerosas en conjunto, con aproximadamente un 76 % de pureza en la fracción enriquecida y casi un 80 % de pureza para los cúmulos celulares. Finalmente, procesaron muestras reales de derrame pleural de tres pacientes con cáncer de pulmón. Partiendo de un fluido en el que las células tumorales y los cúmulos representaban menos del 1 % de todas las células, el chip produjo fracciones en las que las células malignas individuales alcanzaron alrededor del 68 % del total, y los cúmulos supusieron cerca del 35 % de las células en una corriente de salida dedicada.
Qué podría significar esto para los pacientes
Al usar solo el flujo de fluido y la geometría de los canales, este dispositivo puede extraer rápida y suavemente tanto células tumorales individuales como cúmulos intactos de grandes volúmenes de fluido de pacientes sin etiquetas químicas ni instrumentos complejos. Las células enriquecidas permanecen aptas para pruebas estándar como tinción por inmunofluorescencia y microscopía, integrándose sin problemas en los flujos de trabajo hospitalarios existentes. Aunque el estudio actual incluyó un número reducido de pacientes y necesitará ensayos más amplios para demostrar su impacto en el diagnóstico y el pronóstico, el trabajo demuestra un concepto potente: un “concentrador de células” rápido y sin etiquetas que revela tanto el número como el estado en cúmulos de las células tumorales en derrames pleurales. A largo plazo, herramientas así podrían afinar la evaluación de la malignidad, guiar decisiones de tratamiento personalizadas y ofrecer una ventana más clara sobre cómo las metástasis se forman y diseminan.
Cita: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Palabras clave: biopsia líquida, clasificación celular microfluídica, cúmulos de células tumorales, derrame pleural, diagnóstico del cáncer