Clear Sky Science · es
Diseño de un sistema automatizado de microinyección por lotes de células basado en pinzas magnéticas para embriones de pez cebra
Por qué importan los huevos de peces diminutos
Antes de que los nuevos medicamentos o terapias génicas lleguen a las personas, los científicos a menudo los prueban en animales pequeños de crecimiento rápido. Los embriones de pez cebra son preferidos porque son transparentes y se desarrollan con rapidez, lo que permite a los investigadores observar la formación de órganos en tiempo real. Pero para modificar sus genes o administrar fármacos, es necesario inyectar cada huevo delicado con una aguja microscópica, una tarea que suele ser lenta, fatigosa y muy dependiente de la habilidad humana. Este trabajo presenta un nuevo sistema robótico capaz de inyectar automáticamente lotes de embriones de pez cebra más rápido, con más delicadeza y con mayor fiabilidad que un operador humano, abriendo la puerta a experimentos más grandes y consistentes.
Una nueva forma de manipular células frágiles
La microinyección tradicional exige un operador entrenado que guíe una aguja de vidrio bajo un microscopio, localice cada embrión, lo oriente correctamente y lo perfore sin dañar estructuras vitales. Esto es especialmente delicado porque los embriones son esferas blandas con regiones importantes que deben evitarse para mantenerlos vivos. Los sistemas robóticos existentes han ayudado a automatizar el transporte y la perforación, pero por lo general no pueden controlar la rotación de cada embrión en las tres dimensiones. Como resultado, la aguja puede entrar en un ángulo arriesgado, reduciendo las tasas de supervivencia y limitando el número de embriones que pueden procesarse con fiabilidad. El equipo detrás de este estudio se propuso construir una plataforma totalmente integrada que pueda transportar, rotar, inyectar y liberar embriones en una secuencia fluida, sin cambios constantes de lente ni ajustes manuales.
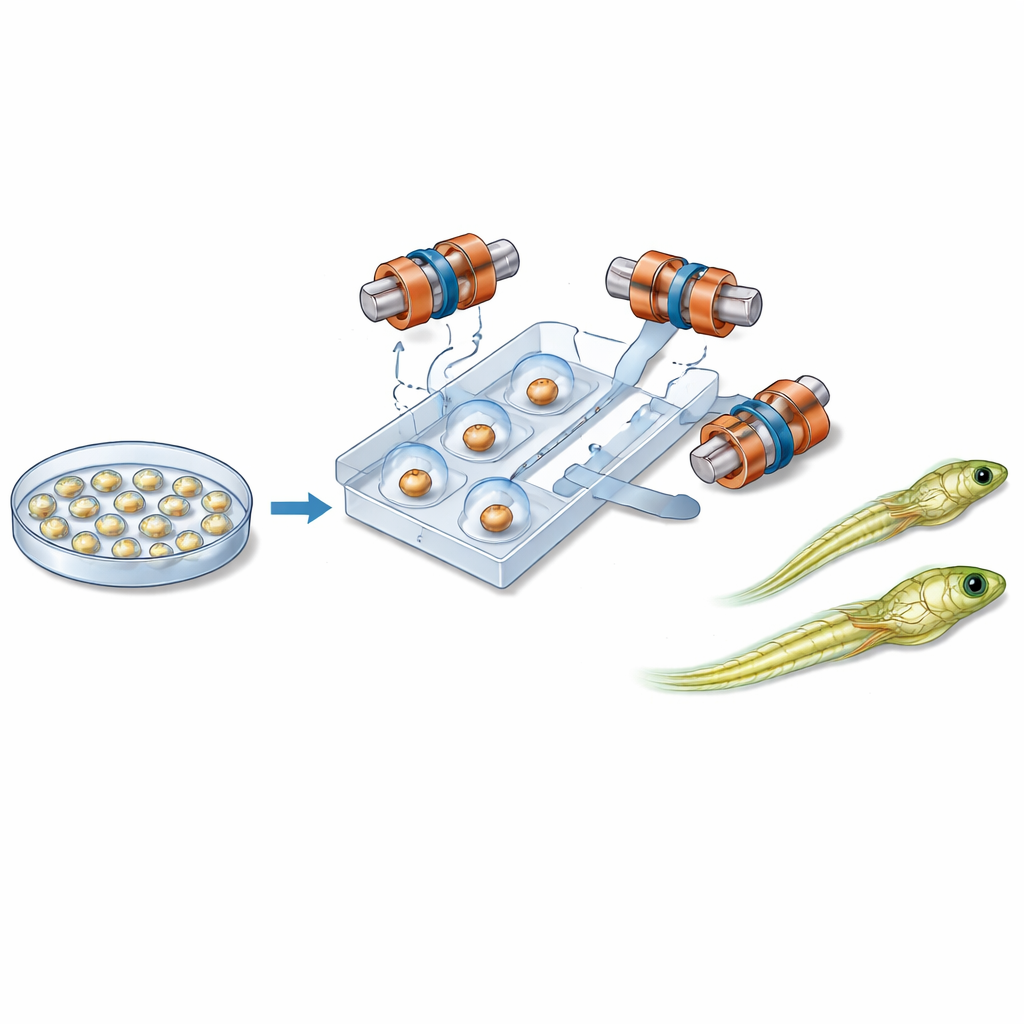
Imanes, microcanales y control delicado
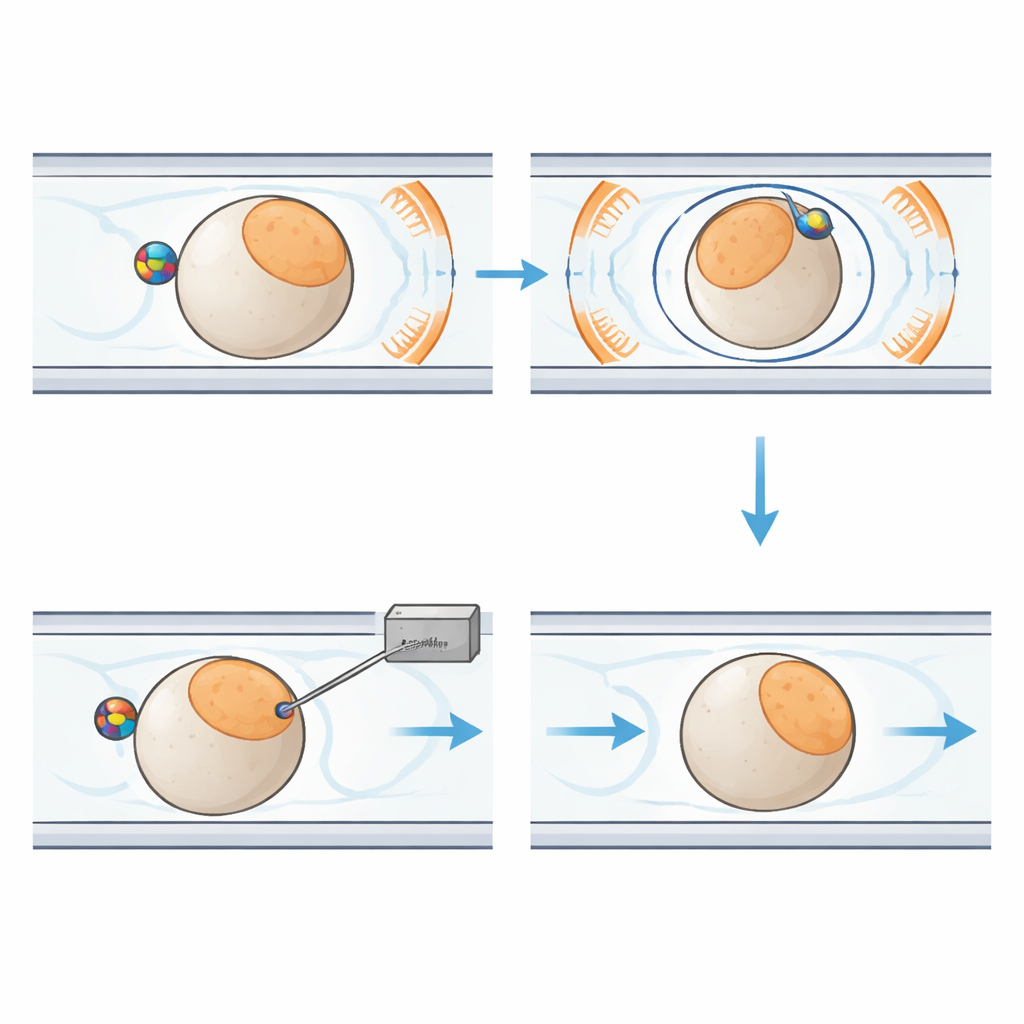
En el núcleo del nuevo sistema hay un chip de plástico del tamaño de la palma que contiene canales estrechos que guían embriones individuales a lo largo de una trayectoria fija. Cerca de cada embrión se sitúa una pequeña perla magnética. Alrededor del chip, seis bobinas dispuestas con cuidado generan un campo magnético uniforme en tres dimensiones. Al cambiar la dirección de este campo en el tiempo, el sistema hace girar la perla. Gracias a la fricción entre la perla y la superficie del embrión, toda la célula se mueve con ella, como dos engranajes entrelazados. Esto permite al robot inclinar el embrión fuera del plano de imagen o hacerlo girar dentro del plano hasta que la región sensible quede posicionada de forma segura, lejos de la aguja entrante. Líquido y una presión de aire suave mueven y mantienen los embriones en su lugar, mientras que un módulo separado controla la aguja de inyección y el diminuto flujo de material genético.
Ver con claridad en un campo visual diminuto
Para que esta coreografía precisa sea posible, los investigadores también diseñaron un sistema avanzado de visión por ordenador, llamado red de percepción para manipulación microscópica. Analiza imágenes de una cámara de microscopio en tiempo real para localizar cada embrión, detectar la fina punta de la aguja y distinguir los dos “polos” opuestos del huevo donde se encuentran las estructuras clave del desarrollo. La red utiliza técnicas modernas de aprendizaje profundo —como rutas duales de extracción de características, módulos de atención que resaltan detalles importantes y fusión multinivel de información de imagen— para manejar el mundo abarrotado y con baja iluminación dentro de un chip microfluídico. En pruebas con miles de imágenes, detectó objetos y segmentó regiones del embrión con una precisión aproximada del 98–99%, proporcionando la retroalimentación fiable necesaria para guiar tanto la rotación magnética como la colocación de la aguja.
Demostrar su eficacia en pez cebra vivo
El equipo comparó su sistema automatizado con operadores humanos experimentados usando 100 embriones de pez cebra cada uno. El robot completó sus inyecciones en aproximadamente 33,8 segundos por embrión, más del doble de rápido que el trabajo manual, y perforó con éxito cada célula. También orientó cada embrión con un error angular medio de solo 2,1 grados, aproximadamente la mitad del error de los operadores humanos. Lo más importante, el 88% de los embriones inyectados por el robot sobrevivieron hasta eclosionar como larvas, frente al 66% tras la inyección manual. Bajo un microscopio de fluorescencia, las larvas procedentes del sistema automatizado brillaron en verde, mostrando que el material genético introducido fue incorporado y expresado según lo planeado. Al rotar los embriones magnéticamente en lugar de apretarlos con herramientas mecánicas, el sistema minimizó la deformación y el daño manteniendo un alto rendimiento.
Qué significa esto para estudios futuros
En términos sencillos, este trabajo demuestra que una combinación cuidadosamente diseñada de microcanales, control magnético y análisis de imagen inteligente puede inyectar embriones de peces frágiles más rápidamente y con mejor supervivencia que una persona experta usando herramientas tradicionales. Dado que el pez cebra es una plataforma clave para estudiar el desarrollo, las enfermedades y los efectos de los fármacos, un inyector fiable de alto rendimiento podría acelerar cribados genéticos a gran escala y estudios biológicos a largo plazo que antes estaban limitados por el trabajo manual. Con los cambios de diseño adecuados en el chip y en los ajustes de control, la misma estrategia podría adaptarse a otros tipos celulares y pequeños organismos, ayudando a convertir la cirugía celular delicada de un arte practicado por unos pocos especialistas en un proceso automatizado y estandarizado.
Cita: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Palabras clave: embriones de pez cebra, microinyección, pinzas magnéticas, microfluidos, manipulación robótica de células