Clear Sky Science · es
Hojas híbridas nanoestructuradas de WS2 con Cu pegilado para terapia multimodal dirigida del cáncer
Por qué importan tratamientos contra el cáncer más inteligentes
Muchas personas con cáncer de mama siguen afrontando terapias agresivas que pueden dañar tejido sano sin detener completamente el tumor. Este estudio describe un nuevo tipo de lámina diminuta e ingeniería —demasiado pequeña para verse a simple vista— diseñada para viajar por el cuerpo, localizar tumores mamarios y atacarlos de varias maneras coordinadas a la vez. Al combinar calor, química y un fármaco oncológico clásico en un único paquete dirigido, los investigadores buscan que el tratamiento sea tanto más potente como menos perjudicial para el resto del organismo. 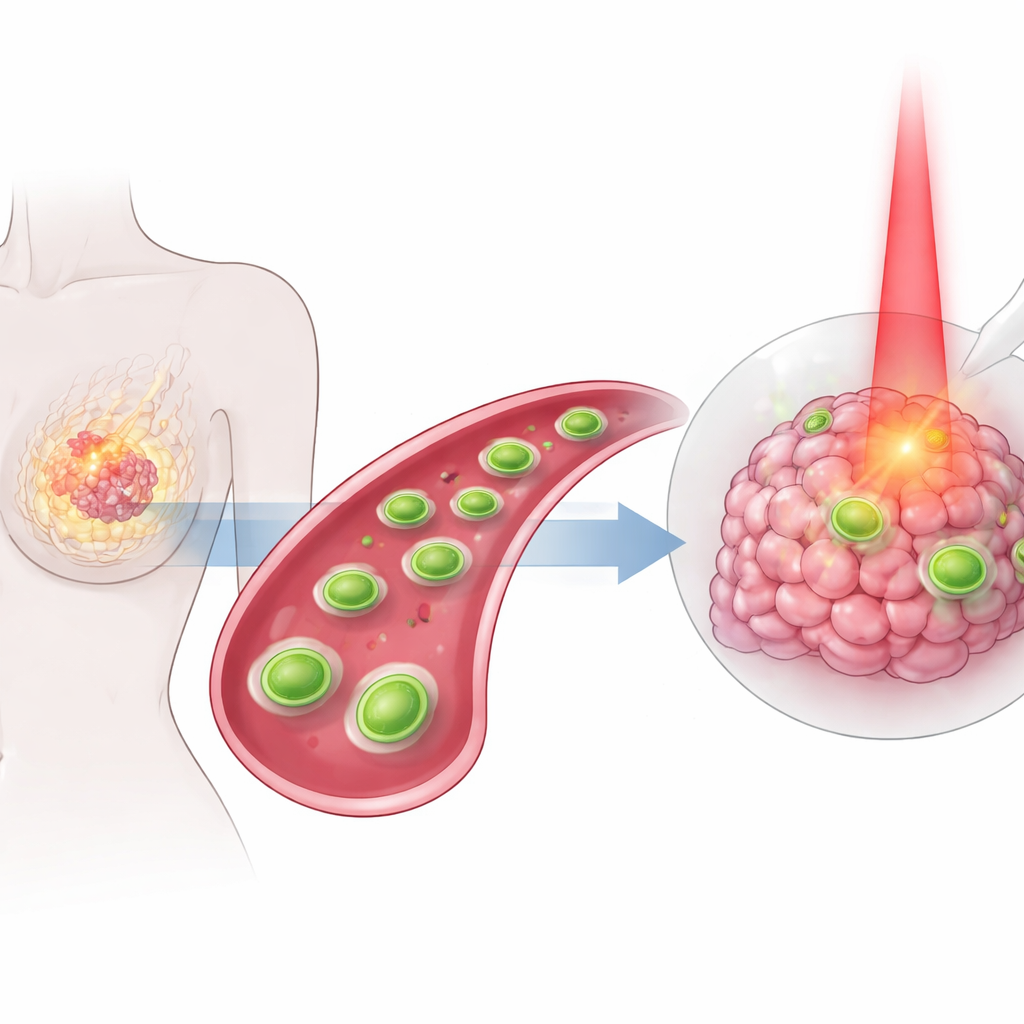
Hojas diminutas diseñadas para transportar y liberar tratamiento
El núcleo del enfoque es un material ultrafino hecho de tungsteno y azufre, con forma de láminas a escala nanométrica. Estas láminas absorben de forma natural la luz del infrarrojo cercano y la convierten en calor. El equipo creó primero estas láminas y luego rugosó cuidadosamente su superficie para que pudieran alojar otros ingredientes útiles. Átomos de cobre fueron anclados de forma altamente dispersa sobre las láminas, y se añadió un recubrimiento blando y flexible similar a un “impermeable” molecular para ayudar a que las partículas se mezclen bien en los fluidos corporales y evitar que se aglomeren. Finalmente, se fijó ácido fólico —una vitamina que muchas células tumorales captan con preferencia— como dispositivo de orientación, y se cargó la superficie con el fármaco quimioterápico común doxorrubicina. El resultado final es una plataforma diminuta y estratificada que puede circular por la sangre, reconocer células tumorales y transportar una carga considerable de tratamiento.
Cómo trabajan juntos la luz, la química y el fármaco
Una vez que estas partículas llegan a un tumor, ocurren varias cosas en concierto. Cuando la zona tumoral se ilumina con un láser rojo suave, las láminas de tungsteno‑azufre se calientan con eficiencia, elevando la temperatura local lo suficiente como para estresar y dañar las células cancerosas sin sobrecalentar el resto del cuerpo. Al mismo tiempo, los átomos de cobre sobre las láminas reaccionan con moléculas de peróxido naturales que ya están presentes en niveles superiores dentro de los tumores. Esta reacción convierte el peróxido en oxidantes muy agresivos y de corta vida que perforan componentes celulares desde el interior. Los tumores también tienden a ser algo más ácidos que el tejido sano; en este entorno más ácido, y bajo la acción térmica del láser, el enlace entre la lámina y la doxorrubicina se debilita, lo que permite que más fármaco se libere precisamente donde se necesita. Estos tres efectos —calor, ataque químico y quimioterapia focalizada— están diseñados para reforzarse mutuamente. 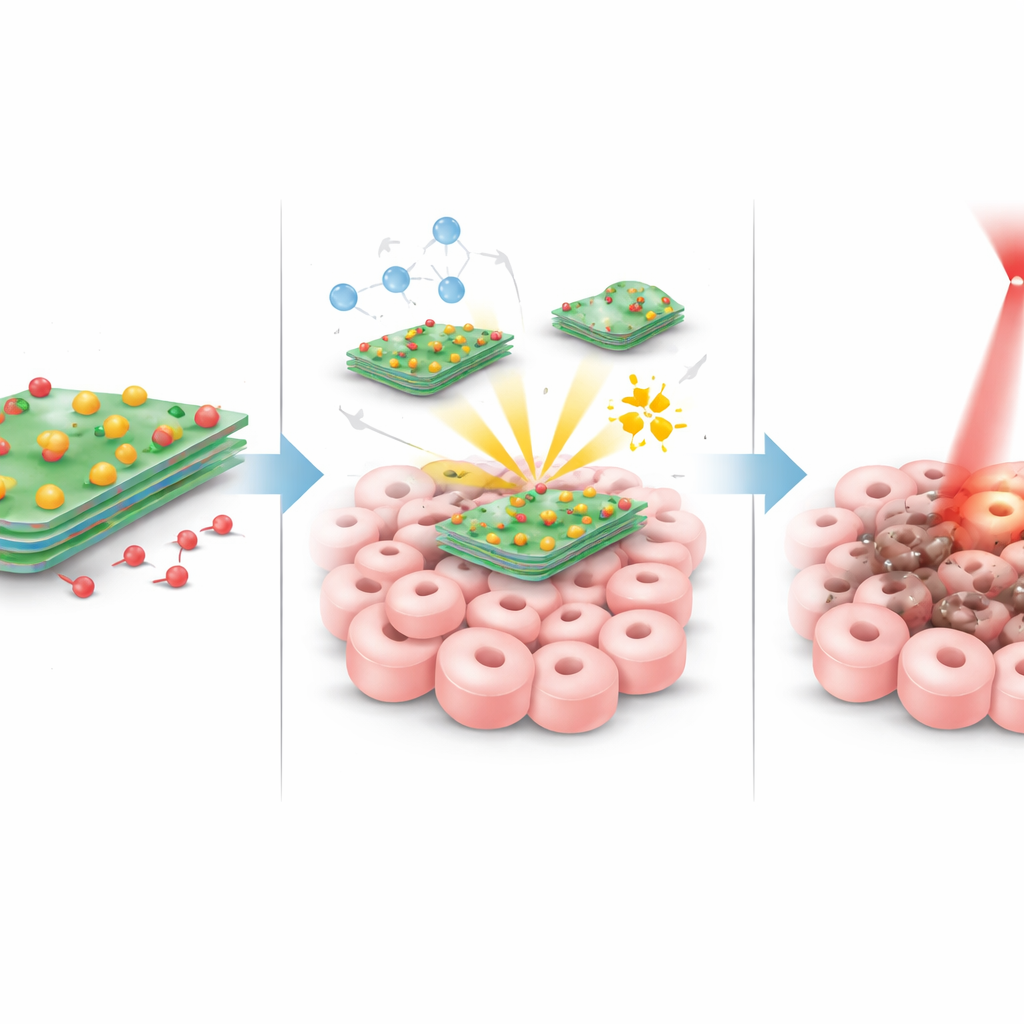
Pruebas en células y en ratones portadores de tumores
En cultivos celulares, las láminas recubiertas por sí solas mostraron poco daño a células normales, lo que sugiere una seguridad básica razonable. Pero cuando se cargaron con doxorrubicina y se expusieron a la luz láser en presencia de peróxido, provocaron una muerte marcada de células de cáncer de mama, mucho mayor que la observada con cualquier tratamiento individual. Los investigadores también demostraron que las partículas generan un aumento de oxidantes reactivos dentro de las células tumorales, confirmando que la química del cobre está activa. En ratones con tumores mamarios, las partículas con recubrimiento de ácido fólico se acumularon de forma mucho más intensa y prolongada en el tejido tumoral que las partículas no dirigidas. Cuando los ratones recibieron la combinación completa —partículas dirigidas más exposición a luz roja—, sus tumores se redujeron de forma drástica, su tiempo de supervivencia aumentó y su peso corporal y la salud de sus órganos se mantuvieron en gran medida normales, lo que indica efectos secundarios limitados en comparación con el tratamiento farmacológico estándar.
Qué podría significar esto para la atención del cáncer en el futuro
En conjunto, los hallazgos sugieren que estas láminas diseñadas actúan como una navaja de múltiples herramientas para el tratamiento del cáncer: buscan los tumores, los calientan, los envenenan desde dentro mediante química reactiva y entregan un fármaco probado con mayor precisión, todo ello mientras preservan gran parte del resto del organismo. El trabajo sigue estando en la fase de estudios en animales, y quedan preguntas importantes sobre la seguridad a largo plazo, la degradación y la mejor manera de fabricar dichas partículas para uso humano. Sin embargo, el diseño muestra cómo combinar varios tratamientos moderados en un solo paquete inteligente adaptado al propio microambiente tumoral puede producir un efecto global mucho más potente. Si estudios futuros confirman su seguridad y eficacia, estas nanoplataformas multifuncionales podrían ayudar a que la terapia del cáncer de mama sea más dirigida, más eficiente y menos dura para los pacientes.
Cita: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Palabras clave: terapia del cáncer de mama, nanomedicina, tratamiento fototérmico, liberación dirigida de fármacos, terapia quimiodinámica