Clear Sky Science · es
Dispositivo microfluídico monocapa de fabricación rápida y económico para el enfoque hidrodinámico tridimensional de alto rendimiento
Por qué importa reducir esos flujos diminutos
La medicina moderna depende cada vez más de observar enormes cantidades de células individuales una por una, por ejemplo para detectar células cancerosas en orina o sangre. Para hacerlo de forma rápida y económica, las células suelen transportarse por canales del grosor de un cabello en microchips, donde las inspeccionan láseres o cámaras. Pero para obtener imágenes nítidas y fiables a velocidades extremas, cada célula debe pasar por prácticamente el mismo punto microscópico. Este artículo presenta una nueva forma de fabricar esos chips para que puedan guiar con precisión las células hacia un estrecho flujo tridimensional, incluso a velocidades muy altas, usando un dispositivo que es más rápido y barato de producir que los sistemas estándar actuales.
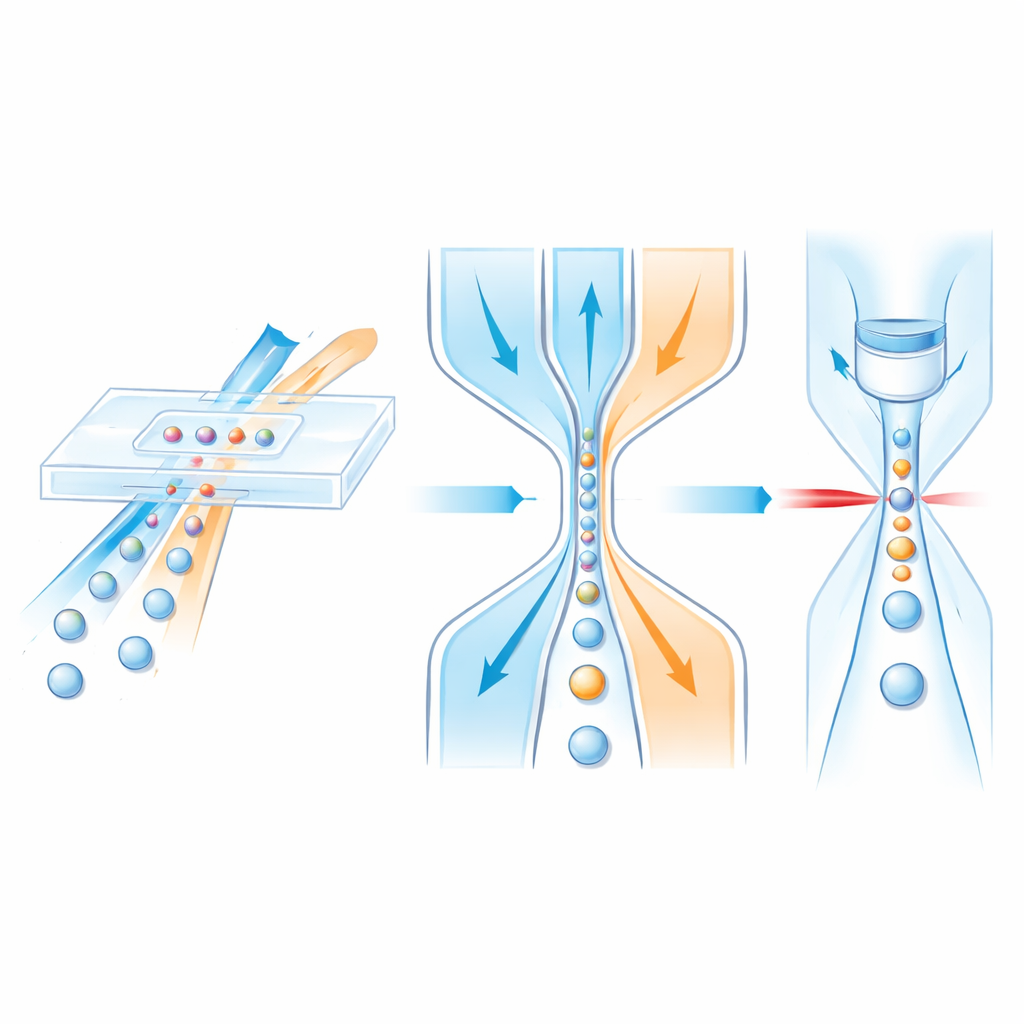
Guiar células con “carriles” de flujo
Dentro de un chip microfluídico, las células viajan en un flujo líquido central mientras que los fluidos circundantes, denominados revestimiento o sheath, actúan como barreras invisibles, comprimiendo suavemente la muestra hacia el centro. Los diseños anteriores normalmente podían enfocar las células solo de lado a lado, no de arriba abajo, o dependían de estructuras multicapa complejas que son lentas y costosas de fabricar. Los autores, en cambio, diseñan un canal monocapa que consigue un control tridimensional completo. Primero, la muestra se incorpora a un flujo sheath vertical en una unión en T angulada que se estrecha a lo largo de su recorrido. Debido a la forma del canal y a la inercia de los líquidos a velocidades más altas, el flujo de muestra se desplaza hacia la mitad superior del canal. A continuación, dos sheath laterales coincidentes más abajo comprimen desde la izquierda y la derecha, apretando la muestra ya elevada en un filamento central estrecho que atraviesa una ventana de detección.
Fabricar mejores chips en minutos, no horas
La mayoría de los chips microfluídicos de investigación actuales se fabrican con silicona blanda (PDMS) mediante litografía blanda, un proceso que requiere varios pasos de calentamiento y curado y puede llevar una hora o más por dispositivo. El PDMS es fácil de moldear pero se deforma bajo alta presión, haciendo que los canales se abulten y el flujo enfocado se disperse. El nuevo dispositivo utiliza un plástico rígido llamado acrilato de poliuretano (PUA), estampado mediante un proceso de “doble transferencia”. Primero, se vierte un molde reutilizable de PDMS con las características de canal en relieve a partir de un maestro de silicio. Luego se vierte PUA líquido en ese molde, se cura con luz ultravioleta y se despega para formar la capa de canal. Una diapositiva de vidrio recubierta de PUA sirve como base. Las dos superficies de PUA se alinean, se presionan entre sí y se enlazan con otra breve exposición a UV. Como cada paso de curado dura solo segundos y no se requiere un horneado prolongado, un chip completo puede producirse en unos cinco minutos, aproximadamente diez veces más rápido que los métodos tradicionales.
Probar el flujo y controlar la deformación
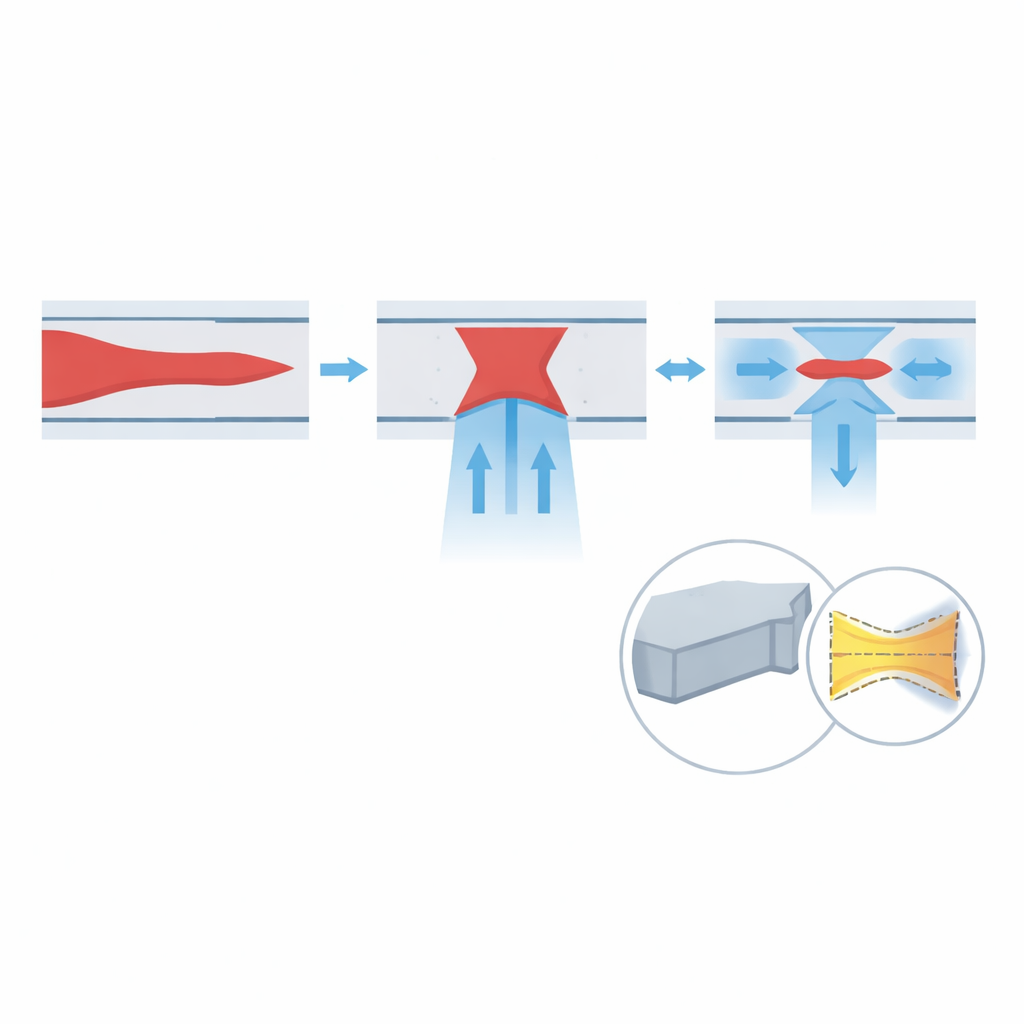
Para entender el rendimiento del diseño, el equipo combina simulaciones por ordenador con experimentos. Primero, simulan cómo cambiar las tasas de flujo de la muestra y de los sheath afecta la forma del núcleo enfocado. Los resultados muestran que aumentar los flujos sheath vertical y lateral ayuda a reducir tanto la altura como el ancho de la muestra, y que mayores velocidades globales (mayor número de Reynolds) mejoran aún más el enfoque. Luego simulan cómo se deforman las paredes del canal cuando están hechas de PDMS blando frente a PUA rígido. En condiciones realistas de alta velocidad, las paredes de PDMS sobresalen más de cien micrómetros, lo suficiente para distorsionar el flujo de forma que la muestra se divide y deriva hacia las esquinas. En contraste, el PUA se deforma menos de cien nanómetros—prácticamente rígido a esta escala—por lo que el flujo enfocado permanece centrado y estrecho incluso a alta presión.
Ver células reales a velocidades extremas
Además de pruebas con colorantes, los autores evalúan el dispositivo usando microscopía por estiramiento temporal óptico (OTS), una técnica que convierte pulsos láser ultrarrápidos en barridos lineales rápidos, permitiendo millones de líneas de imagen por segundo. Hacen pasar muestras de orina tratada de pacientes con cáncer de vejiga por el chip a velocidades de flujo crecientes, mientras OTS registra imágenes bidimensionales de cada célula que pasa. Dado que el sistema óptico tiene una región focal muy delgada, cualquier célula que se desplace hacia arriba o hacia abajo aparece borrosa, proporcionando una medida directa del enfoque vertical. En velocidades de 3,3 a 16,7 metros por segundo, la fracción de imágenes nítidas aumenta, alcanzando el 98,4% a la velocidad más alta probada. El enfoque lateral se evalúa midiendo cuánto se desvía el centro de las células respecto al punto medio del canal; este desplazamiento disminuye con la velocidad, correspondiendo a aproximadamente un 95,0% de eficiencia de enfoque lateral a 16,7 metros por segundo.
Qué significa esto para el análisis celular futuro
En términos sencillos, los investigadores demuestran que un chip plástico monocapa y sencillo puede reunir de forma fiable las células en un flujo estrecho y bien controlado en todas las direcciones, incluso bajo las exigentes condiciones requeridas para imágenes ultra‑rápidas. Al combinar un material resistente a la deformación con una disposición inteligente de flujos sheath, evitan los límites mecánicos de los dispositivos de silicona blanda y acortan dramáticamente el tiempo de fabricación. Esto facilita producir muchos chips idénticos para uso clínico e industrial y realizar pruebas a gran escala y alto rendimiento con muestras reales de pacientes. Como resultado, la tecnología ofrece una vía práctica hacia herramientas de cribado celular más rápidas y precisas que podrían beneficiar el diagnóstico, el seguimiento del cáncer y otras aplicaciones que dependen de observar de cerca a un gran número de células individuales.
Cita: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Palabras clave: citometría de flujo microfluídica, enfoque hidrodinámico 3D, análisis unicelular de alto rendimiento, chips microfluídicos de acrilato de poliuretano, microscopía por estiramiento temporal óptico