Clear Sky Science · es
Matrices de microelectrodos modificadas con PEDOT:PSS/PDA de alta estabilidad mecánica revelan actividad neuronal dinámica específica del estado a lo largo del ciclo sueño-vigilia
Por qué importan mejores sensores cerebrales para el sueño
El sueño condiciona cómo pensamos, sentimos y mantenemos la salud, sin embargo la actividad detallada del cerebro durante el sueño y la vigilia sigue siendo difícil de observar, especialmente en regiones profundas. Este estudio aborda ese reto construyendo sensores cerebrales diminutos y más resistentes que pueden escuchar a neuronas individuales durante semanas, y usándolos para explorar cómo se comporta un centro clave de la recompensa, el área tegmental ventral (VTA), a lo largo del ciclo sueño–vigilia en ratones.
Construir un diminuto y flexible dispositivo de escucha
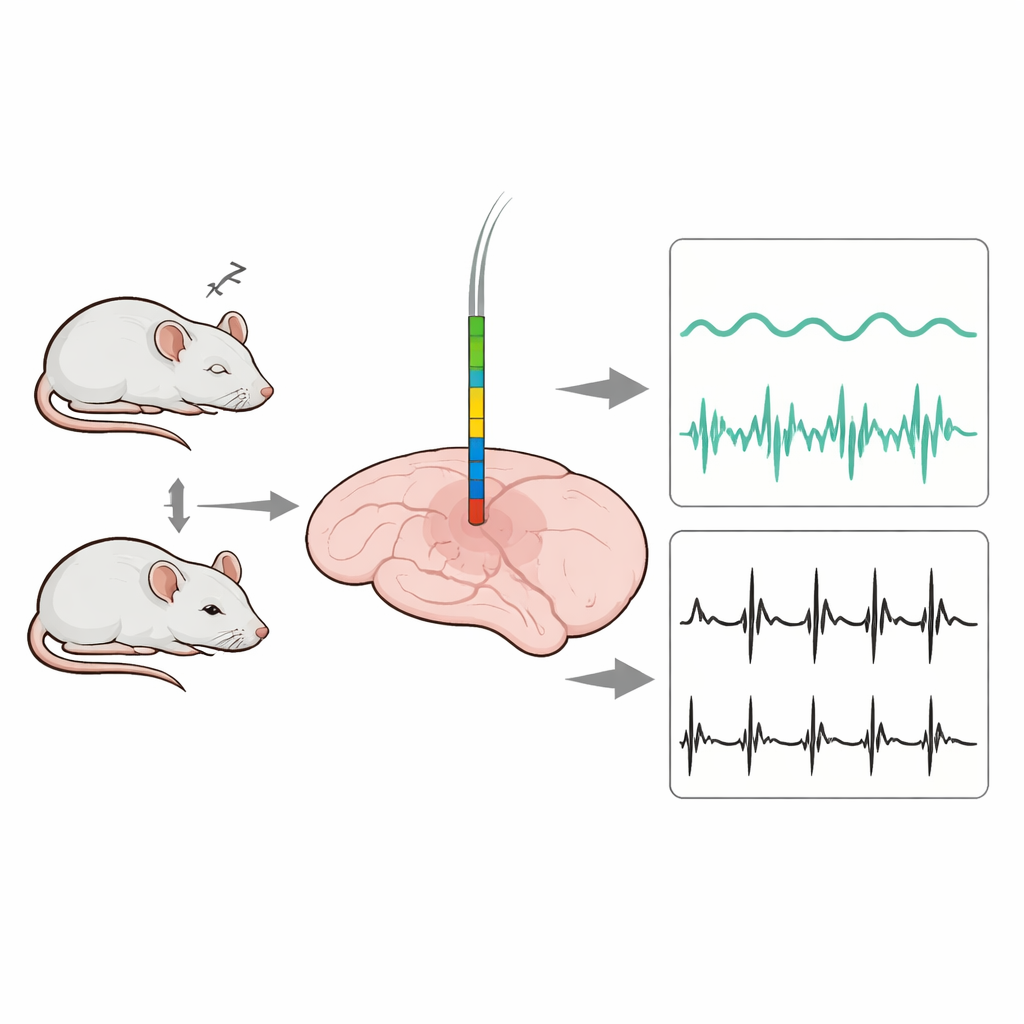
Los investigadores empezaron diseñando una delgada matriz de microelectrodos—una tira en forma de peine con 16 sitios de registro microscópicos—sobre una base de silicio. Cada sitio tiene un tamaño aproximado al de una sola neurona, lo que permite al dispositivo captar tanto ondas de fondo lentas como espigas eléctricas rápidas de células individuales. La sonda mide solo 25 micrómetros de grosor y unos pocos cientos de micrómetros de ancho, por lo que puede introducirse en regiones cerebrales profundas como la VTA minimizando el daño y la inflamación. El sistema completo combina esta sonda profunda con electrodos colocados en el cráneo y el cuello para registrar simultáneamente ondas cerebrales estándar (EEG) y la actividad muscular (EMG).
Hacer electrodos que perduren dentro del cerebro
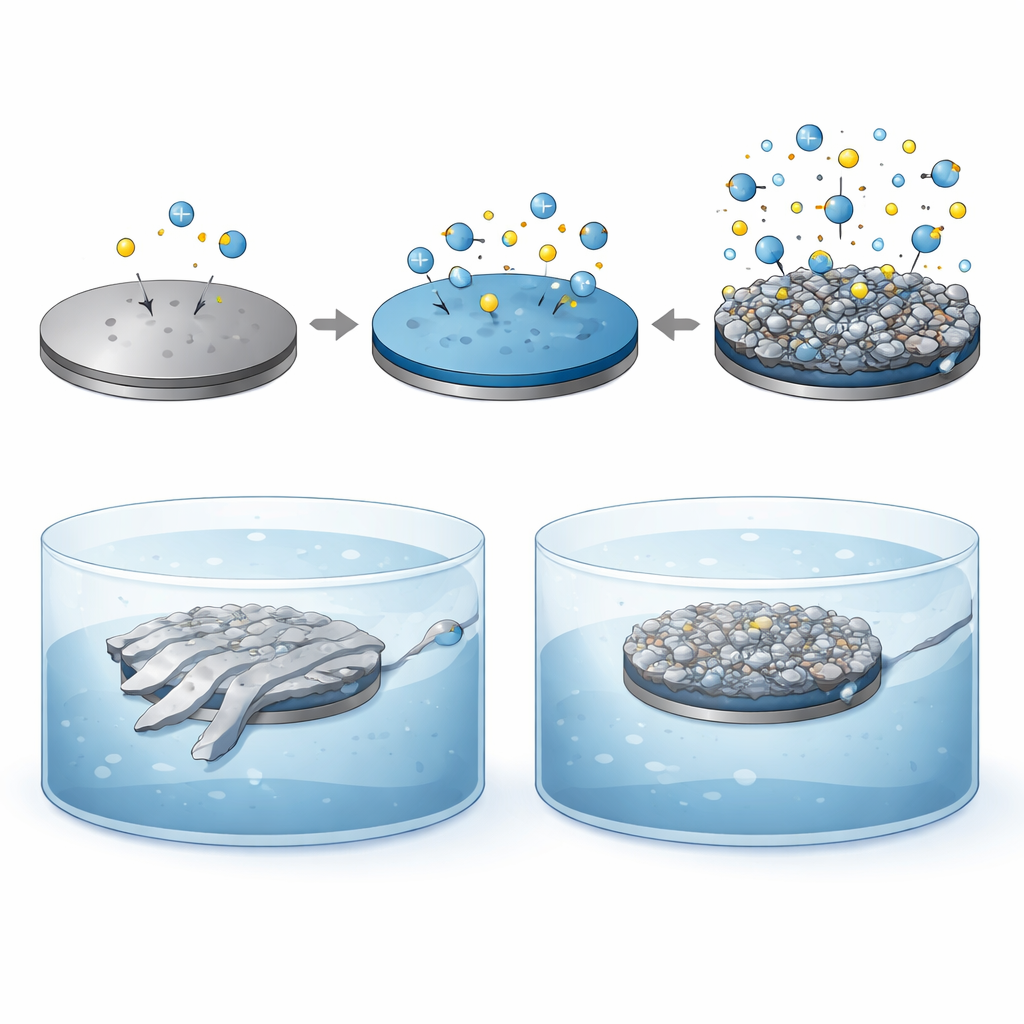
Escuchar el cerebro durante semanas es difícil porque las superficies metálicas de los electrodos diminutos suelen degradarse, soltarse o irritar el tejido circundante. Para resolverlo, el equipo creó un nuevo recubrimiento que combina un polímero conductor conocido, PEDOT:PSS, con un material adhesivo inspirado en la biología llamado polidopamina (PDA). En lugar de aplicarlos por capas en pasos separados, co-depositaron ambos en un único proceso electroquímico, formando una red entrelazada que se adhiere firmemente al metal. Este recubrimiento rugoso y esponjoso aumenta considerablemente el área efectiva de la superficie del electrodo y añade grupos químicos que atraen agua y células, haciendo la interfase tanto más conductora como más acogedora para el tejido cerebral.
Probar resistencia, estabilidad y compatibilidad celular
En el laboratorio, el nuevo recubrimiento transformó el comportamiento eléctrico de los electrodos. La resistencia a las señales neuronales cayó de aproximadamente dos millones de ohmios en el metal desnudo a unos cuarenta mil con PEDOT:PSS solo, y a menos de treinta mil cuando se añadió PDA. La cantidad de carga que el electrodo podía almacenar e intercambiar de forma segura aumentó casi treinta veces en comparación con el metal desnudo. Es importante que, cuando las sondas se agitaron en un baño ultrasónico para imitar las tensiones físicas dentro del cerebro, el recubrimiento tradicional de PEDOT:PSS se desprendió y su rendimiento colapsó, mientras que el recubrimiento PEDOT:PSS/PDA permaneció intacto y estable. Pruebas con células madre neuronales mostraron que la superficie que contenía PDA era mucho más hidrofílica y soportaba una mayor supervivencia y crecimiento celular durante varios días, lo que indica una fuerte biocompatibilidad.
Observar la actividad cerebral profunda durante sueño y vigilia
Con estas sondas mejoradas, los científicos las implantaron en la VTA de ratones y registraron de forma continua durante tres semanas mientras también monitorizaban EEG y EMG para etiquetar vigilia, sueño no REM y sueño REM. El nuevo recubrimiento proporcionó espigas neuronales más nítidas con aproximadamente el doble de relación señal-ruido que los recubrimientos estándar, y estas señales limpias se mantuvieron estables en el tiempo. Al clasificar formas de espiga y patrones de disparo, el equipo identificó 87 neuronas individuales que se agruparon en tres conjuntos: algunas disparaban más durante la vigilia, otras durante el sueño (tanto no REM como REM), y un tercer grupo mantenía actividad similar en todos los estados. Al mismo tiempo, los potenciales de campo local lentos en la VTA cambiaron de una actividad rápida y de baja amplitud en la vigilia a grandes ondas lentas en el sueño no REM, y luego volvieron a ritmos más rápidos en REM, con bandas de frecuencia que siguieron las etapas del sueño incluso con mayor nitidez que el EEG registrado en el cuero cabelludo.
Qué significa esto para el sueño y los dispositivos futuros
En conjunto, estos resultados muestran que la VTA, conocida desde hace tiempo por su papel en la motivación y la recompensa, también contiene conjuntos distintos de neuronas que siguen y posiblemente ayudan a controlar las transiciones entre sueño y vigilia. El estudio también demuestra una receta práctica para electrodos cerebrales duraderos, suaves y muy sensibles basada en un recubrimiento PEDOT:PSS/PDA. Para el público general, la conclusión es doble: ahora tenemos evidencia más clara de que un centro profundo de recompensa participa activamente en la configuración de nuestro sueño, y disponemos de una tecnología prometedora para sensores cerebrales de larga duración que algún día podría mejorar los tratamientos de los trastornos del sueño y apoyar interfaces cerebro-máquina más fiables.
Cita: Miao, J., Liu, Y., Wang, Y. et al. Highly mechanically stable PEDOT:PSS/PDA-modified microelectrode arrays reveal state-specific dynamic neural activity across sleep-wake. Microsyst Nanoeng 12, 105 (2026). https://doi.org/10.1038/s41378-026-01206-3
Palabras clave: regulación sueño–vigilia, área tegmental ventral, matrices de microelectrodos neuronales, revestimientos de polímero conductor, potenciales de campo local