Clear Sky Science · es
Sistema robótico de transporte de células basado en el modelado de la resistencia de micropipetas
Mover células diminutas sin un microscopio
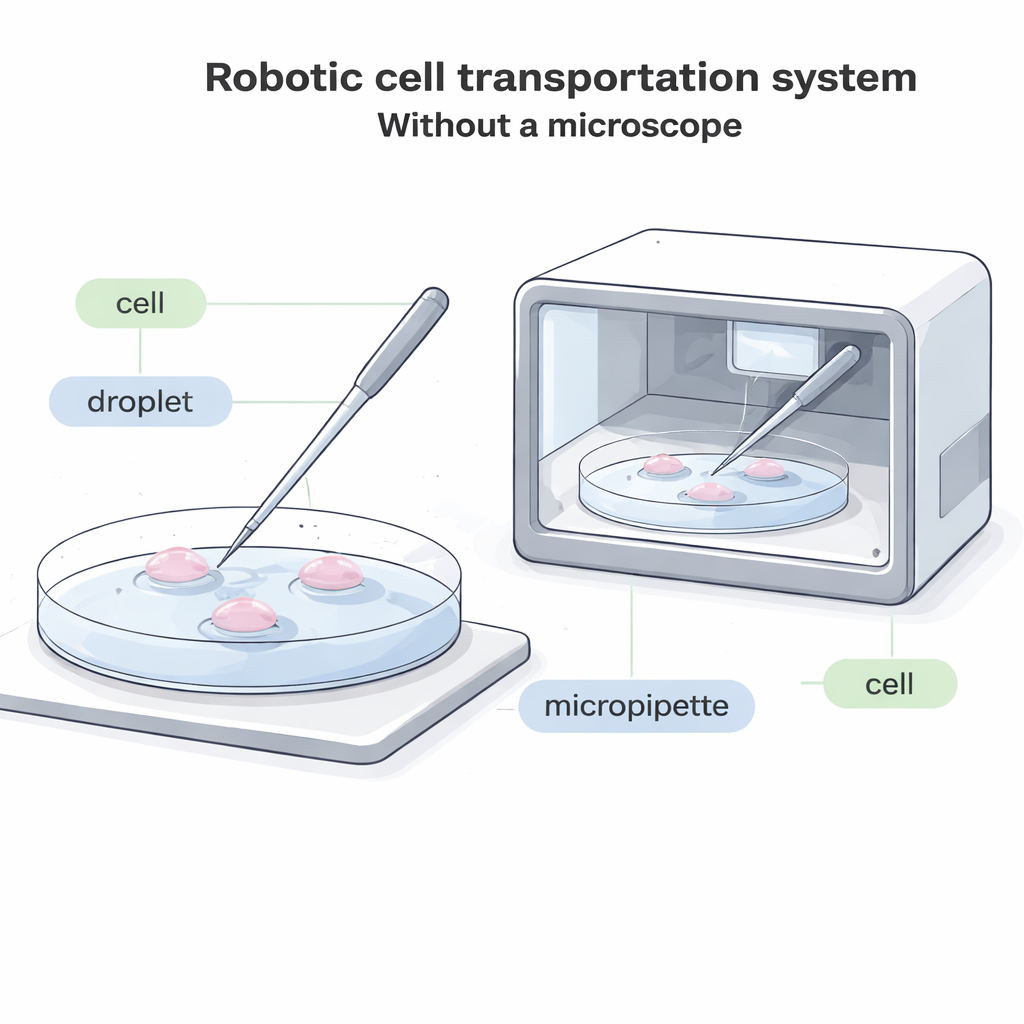
La biología moderna depende a menudo de una tarea sorprendentemente simple: recoger una sola célula con un tubo de vidrio y colocarla en otro sitio. Esto es esencial para tratamientos de fertilidad, congelación de embriones, terapias basadas en células e investigación básica. Sin embargo, hoy en día casi siempre requiere un microscopio voluminoso y un operador humano muy entrenado que supervise cada movimiento. Este artículo describe un nuevo sistema robótico que puede transferir células individuales entre gotas de líquido sin ninguna vista microscópica, abriendo la puerta a “fábricas de células” totalmente cerradas y automatizadas que pueden trabajar más rápido, más barato y con menos daño a células delicadas.
Por qué el traslado de células necesita una renovación
En los laboratorios actuales, un operario mira por un microscopio y usa un tubo delgado de vidrio, llamado micropipeta, para apoyar la punta en el fondo de una placa, aspirar suavemente una célula, desplazarla a una nueva gota de fluido y expulsarla. Este proceso es lento, exige mucha atención visual y es difícil de automatizar. En muchos sistemas futuros —como dispositivos compactos y sellados que cultivan embriones u otras células dentro de una caja— simplemente no hay espacio para un microscopio tradicional. En otros casos, las células están marcadas con tintes fluorescentes que pueden desteñirse o dañarse por la luz, por lo que minimizar la observación microscópica intensa es importante. Los sistemas “a ciegas” existentes que no dependen de imágenes solo funcionan con células inusualmente grandes, dejando a la mayoría de tipos celulares comunes sin una buena solución automática.
Una pajita especial con un tope incorporado
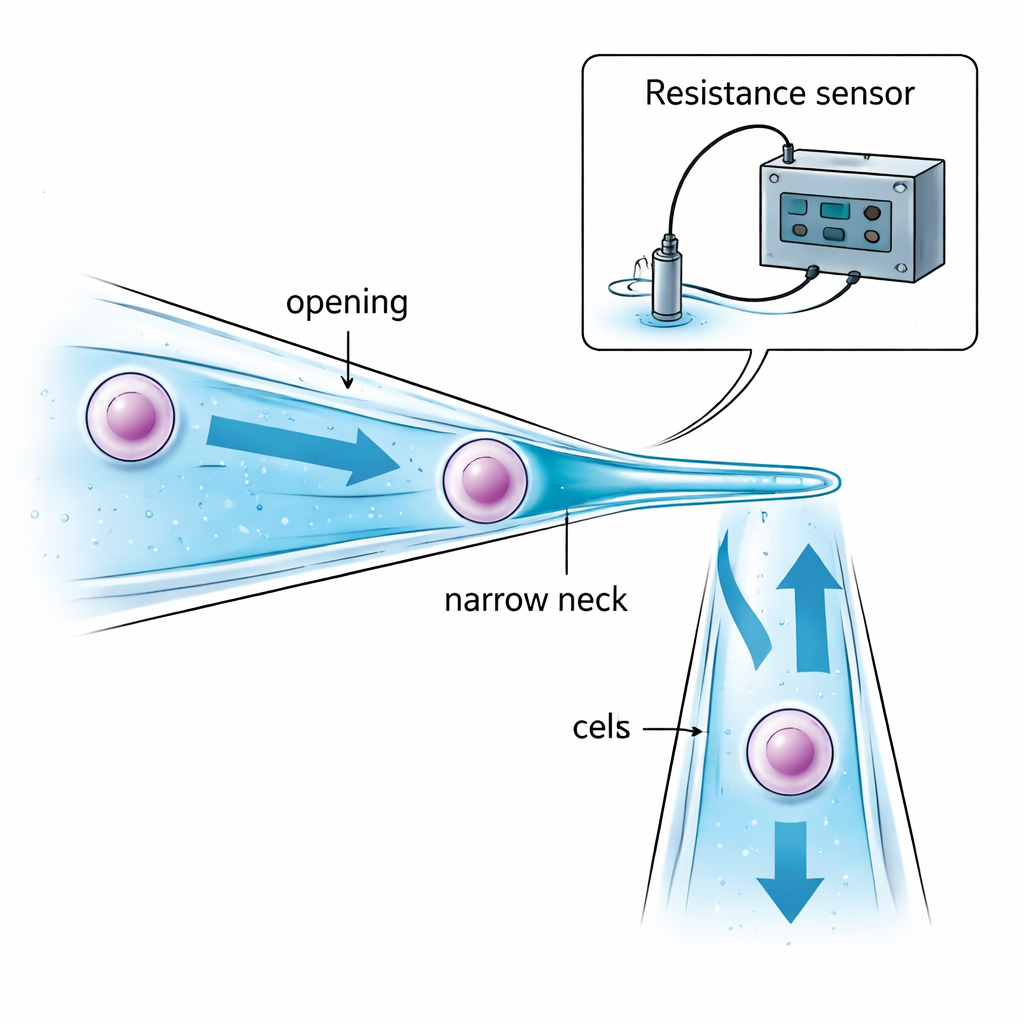
Los autores atacan el problema rediseñando la propia micropipeta. En lugar de un tubo de vidrio recto con el mismo diámetro en toda su longitud, crean una micropipeta con cuello estrecho. Su abertura es ligeramente mayor que la célula objetivo para que esta pueda ser succionada hacia el interior. Más adentro, el tubo se estrecha suavemente hasta formar un “cuello” más pequeño que la célula. Cuando la succión empuja la célula hacia esa constricción, la célula se detiene y queda retenida dentro del tubo —en vez de colgar en la punta y quedar expuesta al aceite o al aire entre gotas. La elección cuidadosa del tamaño de la abertura, el tamaño del cuello y la distancia entre ellos asegura que la célula pueda capturarse de forma segura sin aplastarse en exceso, y que solo se transporte una pequeña cantidad de líquido de una gota a otra, reduciendo la contaminación.
Escuchar señales eléctricas en lugar de mirar
Sin microscopio, el robot aún debe saber tres cosas: cuándo la punta de vidrio está lo suficientemente cerca del fondo de la placa, cuándo la célula ha sido capturada con éxito en el cuello y cuándo se ha liberado por completo en la nueva gota. El equipo resuelve esto monitorizando pequeños cambios en la resistencia eléctrica del líquido dentro y alrededor de la micropipeta. A medida que la pipeta inclinada se aproxima al fondo de la placa, el hueco de líquido entre ambos se reduce y la resistencia eléctrica aumenta de forma predecible, señalando un aterrizaje seguro justo antes del contacto. Cuando una célula bloquea el cuello estrecho, el camino eléctrico a través del líquido se constriñe y la resistencia da un salto repentino; cuando la célula es expulsada, la resistencia cae con la misma brusquedad. Modelos matemáticos de estas resistencias de “hueco”, “aspiración” e “inyección” permiten a un ordenador interpretar estas señales en tiempo real y decidir cuándo detener la succión o la presión, todo sin retroalimentación visual.
Poniendo a prueba el robot
Para comprobar si este enfoque funciona en la práctica, los investigadores construyeron un conjunto robótico completo que combina control de movimiento, control de presión, detección de resistencia y un ordenador anfitrión. Lo probaron con células cancerosas pequeñas conocidas como células HeLa (alrededor de 10 micrómetros de diámetro) y con óvulos porcinos mucho más grandes (unos 150 micrómetros). El sistema pudo detectar de forma fiable el aterrizaje, la captura y la liberación únicamente a partir de señales de resistencia en una amplia gama de tamaños de pipeta. En comparaciones directas, el robot movió células HeLa con un 90 % de éxito —mejor que un método automático anterior basado en visión— y transportó óvulos porcinos con un 95 % de éxito, superior a un enfoque estándar con microscopio. Los tiempos de operación por célula fueron similares o más rápidos que los métodos controlados por humanos, principalmente porque el cuello estrecho elimina la necesidad de ajustar repetidamente la succión para posicionar la célula.
Preservar la viabilidad celular y escalar
Cualquier asistente robótico en el laboratorio de biología debe evitar dañar las células que manipula. Tras el transporte con el nuevo sistema, tanto las células HeLa como los óvulos porcinos se cultivaron durante un día y se tiñeron con un colorante que solo se ilumina en células vivas. Las tasas de supervivencia del nuevo método igualaron o se acercaron a las obtenidas con la transferencia guiada por microscopio y con las células de control sin manipular, lo que indica que el suave apretón mecánico en el cuello estrecho no reduce de forma apreciable la viabilidad celular cuando los umbrales se ajustan correctamente. De cara al futuro, los autores sugieren que la misma detección basada en resistencia y el control de presión pueden integrarse en chips microfluídicos compactos. Eso permitiría que muchos canales operen en paralelo, posibilitando sistemas de manejo celular totalmente cerrados y de alto rendimiento adecuados para medicina reproductiva automatizada, terapias celulares y dispositivos de cultivo a largo plazo donde los microscopios no pueden entrar fácilmente.
Lo que esto significa para el trabajo celular futuro
Para el público general, el mensaje principal es que mover células individuales ya no tiene que depender de una persona mirando por un microscopio. Moldeando cuidadosamente un tubo de vidrio y “escuchando” cómo fluye la electricidad a través del líquido circundante, un robot puede sentir cuándo ha aterrizado, cuándo ha capturado una célula y cuándo la ha soltado —todo a oscuras y en espacios reducidos. Esto hace mucho más práctico diseñar sistemas cerrados y autónomos de cultivo celular que protejan muestras frágiles, simplifiquen los flujos de trabajo clínicos y acerquen la manipulación celular de nivel de laboratorio a una operación automatizada tipo fábrica.
Cita: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Palabras clave: manipulación celular, micropipeta, robótica, microfluidos, automatización