Clear Sky Science · es
Estrategias para controlar la organización espacial celular en sistemas microfisiológicos
Construir tejidos diminutos en el laboratorio
Nuestros órganos funcionan tan bien porque sus células no están dispersas al azar: están cuidadosamente ordenadas en el espacio. Este artículo explora cómo los científicos aprenden a recrear ese orden intrincado dentro de “órganos-en-chips” y otros tejidos miniaturizados cultivados en el laboratorio. Al guiar dónde se sitúan las distintas células y cómo interactúan, los investigadores pueden construir modelos más realistas del corazón, el cerebro, el intestino, los vasos sanguíneos e incluso los ecosistemas humano-microbiano. Estos sistemas avanzados prometen pruebas de fármacos más seguras, menos experimentos con animales y mejores herramientas para estudiar enfermedades y desarrollar tratamientos personalizados.
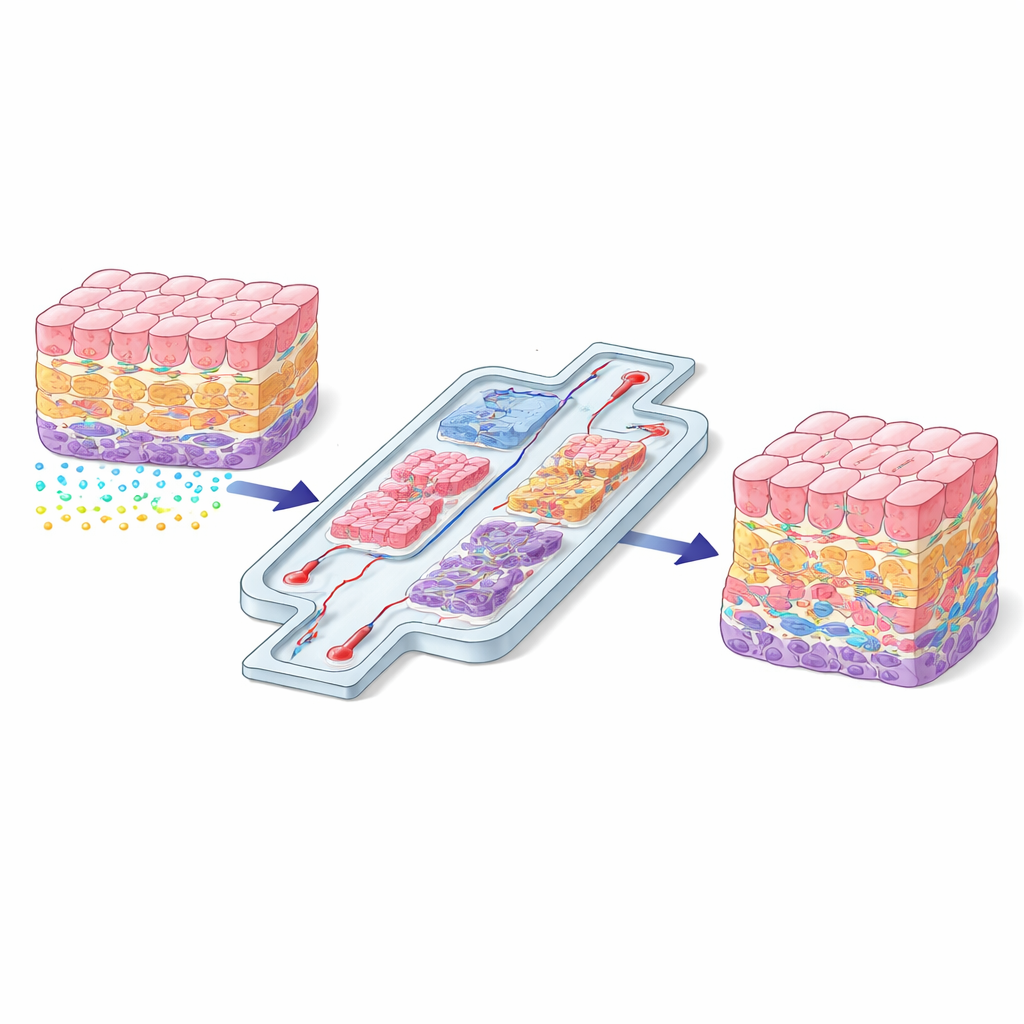
Por qué importa la posición celular
Dentro del cuerpo, cada célula vive en un vecindario específico con su propia mezcla de estructuras de soporte, señales químicas y fuerzas físicas. Una célula hepática cerca de un vaso sanguíneo percibe indicios muy diferentes a los de una célula enterrada en lo profundo del órgano. Estas diferencias de ubicación ayudan a determinar cómo crecen las células, en qué se diferencian y cómo responden a una lesión o a un medicamento. Cuando los científicos cultivan células en placas plásticas planas, esa “conversación” espacial se pierde en gran medida y las células a menudo se comportan de forma poco natural. El artículo sostiene que recrear una organización espacial realista no es una mejora opcional, sino un requisito básico si los tejidos cultivados en el laboratorio han de imitar a los órganos reales.
Dos maneras principales de organizar las células
Los autores agrupan las estrategias actuales en dos familias amplias: control directo e indirecto. Los métodos directos colocan físicamente las células o compartimentos exactamente donde se necesitan. Ejemplos incluyen la bioimpresión 3D, que deposita capas de células y geles blandos como una impresora 3D biológica; chips microfluídicos que tallan tejidos en cámaras y canales conectados; y métodos de captura física que empujan a las células a su posición usando luz, sonido, imanes o campos eléctricos. Estos enfoques son especialmente útiles cuando la geometría precisa es crucial —por ejemplo, recrear una barrera hematoencefálica, una pared vascular en capas o la trayectoria de flujo del intestino al hígado.
Permitir que las células interpreten su entorno
Los métodos indirectos, en cambio, remodelan el entorno y dejan que las células hagan el resto. Aquí, los científicos ajustan el “paisaje” que las células perciben: la composición del gel circundante, la rigidez y textura de las superficies, y gradientes de sustancias disueltas como factores de crecimiento o fármacos. Moléculas de soporte dispuestas con cuidado pueden hacer que ciertos tipos celulares se asienten en regiones específicas. Hidrogeles inteligentes que se ablandan o liberan señales cuando las células los remodelan fomentan estructuras autoorganizadas como redes vasculares o criptas y vellosidades similares a las del intestino. Los dispositivos microfluídicos pueden generar gradientes químicas estables que provocan que células madre adopten identidades distintas a lo largo de un canal, o que células tumorales y del sistema inmune migren a zonas separadas, revelando cómo se propagan las enfermedades.
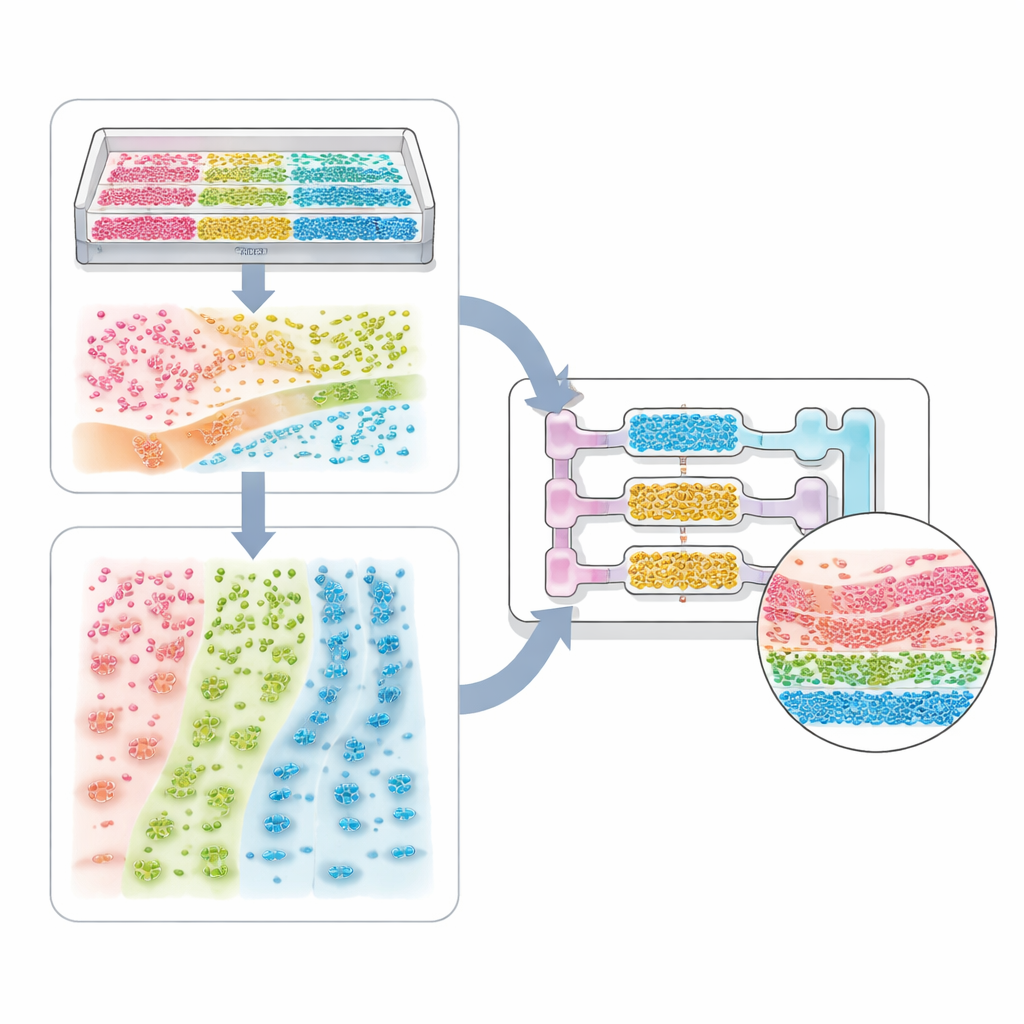
De sistemas de una sola célula a modelos de todo el cuerpo
La revisión recorre un espectro de aplicaciones. En el extremo más simple están los sistemas de un solo tipo celular, donde surcos patrón o gradientes de rigidez pueden hacer que las células cardíacas latan al unísono o que las neuronas extiendan fibras alineadas. Modelos tisulares más complejos mezclan varios tipos celulares —como células tumorales, células de soporte y células vasculares— para formar esferoides y organoides con núcleos y capas internas. Los microcanales y la bioimpresión añaden límites y flujo, permitiendo recrear sacos aéreos pulmonares, filtros renales, zonas hepáticas y circuitos multi-órgano que siguen cómo un fármaco se absorbe, transforma y elimina. Las mismas ideas se extienden a sistemas huésped-microbio, donde la disposición espacial de las bacterias a lo largo de la pared intestinal, o a través de una capa de moco, puede determinar si nos protegen o nos causan enfermedad.
Comprobar que los patrones son reales
Dado que estos sistemas se vuelven más intrincados, los científicos necesitan formas fiables de confirmar que las células acaban donde deben y se comportan como se espera. El artículo destaca métodos de imagen que pueden observar células vivas moverse y cambiar con el tiempo, así como técnicas avanzadas de tinción y secuenciación que cartografían qué genes, proteínas y metabolitos aparecen en cada ubicación. Sensores integrados en los chips pueden rastrear oxígeno, nutrientes, ácidos y fuerzas mecánicas, relacionando las condiciones locales con las respuestas celulares. En conjunto, estas herramientas ayudan a los investigadores a verificar que un diseño no solo sea convincente a nivel visual, sino fiel en su función respecto al tejido real.
Hacia dónde se dirige este trabajo
Los autores concluyen que los sistemas más potentes combinarán estrategias directas e indirectas: usar chips y bioimpresoras para establecer la distribución general, y luego incorporar geles, texturas y gradientes ajustables que permitan que los tejidos maduren y se remodelen con el tiempo. También señalan obstáculos prácticos —como escalar la fabricación, reducir la variabilidad entre laboratorios y abordar cuestiones éticas en torno a modelos humanos complejos—. Aun así, el mensaje es claro: dominar la organización espacial es clave para convertir los sistemas microfisiológicos en sustitutos fiables de órganos humanos, abriendo nuevas puertas para estudiar el desarrollo, evaluar terapias y personalizar la medicina para cada paciente.
Cita: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Palabras clave: órgano-en-un-chip, organización espacial celular, bioimpresión 3D, modelos tisulares microfluídicos, sistemas microfisiológicos