Clear Sky Science · es
Plataforma de punto de atención CRISPR en un solo paso para la detección rápida, específica y sensible de HPV 16 sin preamplificación
Por qué identificar un tipo de virus importa de verdad
El cáncer de cuello uterino suele estar relacionado con la infección por papilomavirus humanos (VPH), pero no todos los tipos de VPH conllevan el mismo riesgo. Por eso los médicos necesitan pruebas que diferencien con fiabilidad estos virus muy similares, en especial el tipo de alto riesgo denominado VPH16. El problema es que las pruebas genéticas actuales a veces confunden parientes cercanos, lo que conduce a falsas alarmas o a casos no detectados. Este estudio presenta un nuevo método de análisis que mejora notablemente tanto la precisión como la practicidad, con el objetivo de llevar la subtipificación precisa de VPH a clínicas y entornos de punto de atención.
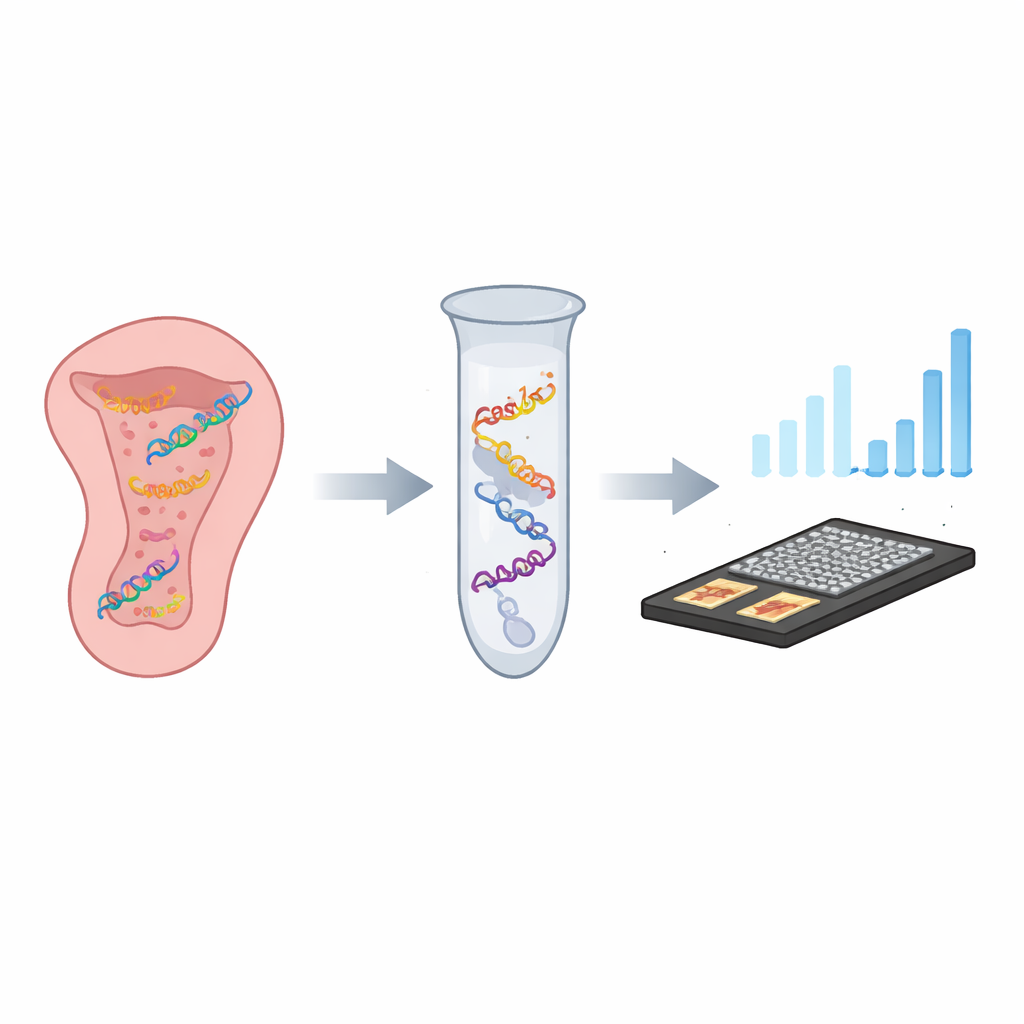
Un candado molecular inteligente
Los investigadores desarrollaron una prueba en un solo tubo que denominan CASTSA y que combina dos ideas potentes: la precisión del CRISPR, un sistema de localización genética adaptado de bacterias, y la capacidad de amplificación de la PCR, el método estándar para copiar ADN. En CASTSA, una proteína CRISPR llamada Cas12a es guiada hacia la secuencia genética de VPH16 por medio de un pequeño ARN “llave”. Cuando encuentra la coincidencia exacta y un patrón corto cercano que requiere, Cas12a corta el ADN viral en un punto predecible. Ese corte genera un extremo característico en una hebra de ADN que actúa como punto de partida único para la amplificación. Otros tipos de VPH, aunque tengan secuencias muy parecidas, o bien no son cortados o bien no generan el punto de inicio correcto, por lo que no se amplifican.
Convertir un pequeño corte en una señal potente
Para transformar ese corte de CRISPR en una señal detectable, el equipo diseñó un cebador de ADN especial llamado cebador terminal‑específico. Este cebador solo se une correctamente a la hebra producida por el corte de Cas12a, luego se pliega sobre sí mismo como una horquilla y ayuda a formar una plantilla estable para la PCR. Secuencias adicionales de cebadores “universales” se acoplan después y desencadenan una reacción convencional de PCR en tiempo real. De forma crucial, la amplificación solo ocurre si Cas12a ha actuado antes y si el cebador se pliega correctamente, creando dos capas de verificación. Esta arquitectura reduce drásticamente la posibilidad de que ADN parcialmente coincidente y no objetivo se amplifique por error, resolviendo una debilidad común de pruebas CRISPR previas que dependían de un paso separado de preamplificación.
Todo en un solo tubo, con menos errores
Un avance práctico clave es que el corte por CRISPR y la amplificación por PCR ocurren juntos en el mismo tubo sellado, evitando la necesidad de abrir los tubos entre pasos, una fuente principal de contaminación en muchos flujos de trabajo de laboratorio. Los autores ajustaron cuidadosamente las condiciones de reacción, especialmente los niveles de magnesio, para que tanto Cas12a como la enzima copiante de ADN funcionen bien sin favorecer reacciones espurias. Demostraron que su configuración en un solo tubo puede distinguir fielmente VPH16 de varios otros tipos de alto riesgo, incluidos VPH18, 33, 45 y 52, a pesar de que estos virus comparten regiones genéticas muy conservadas. En comparación con la PCR en tiempo real estándar sola, o con pruebas CRISPR que primero amplifican el ADN y luego realizan la detección CRISPR, CASTSA produjo muchas menos señales engañosas procedentes de tipos de VPH no objetivo.
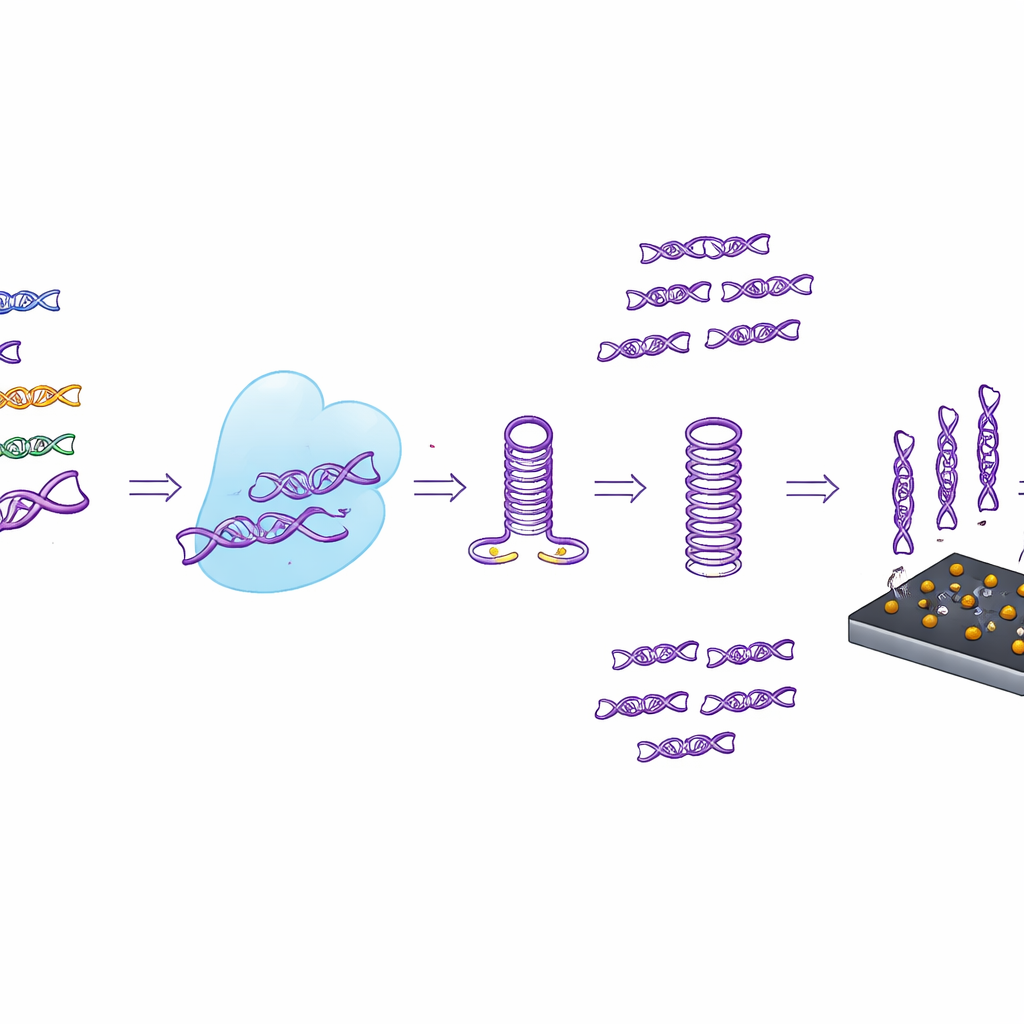
Del tubo de ensayo al sensor de mano
En lugar de depender solo de lecturas fluorescentes, los investigadores también acoplaron CASTSA a un sensor electroquímico compacto fabricado con grafeno inducido por láser. Esta superficie de carbono porosa y altamente conductora está decorada con nanopartículas de oro que llevan hebras de captura diseñadas para unirse únicamente a los productos de amplificación CASTSA de VPH16. Cuando estos productos se adhieren, la corriente eléctrica a través del sensor cambia de forma medible. Al usar una matriz de cuatro electrodos—tres puntos de medida y un control de fondo incorporado—el dispositivo puede restar el ruido debido a adherencias no específicas. En los ensayos, este sistema integrado detectó tan solo 18 copias del objetivo VPH16 por reacción, superando la sensibilidad de la fluorescencia sola y manteniendo una excelente repetibilidad.
Cómo esto podría cambiar las pruebas de VPH
Para evaluar el rendimiento en condiciones reales, el equipo probó 20 muestras clínicas conocidas por contener VPH16 y 10 muestras de donantes sanos. CASTSA, tanto en su formato de fluorescencia como cuando se combinó con el sensor basado en grafeno, coincidió completamente con las pruebas PCR hospitalarias estándar. Al mismo tiempo, mostró una mayor capacidad para ignorar otros tipos de VPH de alto riesgo que suelen causar confusión. Para los pacientes, esto podría traducirse en menos resultados ambiguos y decisiones más seguras sobre seguimiento y tratamiento. En términos más amplios, la estrategia CASTSA—reconocimiento CRISPR primero, amplificación después, todo en un tubo sellado—ofrece un modelo para pruebas genéticas altamente específicas y con baja contaminación que podría adaptarse a muchos patógenos y mutaciones, especialmente en entornos que exigen respuestas rápidas y fiables.
Cita: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Palabras clave: Detección de HPV16, Diagnósticos CRISPR, Pruebas basadas en PCR, Biosensor electroquímico, Ensayo punto de atención