Clear Sky Science · es
Microscopía de barrido por imagen interferométrica para obtención de imágenes sin marcadores con 120 nm de resolución lateral dentro de células vivas
Ver células vivas sin tintes añadidos
La biología moderna suele apoyarse en etiquetas fluorescentes que brillan para revelar la arquitectura oculta dentro de las células. Pero esas etiquetas pueden estresar a las células, alterar su comportamiento y, en ocasiones, no ser utilizables en muestras frágiles o difíciles de manipular genéticamente. Este artículo presenta una forma nueva de observar lo que ocurre dentro de células vivas con alto detalle—aunque sin añadir tintes ni etiquetas genéticas—prometiendo observaciones más suaves, más duraderas y más naturales de cómo funcionan realmente las células.
Observar las células por cómo dispersan la luz
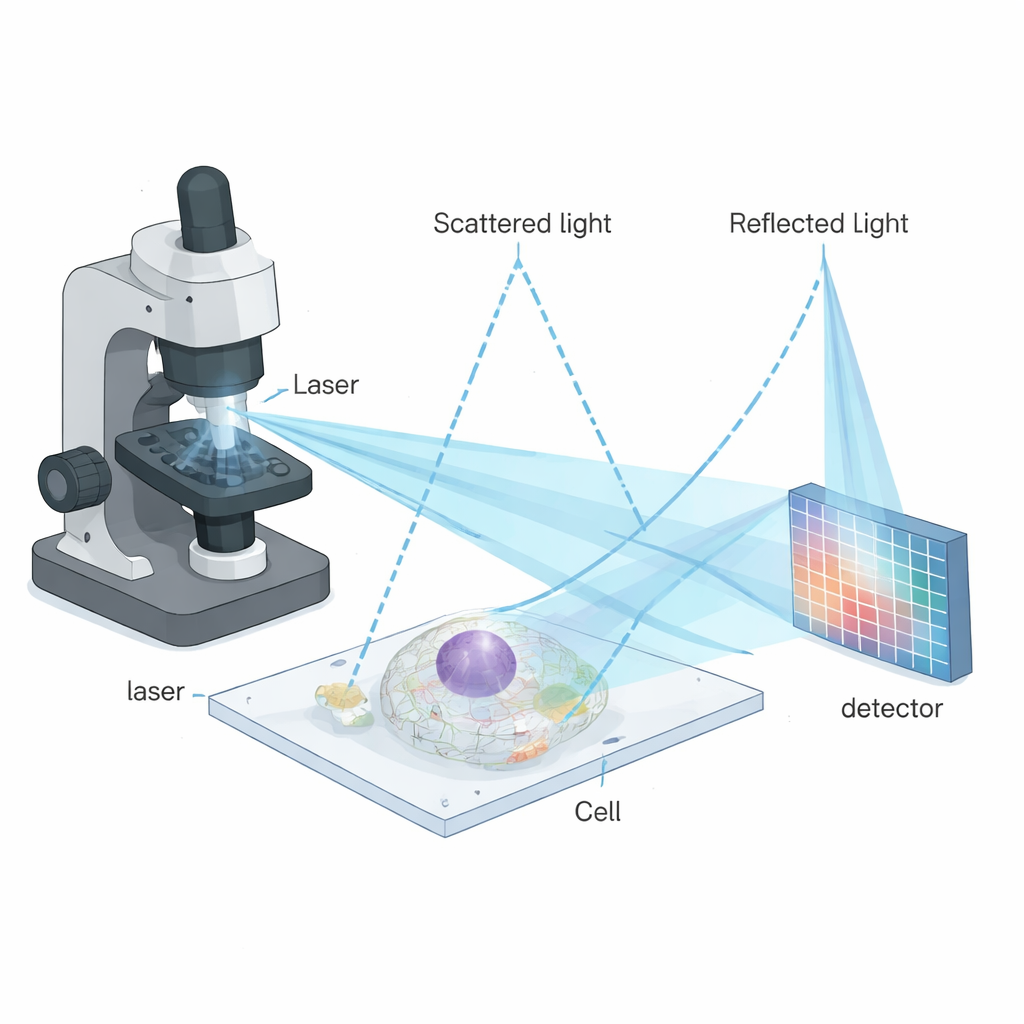
El método se apoya en una familia de técnicas que no dependen de la fluorescencia, sino que miden cómo pequeñas estructuras dispersan la luz. Una de esas técnicas, la microscopía por dispersión interferométrica (iSCAT), mezcla la luz dispersada por un objeto a escala nanométrica con una reflexión de referencia desde una superficie de vidrio. El patrón de interferencia resultante es extremadamente sensible a partículas muy pequeñas como proteínas, virus o vesículas. iSCAT ha funcionado mejor en muestras simples y limpias, como partículas aisladas sobre vidrio. Sin embargo, aplicarla en el interior profundo de células vivas ha sido difícil porque las células son densas y desordenadas: muchos eventos de dispersión superpuestos generan un fondo moteado que oculta los detalles finos.
Combinar dos ideas para una imagen más nítida y menos agresiva
Para superar estas limitaciones, los autores combinaron iSCAT con una poderosa estrategia de imagen llamada microscopía por barrido de imagen (ISM). En ISM, la muestra se explora punto por punto con un haz focalizado y, en lugar de usar un único detector, una matriz de píxeles detectores registra muchas vistas ligeramente desplazadas de cada punto. Mediante una realineación y combinación ingeniosa de estas vistas, se puede afinar la imagen final sin desperdiciar fotones valiosos. La nueva técnica—microscopía de barrido por imagen interferométrica, o iISM—adapta esta idea a las señales más complejas y sensibles a la fase de la dispersión interferométrica. El microscopio usa un láser azul, óptica especial para hacer simétrica la polarización de la luz y una cámara sensible para registrar la luz dispersada y reflejada en cada posición de barrido. Un flujo de trabajo computacional a medida reasigna luego la información de los píxeles de manera que respeta la naturaleza ondulatoria de la señal, produciendo imágenes con unos 120 nanómetros de resolución lateral, aproximadamente el doble de finas que la óptica limitada por difracción convencional.
Algoritmos inteligentes convierten patrones ruidosos en imágenes claras
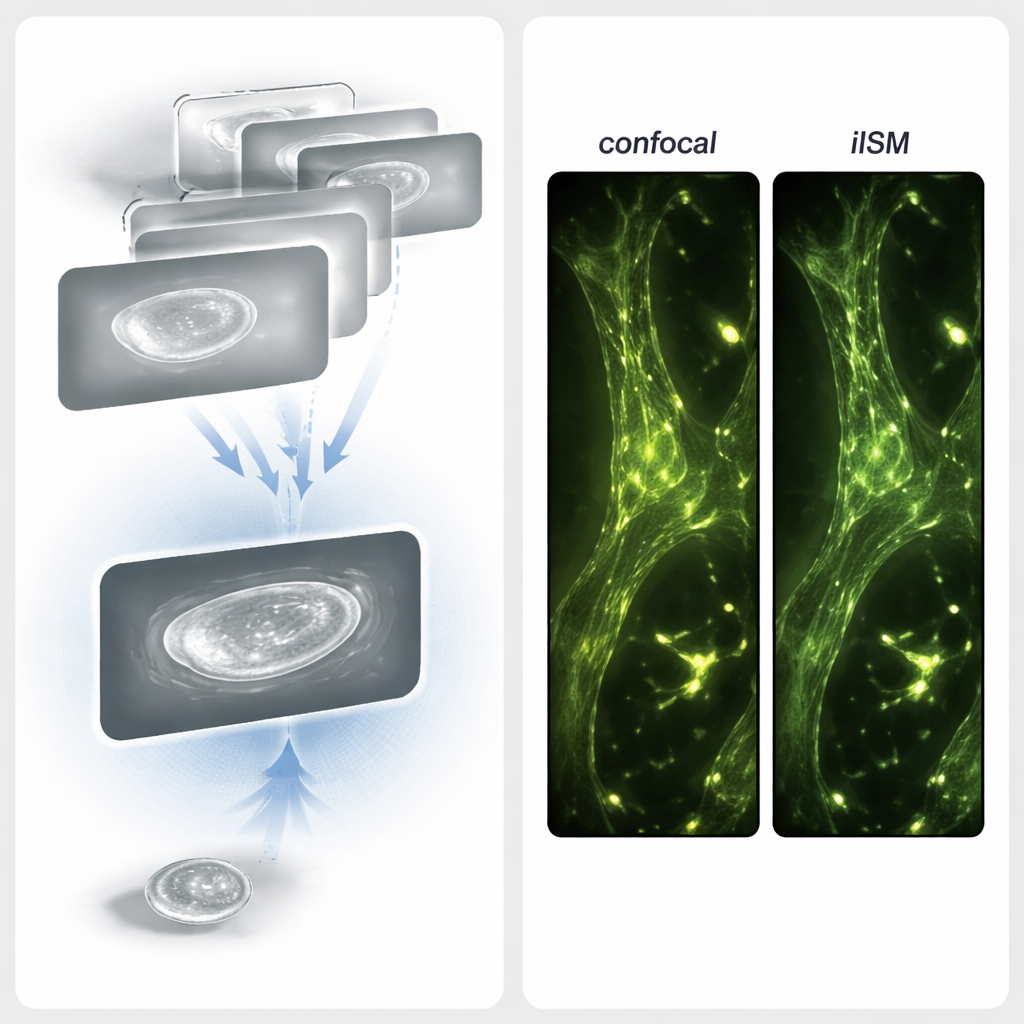
Porque las señales interferométricas llevan información tanto de intensidad como de fase, los trucos de procesamiento habituales en imágenes de fluorescencia no son suficientes. Los autores diseñaron un procedimiento de reasignación adaptativa de píxeles (APR) adaptado para luz coherente. Primero, transforman cada pequeño patrón interferométrico en un mapa de “varianza radial” que destaca centros de simetría sin importar si la señal es positiva o negativa. Este paso convierte de forma efectiva las franjas de interferencia complicadas en imágenes que se comportan más como imágenes de intensidad convencionales. Luego, usando software de código abierto, determinan cuánto está desplazada la imagen de cada píxel del detector respecto al centro y las desplazan de vuelta antes de sumarlas. Esta alineación refinada concentra la señal útil mientras promedia el ruido, aumentando la relación contraste-ruido en torno a un factor de cuatro respecto a una imagen confocal iSCAT con un pinhole estrecho, todo con el mismo nivel de iluminación.
Observar orgánulos y citoesqueletos en acción
Con estos avances técnicos, el equipo probó iISM en células COS-7 vivas para evaluar su rendimiento en la práctica. Con una iluminación muy baja—alrededor de diez veces menor por punto focal que la que suelen usar los microscopios confocales convencionales—pudieron distinguir claramente orgánulos clave: el retículo endoplásmico, mitocondrias, vesículas, el citoesqueleto de actina, la membrana plasmática y estructuras delanteras finas llamadas lamelipodios. Debido a que el contraste interferométrico depende de la posición vertical, orgánulos similares podían aparecer con contraste positivo o negativo, revelando sutiles diferencias de altura de solo unos pocos cientos de nanómetros. Al grabar secuencias temporales, siguieron vesículas en movimiento y el remodelado de túbulos del retículo endoplásmico durante muchos minutos, sin daño fotoinducido evidente ni indicios de que la propia imagen perturbara el comportamiento celular.
Comparar vistas sin marcadores con mapas fluorescentes
Para comprobar que las imágenes sin marcadores reflejaban realmente estructuras celulares, los investigadores también realizaron mediciones combinadas de iISM y ISM de fluorescencia en células fijadas. Tiñeron el citoesqueleto de actina con un tinte fluorescente rojo y registraron imágenes de fluorescencia superresueltas junto con imágenes sin marcadores de iISM de la misma región. Al superponer ambas, los filamentos brillantes de actina en el canal de fluorescencia coincidían estrechamente con las características filamentosas en las imágenes iISM. En algunas regiones, iISM incluso reveló detalles de dispersión adicionales—como variaciones a lo largo de los filamentos o estructuras no marcadas cercanas, por ejemplo adhesiones focales—que eran invisibles en el canal de fluorescencia. En conjunto, estos resultados muestran que iISM puede tanto confirmar estructuras conocidas como descubrir información extra sobre el entorno no marcado.
Una nueva ventana a las células, con menos perturbación
Para el público general, el mensaje clave es que iISM ofrece una forma de ver detalles finos dentro de células vivas sin hacerlas brillar artificialmente. Combina la sensibilidad de la dispersión interferométrica con el poder de afinamiento de la microscopía por barrido de imagen, logrando aproximadamente 120 nanómetros de resolución mientras usa mucha menos luz que muchos microscopios existentes. Como está construido con componentes ya comunes en sistemas confocales avanzados, en principio puede añadirse a instrumentos comerciales. En el futuro, iISM podría combinarse con fluorescencia tradicional, detectores rápidos o incluso “teñidos virtuales” por aprendizaje automático para seguir infecciones, transporte de cargas o reorganizaciones del citoesqueleto en condiciones más cercanas al estado natural y no perturbado de las células.
Cita: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Palabras clave: imagen sin marcadores, microscopía en células vivas, dispersión interferométrica, superresolución, orgánulos celulares