Clear Sky Science · es
Letalidad sintética de la inhibición de MCL-1 y la terapia CAR-T en el linfoma B agresivo
Por qué esto importa para el tratamiento del cáncer
Los linfomas B agresivos son cánceres sanguíneos de crecimiento rápido que con frecuencia reaparecen después del tratamiento. Incluso enfoques novedosos y potentes como la terapia CAR-T, que reprograma las propias células inmunitarias del paciente para atacar el cáncer, fracasan en aproximadamente la mitad de los pacientes con el tiempo. Este estudio explora una manera de convertir esa vulnerabilidad en una fortaleza: usar un fármaco que apunta a una proteína clave de supervivencia en las células del linfoma para tanto matar tumores como hacer que las células restantes sean más fáciles de eliminar por las células CAR-T.
El problema de las células de linfoma persistentes
Los linfomas B agresivos están frecuentemente impulsados por la actividad excesiva de un gen llamado MYC, que empuja a las células a dividirse rápidamente y también las ayuda a ocultarse del sistema inmune. Los tratamientos estándar e incluso la terapia CAR-T pueden dejar pequeños focos de células de linfoma que toleran los fármacos y más tarde causan recaída. Estas células “persister” y resistentes viven en un vecindario tumoral lleno de células inmunes supresoras que mantienen a las células T asesinas a raya. Los autores se preguntaron si bloquear MCL-1, una proteína de la que dependen las células del linfoma para evitar autodestruirse, podría exponer una debilidad oculta en este sistema.
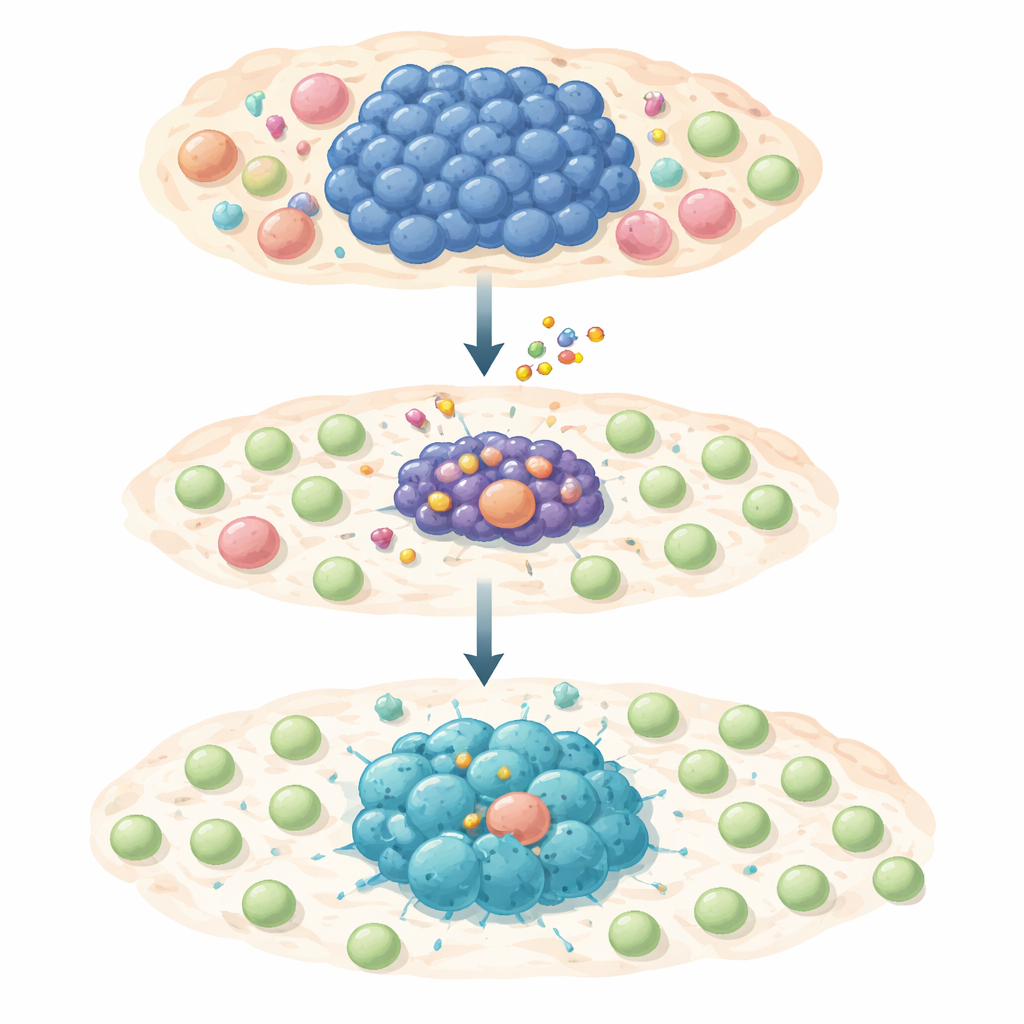
Un ataque en dos pasos contra la supervivencia y el ocultamiento del tumor
El equipo probó un fármaco selectivo bloqueador de MCL-1, S63845, en un amplio panel de líneas celulares humanas de linfoma dependientes de MYC. La mayoría de estas células cancerosas fueron muy sensibles al fármaco y sufrieron muerte programada cuando se bloqueó MCL-1. Sin embargo, una pequeña fracción sobrevivió a exposiciones a corto o largo plazo y se volvió tolerante al fármaco o completamente resistente. Al examinar en detalle a estos sobrevivientes, los investigadores encontraron que la actividad de MYC estaba atenuada mientras que otra molécula, STAT1, y su vía de alarma de interferón estaban activadas. Este cambio encendió genes que promueven señales inflamatorias y quimiocinas—“destellos” moleculares que pueden atraer células T hacia la zona tumoral.
Reavivar el vecindario inmunológico
Para ver cómo se manifiesta esto en un organismo vivo, los autores trataron ratones portadores de linfomas impulsados por MYC con una dosis baja del inhibidor de MCL-1. El fármaco redujo la carga tumoral mientras respetaba las células B normales, pero su impacto fue más allá de la simple reducción de masa. Los tumores tratados mostraron más células T CD4 y CD8, menos células T exhaustas, menos células T regulatorias y menos células mieloides supresoras, todas señales de un entorno más favorable para la respuesta inmune. Secuenciación de ARN de célula única de las células tumorales y circundantes confirmó que las células de linfoma residuales presentaban menor MYC, aumento de STAT1 y señales más fuertes de interferón e inflamación, mientras que el tejido circundante fue repoblado por células T y células natural killer activas en lugar de células supresoras.
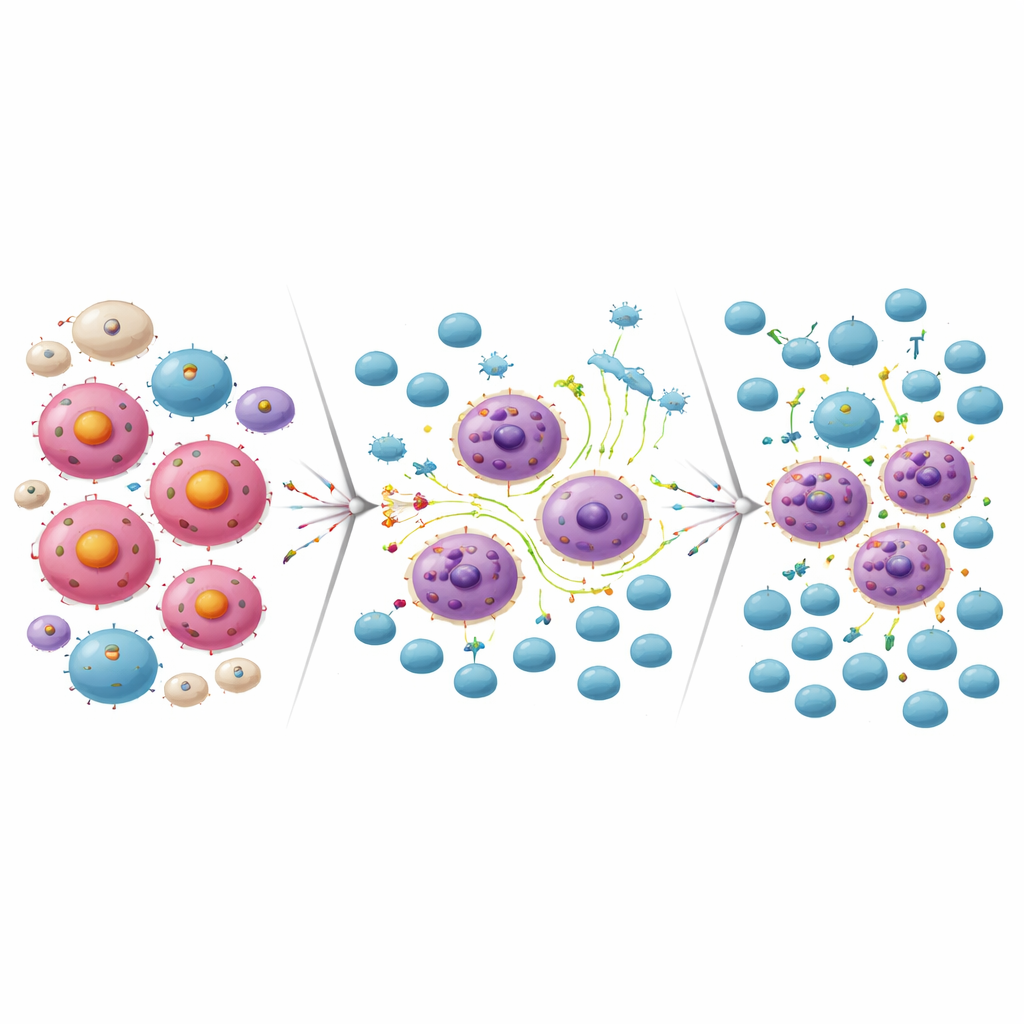
Convertir la resistencia en una oportunidad para las células CAR-T
La misma reprogramación inflamatoria que ayudó a algunas células del linfoma a sobrevivir al bloqueo de MCL-1 también las hizo más vulnerables al ataque inmune. En el laboratorio, las células CAR-T dirigidas a CD19 mataron de manera eficiente a las células de linfoma que se habían vuelto resistentes al fármaco contra MCL-1. A la inversa, las células de linfoma que se habían hecho resistentes a la terapia CAR-T contra CD19 resultaron altamente sensibles al inhibidor de MCL-1. Cuando los investigadores combinaron una dosis subletal del fármaco de MCL-1 con células CAR-T en cultivo celular, los dos tratamientos juntos eliminaron muchas más células de linfoma que cualquiera de los dos por separado. En modelos murinos, administrar el inhibidor de MCL-1 seguido de células CAR-T contra CD19 condujo a una eliminación tumoral casi completa y a una supervivencia significativamente más larga en comparación con los tratamientos individuales.
Un golpe doble con potencial curativo
En pocas palabras, el estudio sugiere una estrategia de “golpe doble”. Primero, un fármaco que bloquea MCL-1 reduce la mayor parte del linfoma y obliga a las células cancerosas supervivientes a entrar en un estado inflamado y altamente visible que atrae a las células T y les quita sus escudos protectores. Segundo, las células CAR-T contra CD19 explotan esta debilidad recién expuesta para erradicar la enfermedad restante. Al atacar tanto el cableado interno de supervivencia del tumor como su vecindario protector, este enfoque combinado podría reducir las recaídas y acercar a los linfomas B agresivos a una remisión duradera.
Cita: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Palabras clave: Linfoma B, Terapia CAR-T, Inhibición de MCL-1, Microambiente tumoral, Resistencia a fármacos